Clear Sky Science · es
Eje TGF-β/SMAD4/14-3-3σ/TFEB promueve la transición mesenquimal-epitelial e inhibe la autofagia en el cáncer colorrectal
Por qué este estudio importa para el cáncer de colon
El cáncer colorrectal es una de las principales causas de muerte por cáncer porque las células tumorales con frecuencia se diseminan desde el intestino a órganos distantes. Este estudio descubre un circuito de seguridad hasta ahora desconocido dentro de las células intestinales que puede frenar esa diseminación. Al cartografiar cómo varias moléculas se comunican entre sí, los investigadores muestran cómo señales normales en el intestino pueden empujar a las células cancerosas de vuelta hacia un estado más ordenado y cortar uno de sus trucos de supervivencia, un proceso de autorreciclaje llamado autofagia.
Un mensaje protector en el intestino
Nuestros intestinos están constantemente expuestos a alimentos, bacterias y estrés mecánico, por lo que las células del epitelio intestinal dependen de sistemas de control robustos para mantener el crecimiento y la reparación en equilibrio. Una señal principal, llamada TGF‑β, actúa habitualmente como freno en el desarrollo tumoral temprano. Funciona a través de una proteína llamada SMAD4, que se traslada al núcleo celular y enciende o apaga genes. En los cánceres colorrectales, SMAD4 se pierde con frecuencia, y los pacientes cuyos tumores carecen de esta proteína tienden a presentar más metástasis y peor supervivencia. Los autores se propusieron entender qué genes específicos controla SMAD4 que podrían explicar su capacidad para bloquear la invasión y la diseminación.
Una cadena de guardianes dentro de las células cancerosas
El equipo descubrió que SMAD4 activa directamente un gen llamado 14‑3‑3σ, conocido desde hace tiempo como supresor tumoral. Usando líneas celulares humanas de cáncer colorrectal, mini‑tumores derivados de pacientes cultivados en el laboratorio y modelos de ratón, mostraron que la activación de SMAD4 aumenta de forma consistente los niveles de 14‑3‑3σ, mientras que la eliminación de SMAD4 impide ese incremento. Identificaron sitios de unión para SMAD4 en la región reguladora de 14‑3‑3σ y confirmaron que SMAD4 ocupa físicamente esos sitios, estableciendo firmemente a 14‑3‑3σ como diana directa tanto en células intestinales humanas como de ratón. En el intestino normal de ratón, 14‑3‑3σ es especialmente abundante en las puntas de las vellosidades, pero este patrón desaparece cuando Smad4 se elimina, lo que subraya la estrecha relación entre ambos durante la diferenciación tisular.
Empujando a las células cancerosas de vuelta al orden
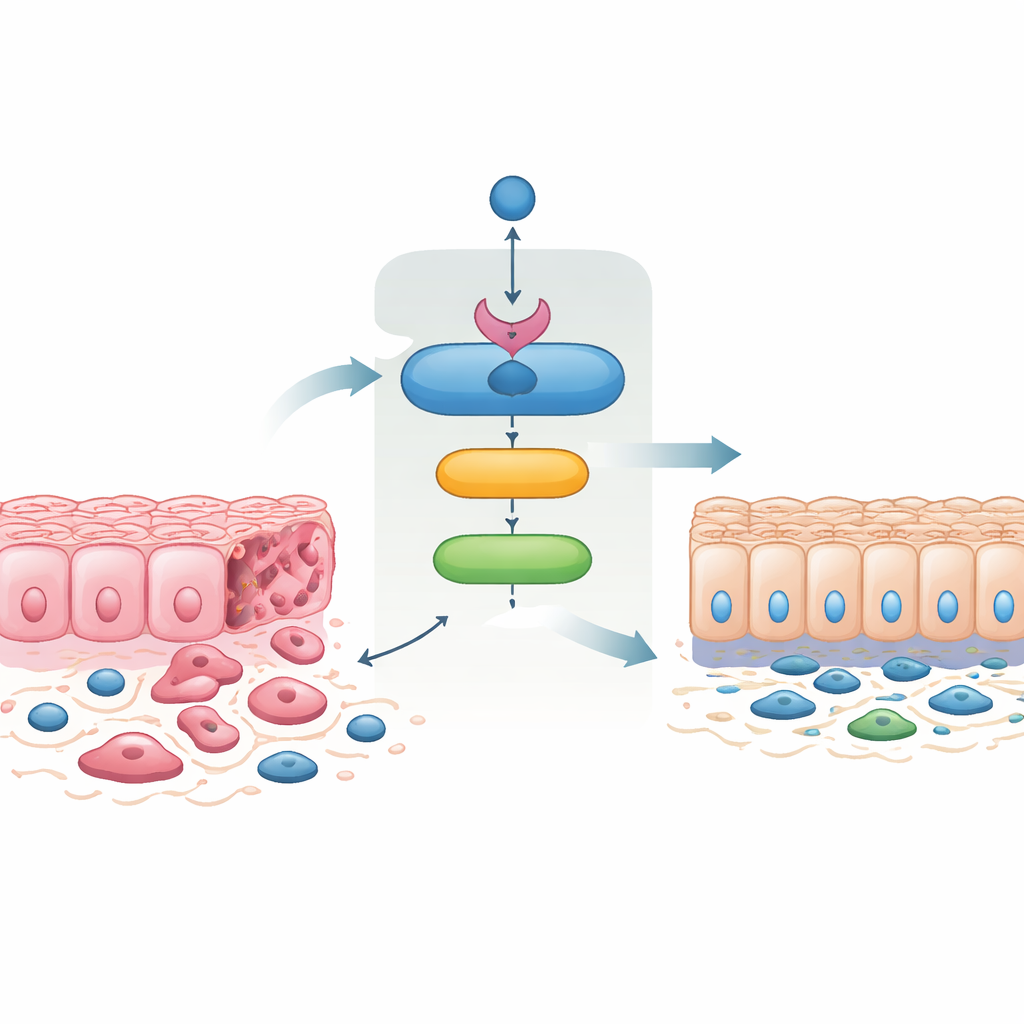
Las células cancerosas a menudo experimentan una "transición epitelial‑mesenquimal", pasando de células estrechamente conectadas en láminas a células más móviles y alargadas que invaden y forman metástasis con mayor facilidad. El proceso inverso, la transición mesenquimal‑epitelial, restaura contactos celulares estrechos y reduce la invasividad. Cuando los investigadores reintrodujeron SMAD4 en células colorrectales agresivas que normalmente carecían de ella, las células cambiaron hacia una apariencia epitelial, recuperaron proteínas de adhesión en la membrana y perdieron rasgos asociados con movilidad e invasión. Estas células con SMAD4 restaurado migraron menos, invadieron menos a través de membranas artificiales y formaron menos colonias. De forma notable, forzar la expresión de 14‑3‑3σ por sí sola produjo cambios muy similares, y bloquear 14‑3‑3σ borró en gran medida los efectos de SMAD4. Esto demuestra que 14‑3‑3σ no es un mero espectador, sino un mediador clave de la capacidad de SMAD4 para domar el comportamiento invasivo.
Apagando una vía de supervivencia
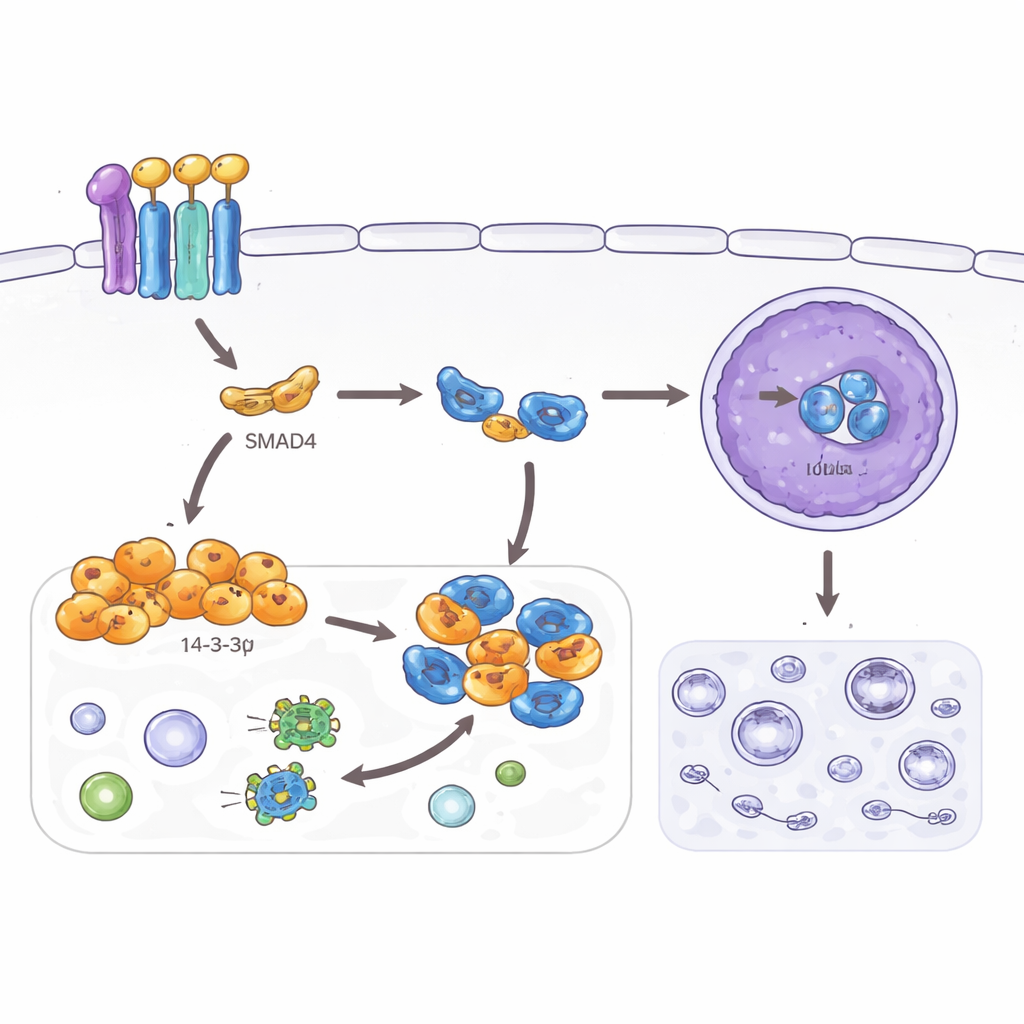
El estudio también examinó la autofagia, un programa de reciclaje que ayuda a las células a sobrevivir al estrés degradando componentes internos. Aunque útil en tejidos normales, una autofagia elevada puede ayudar a las células cancerosas a sobrellevar entornos hostiles y los tratamientos. Los autores encontraron que SMAD4 y 14‑3‑3σ reducen marcadores de autofagia en células de cáncer colorrectal y disminuyen el número de vesículas de reciclaje observadas al microscopio. Rastrearon este efecto hasta otra proteína, TFEB, un controlador maestro de la autofagia y de los lisosomas. Normalmente, cuando TFEB entra en el núcleo activa muchos genes relacionados con la autofagia. Aquí, 14‑3‑3σ inducido por SMAD4 se une a TFEB en el compartimento citoplasmático y evita que llegue al núcleo, pero solo cuando un sitio específico en TFEB ha sido etiquetado químicamente. Cuando ese sitio está mutado, 14‑3‑3σ ya no puede retener a TFEB, la autofagia se reanuda y los efectos supresores sobre la invasión y la morfología celular se debilitan.
Qué significa esto para los pacientes
En conjunto, los hallazgos describen un eje protector lineal en el intestino: TGF‑β activa SMAD4, SMAD4 enciende 14‑3‑3σ, y 14‑3‑3σ atrapa a TFEB fuera del núcleo. Esta combinación empuja a las células de cáncer colorrectal hacia un estado más ordenado y menos móvil y atenúa su maquinaria de autorreciclaje, lo que podría hacerlas menos capaces de diseminarse y más vulnerables al tratamiento. Cuando SMAD4 o 14‑3‑3σ se pierden, TFEB se vuelve más activo, lo que podría aumentar tanto la plasticidad celular como la resistencia al estrés. Aunque se necesitan más estudios en animales vivos y muestras clínicas, la vía revelada aquí destaca nuevos puntos moleculares donde futuros fármacos podrían reforzar las propias defensas del organismo contra el cáncer colorrectal metastásico.
Cita: Chen, X., Winter, M., Rokavec, M. et al. TGF-β/SMAD4/14-3-3σ/TFEB axis promotes mesenchymal-epithelial transition and inhibits autophagy in colorectal cancer. Cell Death Dis 17, 397 (2026). https://doi.org/10.1038/s41419-026-08733-x
Palabras clave: cáncer colorrectal, metástasis, autofagia, plasticidad epitelial, TFEB