Clear Sky Science · ar
محور TGF-β/SMAD4/14-3-3σ/TFEB يعزّز الانتقال من النسج إلى الطلائي ويثبط الالتهام الذاتي في سرطان القولون والمستقيم
لماذا تهم هذه الدراسة سرطان القولون
يُعد سرطان القولون والمستقيم من الأسباب الرئيسية لوفيات السرطان لأن خلايا الورم غالبًا ما تنتشر من الأمعاء إلى أعضاء بعيدة. تكشف هذه الدراسة عن دائرة أمان داخل خلايا الأمعاء لم تكن معروفة سابقًا ويمكن أن تكبح هذه الانتشار. عبر تتبع كيفية تواصل عدة جزيئات مع بعضها، يبيّن الباحثون كيف يمكن للإشارات الطبيعية في الأمعاء أن تدفع خلايا السرطان للعودة إلى حالة أكثر انتظامًا وتقطع إحدى حيل بقائها، وهي عملية التنظيف الذاتي المعروفة بالالتهام الذاتي.
رسالة وقائية في الأمعاء
تتعرض أمعاتنا باستمرار للطعام والبكتيريا والإجهاد الميكانيكي، لذا تعتمد خلايا الأمعاء على أنظمة رقابة قوية للحفاظ على التوازن بين النمو والإصلاح. إشارة رئيسية واحدة، تُسمى TGF‑β، تعمل عادة كفرامل في المراحل المبكرة لتطور الورم. تعمل عبر بروتين يُدعى SMAD4، الذي ينتقل إلى نواة الخلية ويشغّل أو يطفئ جينات. في سرطانات القولون والمستقيم يُفقد SMAD4 بشكل متكرر، والمرضى الذين تفتقر أورامهم إلى هذا البروتين يميلون إلى وجود مزيد من الانبثاث وبقاء أسوأ. سعى المؤلفون لفهم أي الجينات المحددة يتحكم بها SMAD4 والتي قد تفسر قدرته على منع الغزو والانتشار.
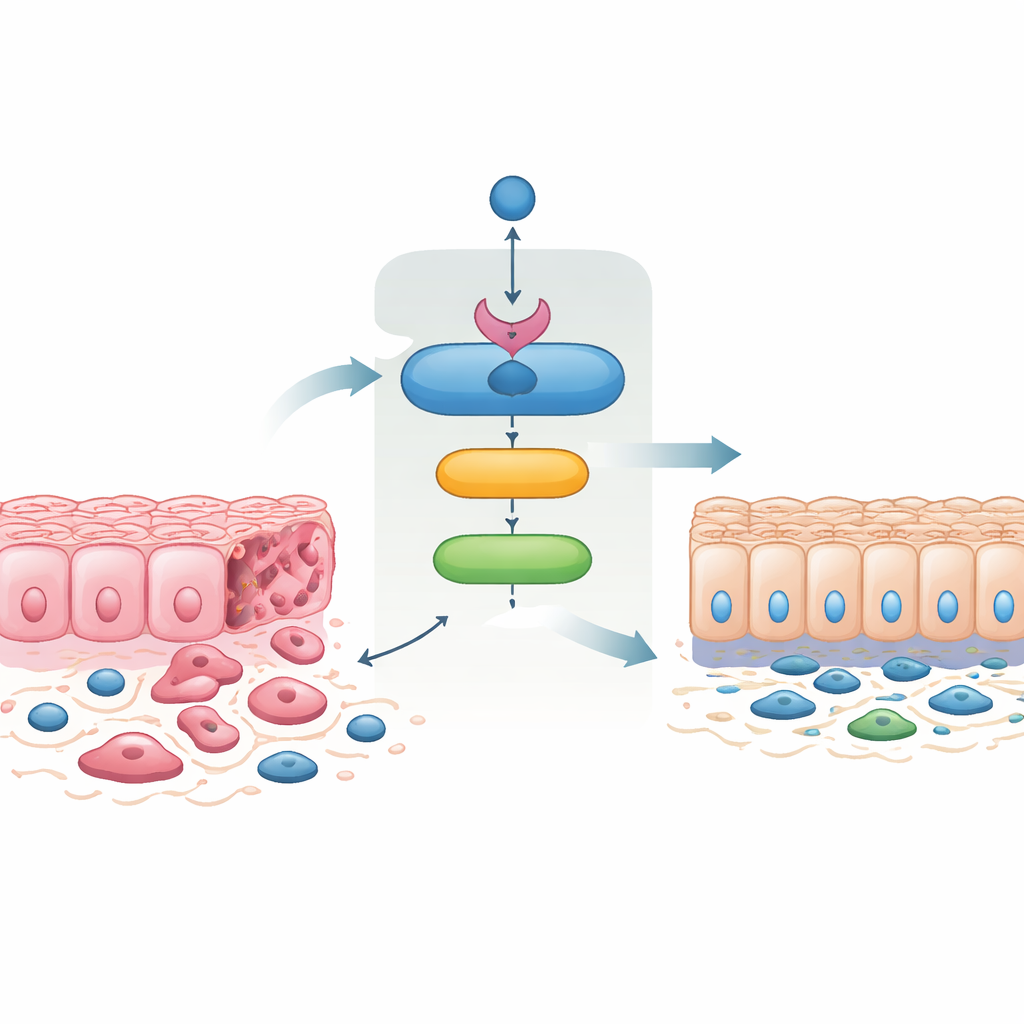
سلسلة من الحماة داخل الخلايا السرطانية
اكتشف الفريق أن SMAD4 ينشط مباشرة جينًا يُدعى 14‑3‑3σ، المعروف منذ زمن طويل بأنه مكبح للورم. باستخدام خطوط خلايا بشرية لسرطان القولون والمستقيم، والأورام المصغرة المستمدة من مرضى مزروعة في المختبر، ونماذج الفئران، أظهروا أن إعادة تشغيل SMAD4 ترفع مستويات 14‑3‑3σ بشكل موثوق، بينما يمنع فقدان SMAD4 هذا الارتفاع. حددوا مواقع ارتكاز لـ SMAD4 في منطقة التحكم بجين 14‑3‑3σ وأكدوا أن SMAD4 يحتل هذه المواقع فعليًا، مُثبتين بذلك أن 14‑3‑3σ هو هدف مباشر في خلايا الأمعاء البشرية والفأرية على حد سواء. في الأمعاء الطبيعية للفئران، يكون 14‑3‑3σ وفيرًا بشكل خاص عند قمم الزغابات، لكن هذا النمط يختفي عندما يُحذف Smad4، مما يبرز الروابط الوثيقة بين الاثنين خلال تمايز الأنسجة.
إعادة خلايا السرطان إلى حالة منظمة
غالبًا ما تخضع خلايا السرطان لـ "الانتقال الطلائي-الميزنكيمي"، فتتحول من خلايا متصلة بإحكام ومسطحة إلى خلايا أكثر حركة وذات شكل مغزلي تسهل غزوها وزرعها كرؤوس للنقائل. العملية العكسية، الانتقال الميزنكيمي-الطلائي، تستعيد الاتصالات الخلوية المحكمة وتقلل الغزو. عندما أعاد الباحثون إدخال SMAD4 إلى خلايا سرطان القولون والمستقيم العدوانية التي تفتقده عادةً، تحولت الخلايا إلى مظهر طلائي، وعادت بروتينات الالتصاق المرتبطة بالغشاء، وفقدت سمات مرتبطة بالحركة والغزو. هذه الخلايا المستعادة لـ SMAD4 هاجرت أقل، وغزت أقل عبر أغشية اصطناعية، وشكلت مستعمرات أقل. بشكل ملحوظ، أدى إجبار الخلايا على إنتاج 14‑3‑3σ وحده إلى تغييرات شبيهة جدًا، وإسكات 14‑3‑3σ ألغى إلى حد كبير تأثيرات SMAD4. هذا يوضح أن 14‑3‑3σ ليس مجرد متفرج بل وسيط رئيسي لقدرة SMAD4 على كبح السلوك الغازي.
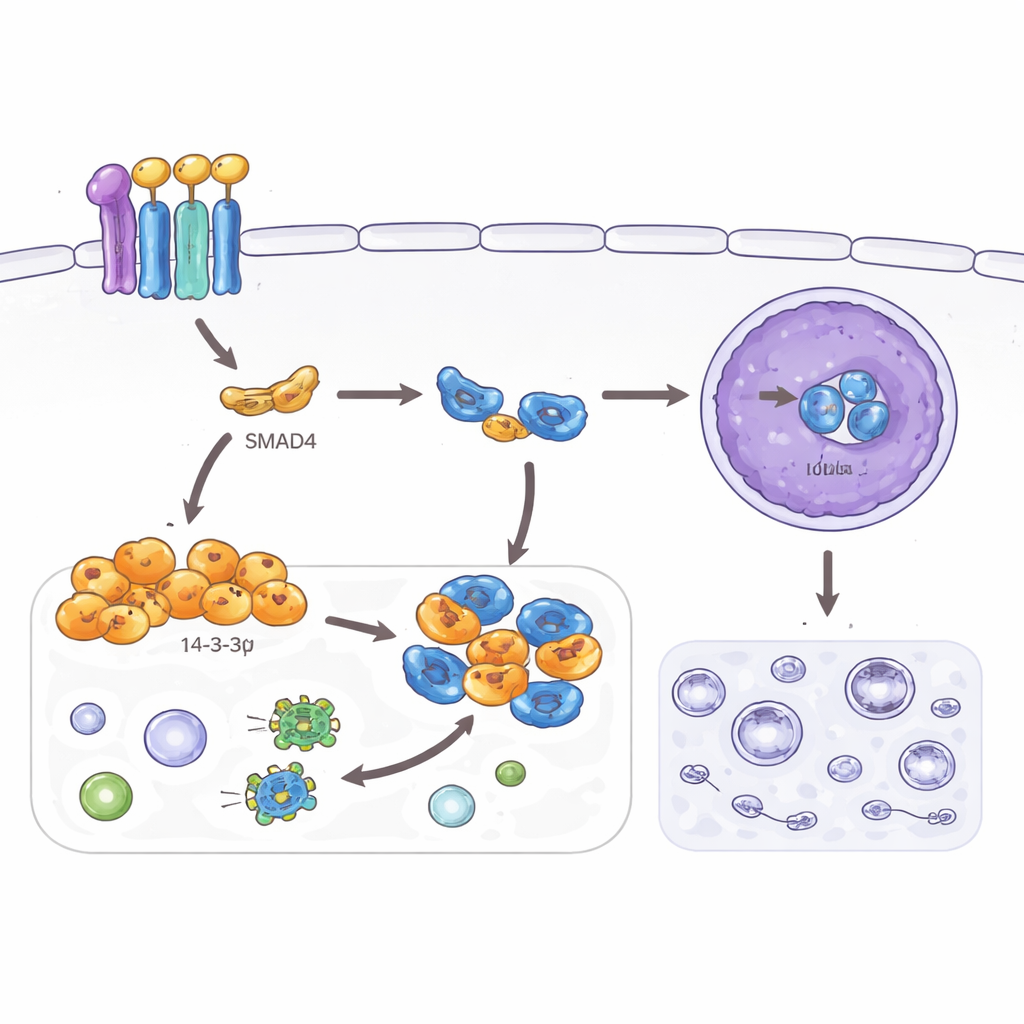
إيقاف مسار بقاء
فحصت الدراسة أيضًا الالتهام الذاتي، وهو برنامج إعادة تدوير يساعد الخلايا على النجاة من الإجهاد عبر تفكيك مكونات داخلية. رغم فائدته في الأنسجة الطبيعية، يمكن أن يساعد الالتهام الذاتي المعزز خلايا السرطان على التعامل مع بيئات معادية والعلاج. وجد المؤلفون أن SMAD4 و14‑3‑3σ يقللان كلاهما من مؤشرات الالتهام الذاتي في خلايا سرطان القولون والمستقيم ويقللان عدد الحويصلات المعاد تدويرها المرصودة تحت المجهر. تتبعوا هذا التأثير إلى بروتين آخر، TFEB، المتحكم الرئيسي في الالتهام الذاتي والليزوزومات. عادةً عندما يدخل TFEB النواة، يُفعّل العديد من الجينات المرتبطة بالالتهام الذاتي. هنا، يربط 14‑3‑3σ المدفوع بواسطة SMAD4 TFEB في الحيز الخلوي الخارجي ويمنعه من الوصول إلى النواة، لكن ذلك يحدث فقط عندما يتم وسم موقع محدد على TFEB كيميائيًا. عندما يتحور هذا الموقع، لا يعود بإمكان 14‑3‑3σ حجز TFEB، يستأنف الالتهام الذاتي، وتضعف التأثيرات الكابحة على الغزو وشكل الخلية.
ماذا يعني هذا للمرضى
تشير النتائج مجتمعة إلى محور وقائي خطي في الأمعاء: تنشط TGF‑β SMAD4، ويشغّل SMAD4 14‑3‑3σ، ويحبس 14‑3‑3σ TFEB خارج النواة. هذا التركيب يدفع خلايا سرطان القولون والمستقيم إلى حالة أكثر انتظامًا وأقل حركة ويخفّض من آلية التنظيف الذاتي لديها، مما قد يجعلها أقل قدرة على الانتشار وأكثر عرضة للعلاج. عندما يُفقد SMAD4 أو 14‑3‑3σ، يصبح TFEB أكثر نشاطًا، مما قد يعزز كلًا من الليونة الخلوية ومقاومة الإجهاد. رغم أن هناك حاجة لمزيد من العمل في حيوانات حية وعينات سريرية، يبرِز المسار المكشوف هنا نقاطًا جزيئية جديدة قد تستهدفها أدوية مستقبلية لتعزيز دفاعات الجسم ضد سرطان القولون والمستقيم النقيلي.
الاستشهاد: Chen, X., Winter, M., Rokavec, M. et al. TGF-β/SMAD4/14-3-3σ/TFEB axis promotes mesenchymal-epithelial transition and inhibits autophagy in colorectal cancer. Cell Death Dis 17, 397 (2026). https://doi.org/10.1038/s41419-026-08733-x
الكلمات المفتاحية: سرطان القولون والمستقيم, الانبثاث, الالتهام الذاتي, الليونة الطلائية, TFEB