Clear Sky Science · tr
TGF-β/SMAD4/14-3-3σ/TFEB ekseni kolorektal kanserde mezenkimal‑epitelyal geçişi destekler ve otofajiyi baskılar
Bu çalışma kolon kanseri için neden önemli
Kolorektal kanser, tümör hücrelerinin sıklıkla bağırsaktan uzak organlara yayılması nedeniyle kanser ölümlerinin önde gelen nedenlerinden biridir. Bu çalışma, bu yayılmayı sınırlayabilen bağırsak hücreleri içinde daha önce tanınmamış bir koruyucu devreyi ortaya koyuyor. Araştırmacılar, birkaç molekülün birbirleriyle nasıl iletişim kurduğunu haritalandırarak, bağırsaktaki normal sinyallerin kanser hücrelerini daha düzenli bir duruma geri itebileceğini ve onların hayatta kalma hilelerinden biri olan kendi kendini temizleme süreci otofajiyi kesebileceğini gösteriyor.
Bağırsakta koruyucu bir mesaj
Bağırsaklarımız sürekli yiyecek, bakteri ve mekanik strese maruz kalır; bu nedenle bağırsaktaki hücreler büyüme ve onarım dengesini korumak için güçlü kontrol sistemlerine güvenir. TGF‑β adı verilen önemli bir sinyal genellikle erken tümör gelişimine frene basar. Bu sinyal, hücre çekirdeğine girip genleri açıp kapatan SMAD4 adlı bir protein aracılığıyla işler. Kolorektal kanserlerde SMAD4 sıkça kaybolur ve tümörleri bu proteini içermeyen hastalar genellikle daha fazla metastaz yapar ve daha kötü sağkalım gösterir. Yazarlar, SMAD4’ün invazyonu ve yayılmayı engelleme yeteneğini açıklayabilecek hangi spesifik genleri kontrol ettiğini anlamayı amaçladılar.
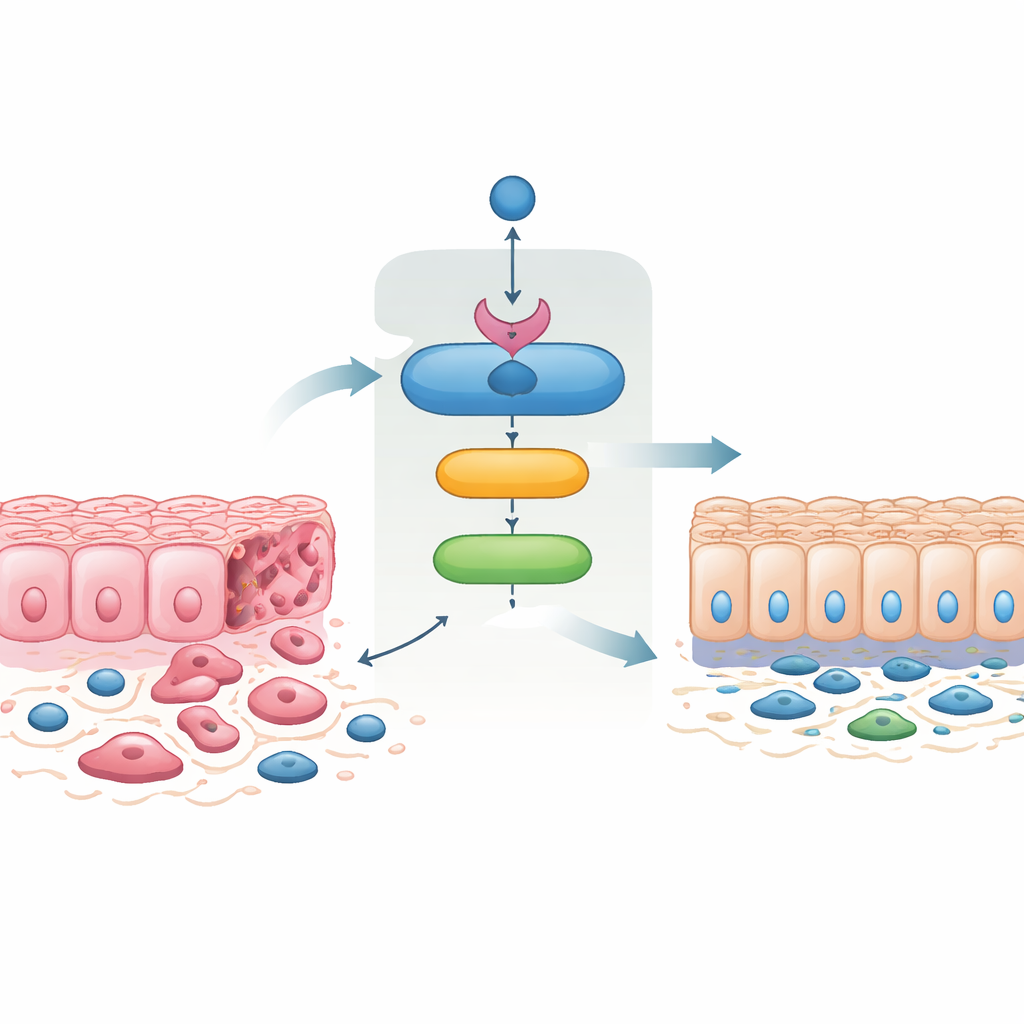
Kanser hücreleri içinde bir dizi koruyucu
Ekip, SMAD4’ün uzun süredir tümör baskılayıcı olarak bilinen 14‑3‑3σ adlı bir geni doğrudan aktive ettiğini keşfetti. İnsan kolorektal kanser hücre hatları, laboratuvarda yetiştirilen hasta kaynaklı mini‑tümörler ve fare modelleri kullanarak, SMAD4’ü açmanın 14‑3‑3σ seviyelerini güvenilir şekilde artırdığını, SMAD4’ü ortadan kaldırmanın ise bu artışı engellediğini gösterdiler. SMAD4 için 14‑3‑3σ kontrol bölgesinde tutunma yerlerini belirlediler ve SMAD4’ün bu bölgeleri fiziksel olarak işgal ettiğini doğrulayarak 14‑3‑3σ’ü hem insan hem fare bağırsak hücrelerinde doğrudan bir hedef olarak kesinleştirdiler. Normal fare bağırsağında 14‑3‑3σ özellikle villa uçlarında bol bulunur, ancak Smad4 silindiğinde bu desen kaybolur; bu da ikisi arasındaki bağın doku farklılaşması sırasında ne kadar yakın olduğunu vurguluyor.
Kanser hücrelerini yeniden düzene itmek
Kanser hücreleri sıklıkla sıkı bağlı, tabaka şeklindeki hücrelerden daha hareketli, iğsi şekilli hücrelere dönüşen bir "epitelyal‑mezenkimal geçiş" geçirir; bu değişim invazyonu ve metastaz oluşturmayı kolaylaştırır. Ters süreç olan mezenkimal‑epitelyal geçiş ise sıkı hücre–hücre bağlantılarını geri kazandırır ve invazivliği azaltır. Araştırmacılar, normalde SMAD4 içermeyen agresif kolorektal kanser hücrelerine SMAD4’ü yeniden tanıttıklarında, hücrelerin epitelyal bir görünüme kaydığını, membrana bağlı hücre adezyon proteinlerini yeniden kazandığını ve hareketlilik ile invazyonla ilişkili özellikleri kaybettiklerini gözlemlediler. Bu SMAD4‑yeniden kazanmış hücreler daha az göç etti, yapay membranlardan daha az invaze oldu ve daha az koloni oluşturdu. İlginç şekilde, hücrelere yalnızca 14‑3‑3σ üretmelerini zorlamak da çok benzer değişiklikler yarattı ve 14‑3‑3σ’yü engellemek SMAD4’ün etkilerini büyük ölçüde ortadan kaldırdı. Bu durum 14‑3‑3σ’ün sadece bir seyirci değil, SMAD4’ün invazif davranışı yatıştırma yeteneğinin kilit bir aracısı olduğunu gösteriyor.
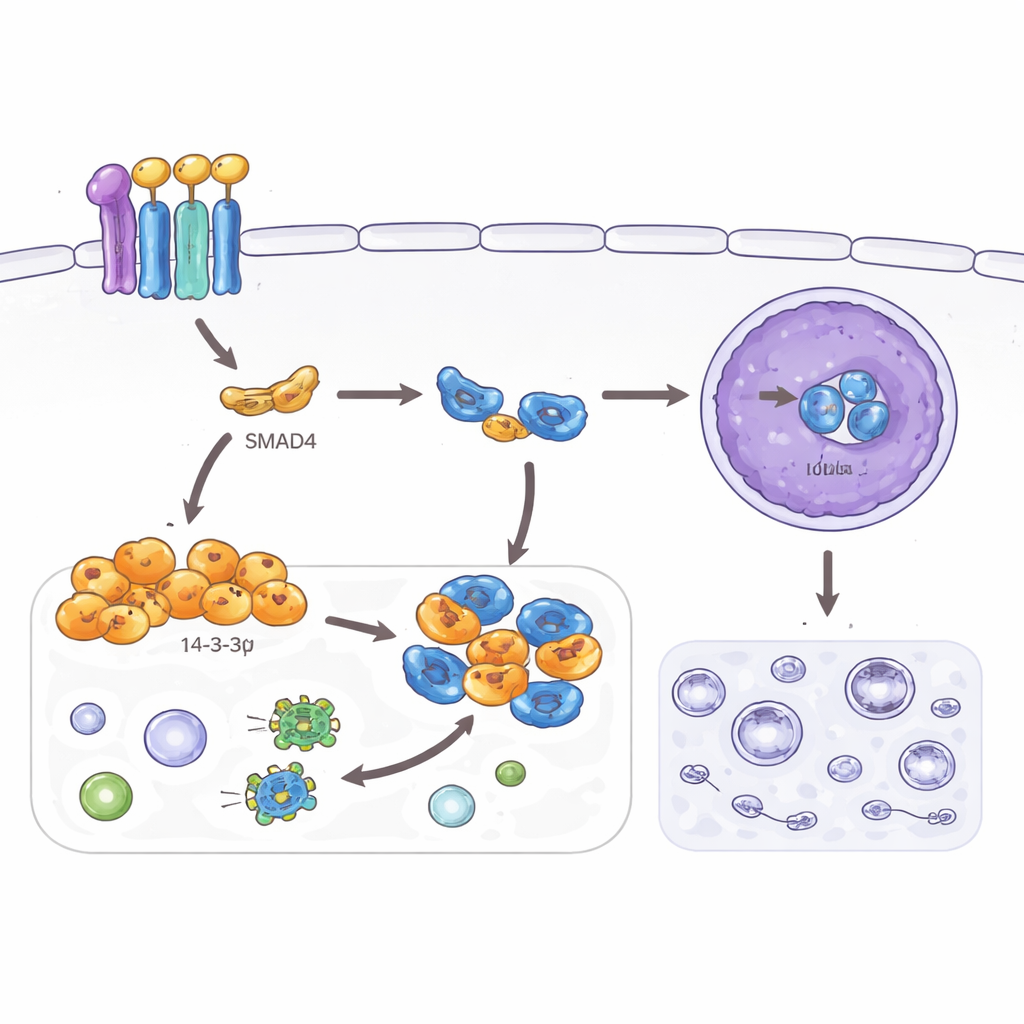
Bir hayatta kalma yolunu kapatmak
Çalışma ayrıca hücrelerin stresle başa çıkmasına yardımcı olan bir geri dönüşüm programı olan otofajiyi inceledi. Normal dokularda faydalı olmasına karşın, artmış otofaji kanser hücrelerinin zorlu ortamlar ve tedavilere karşı dayanmasını kolaylaştırabilir. Yazarlar, SMAD4 ve 14‑3‑3σ’ün kolorektal kanser hücrelerinde otofaji belirteçlerini düşürdüğünü ve mikroskop altında gözlemlenen geri dönüşüm veziküllerinin sayısını azalttığını buldular. Bu etkiyi otofaji ve lizozomların baş kontrolörü olan TFEB adlı başka bir proteine bağladılar. Normalde TFEB çekirdeğe girdiğinde birçok otofaji ilişkili geni aktive eder. Burada SMAD4 kaynaklı 14‑3‑3σ, TFEB’i hücrenin dış bölümünde bağlayıp çekirdeğe ulaşmasını engelliyor; ancak bunun olabilmesi için TFEB üzerindeki belirli bir bölgenin kimyasal olarak işaretlenmiş olması gerekiyor. Bu bölge mutasyona uğradığında 14‑3‑3σ TFEB’i artık tutamıyor, otofaji yeniden başlıyor ve invazyon ile hücre şekli üzerindeki baskılayıcı etkiler zayıflıyor.
Bu hastalar için ne anlama geliyor
Birlikte ele alındığında bulgular, bağırsakta doğrusal bir koruyucu ekseni ortaya koyuyor: TGF‑β SMAD4’ü aktifleştirir, SMAD4 14‑3‑3σ’ü açar ve 14‑3‑3σ TFEB’i çekirdek dışında hapseder. Bu kombinasyon kolorektal kanser hücrelerini daha düzenli, daha az hareketli bir duruma iter ve onların otofaji mekanizmasını azaltır; bu da hücrelerin yayılma yeteneğini düşürebilir ve tedaviye duyarlılıklarını artırabilir. SMAD4 veya 14‑3‑3σ kaybolduğunda TFEB daha aktif hale gelir ve potansiyel olarak hem hücresel plastisiteyi hem de stres direncini artırır. Canlı hayvanlar ve klinik örneklerde daha fazla çalışma gerekliliğine rağmen, burada ortaya konan yolak metastatik kolorektal kanserle mücadelede gelecekteki ilaçların vücudun kendi savunmalarını güçlendirebileceği yeni moleküler hedefleri vurguluyor.
Atıf: Chen, X., Winter, M., Rokavec, M. et al. TGF-β/SMAD4/14-3-3σ/TFEB axis promotes mesenchymal-epithelial transition and inhibits autophagy in colorectal cancer. Cell Death Dis 17, 397 (2026). https://doi.org/10.1038/s41419-026-08733-x
Anahtar kelimeler: kolorektal kanser, metastaz, otofaji, epitelyal plastisite, TFEB