Clear Sky Science · it
L'asse TGF-β/SMAD4/14-3-3σ/TFEB promuove la transizione mesenchimale‑epiteliale e inibisce l'autofagia nel cancro colorettale
Perché questo studio è importante per il cancro del colon
Il cancro colorettale è una delle principali cause di morte per tumore perché le cellule tumorali spesso si diffondono dall'intestino ad organi distanti. Questo studio scopre un circuito di protezione prima non riconosciuto all'interno delle cellule intestinali che può limitare questa diffusione. Mappando come diverse molecole comunicano tra loro, i ricercatori mostrano come segnali normali nell'intestino possano spingere le cellule tumorali verso uno stato più ordinato e interrompere uno dei loro stratagemmi di sopravvivenza, un processo di auto‑pulizia chiamato autofagia.
Un messaggio protettivo nell'intestino
I nostri intestini sono costantemente esposti a cibo, batteri e stress meccanico, perciò le cellule intestinali fanno affidamento su sistemi di controllo robusti per mantenere l'equilibrio tra crescita e riparazione. Un segnale principale, chiamato TGF‑β, agisce normalmente come freno allo sviluppo tumorale precoce. Opera tramite una proteina denominata SMAD4, che si sposta nel nucleo cellulare e attiva o spegne geni. Nei tumori colorettali, SMAD4 viene frequentemente perso, e i pazienti i cui tumori mancano di questa proteina tendono ad avere più metastasi e una sopravvivenza peggiore. Gli autori hanno cercato di capire quali geni specifici SMAD4 controlli che possano spiegare la sua capacità di bloccare l'invasione e la diffusione.
Una catena di guardian all'interno delle cellule tumorali
Il gruppo ha scoperto che SMAD4 attiva direttamente un gene chiamato 14‑3‑3σ, noto da tempo come soppressore tumorale. Usando linee cellulari umane di cancro colorettale, mini‑tumori derivati da pazienti coltivati in laboratorio e modelli murini, hanno mostrato che l'attivazione di SMAD4 aumenta in modo affidabile i livelli di 14‑3‑3σ, mentre la rimozione di SMAD4 impedisce questo incremento. Hanno identificato siti di legame per SMAD4 nella regione di controllo di 14‑3‑3σ e confermato che SMAD4 occupa fisicamente questi siti, stabilendo in modo netto 14‑3‑3σ come bersaglio diretto sia nelle cellule intestinali umane sia in quelle murine. Nell'intestino murino normale, 14‑3‑3σ è particolarmente abbondante alle punte dei villi, ma questo schema scompare quando Smad4 viene eliminato, sottolineando quanto strettamente i due siano collegati durante la differenziazione tissutale.
Spingere le cellule tumorali verso l'ordine
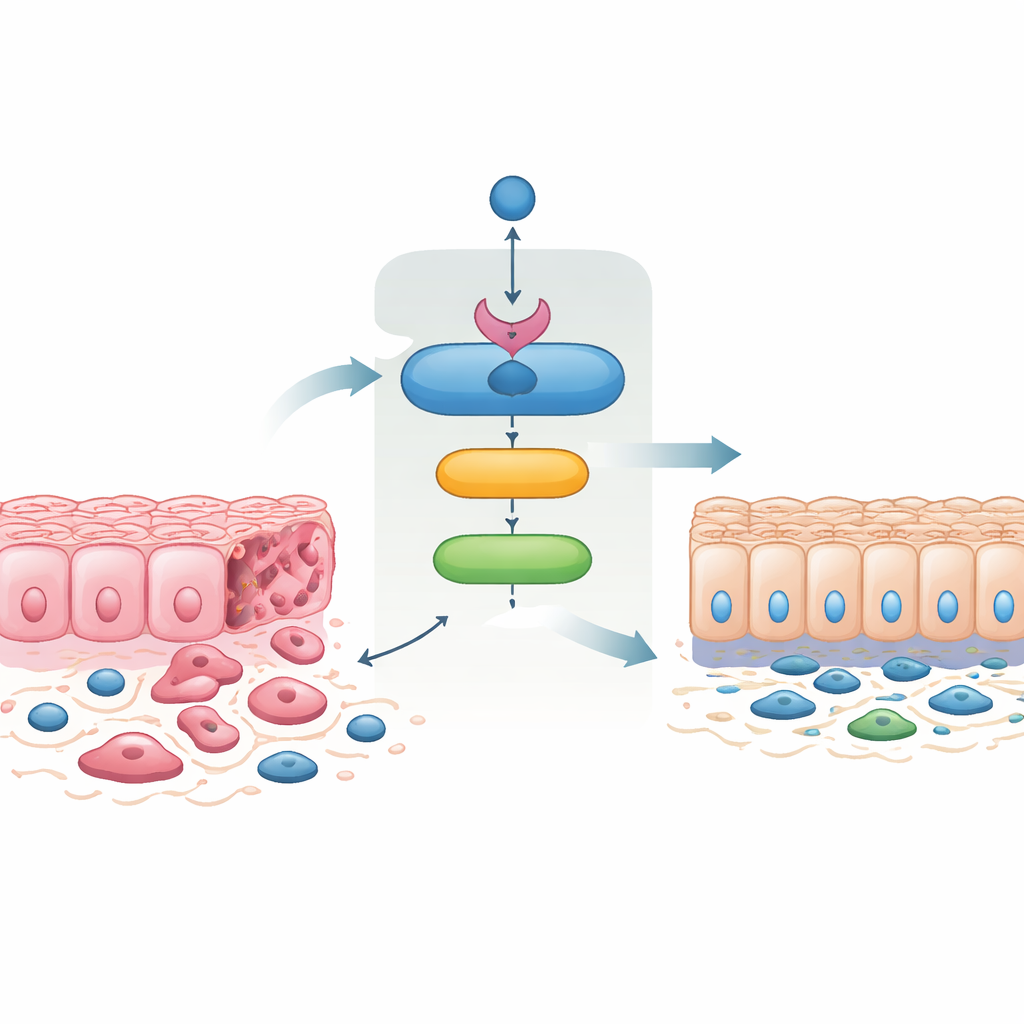
Le cellule tumorali spesso subiscono una «transizione epitelio‑mesenchimale», passando da cellule compatte e connesse in fogli a cellule più mobili, a forma di fuso, che invadono più facilmente e generano metastasi. Il processo inverso, transizione mesenchimale‑epiteliale, ripristina contatti stretti fra le cellule e riduce l'invasività. Quando i ricercatori reintrodussero SMAD4 in cellule di cancro colorettale aggressive che normalmente ne sono prive, le cellule assunsero un aspetto più epiteliale, riacquistarono proteine di adesione associate alla membrana e persero caratteristiche legate alla mobilità e all'invasione. Queste cellule con SMAD4 ristabilito migrarono di meno, invasero meno attraverso membrane artificiali e formarono meno colonie. Sorprendentemente, forzare la produzione di 14‑3‑3σ da sola generò cambiamenti molto simili, e bloccare 14‑3‑3σ annullò in gran parte gli effetti di SMAD4. Ciò dimostra che 14‑3‑3σ non è un semplice spettatore ma un mediatore chiave della capacità di SMAD4 di addomesticare il comportamento invasivo.
Spegnere una via di sopravvivenza
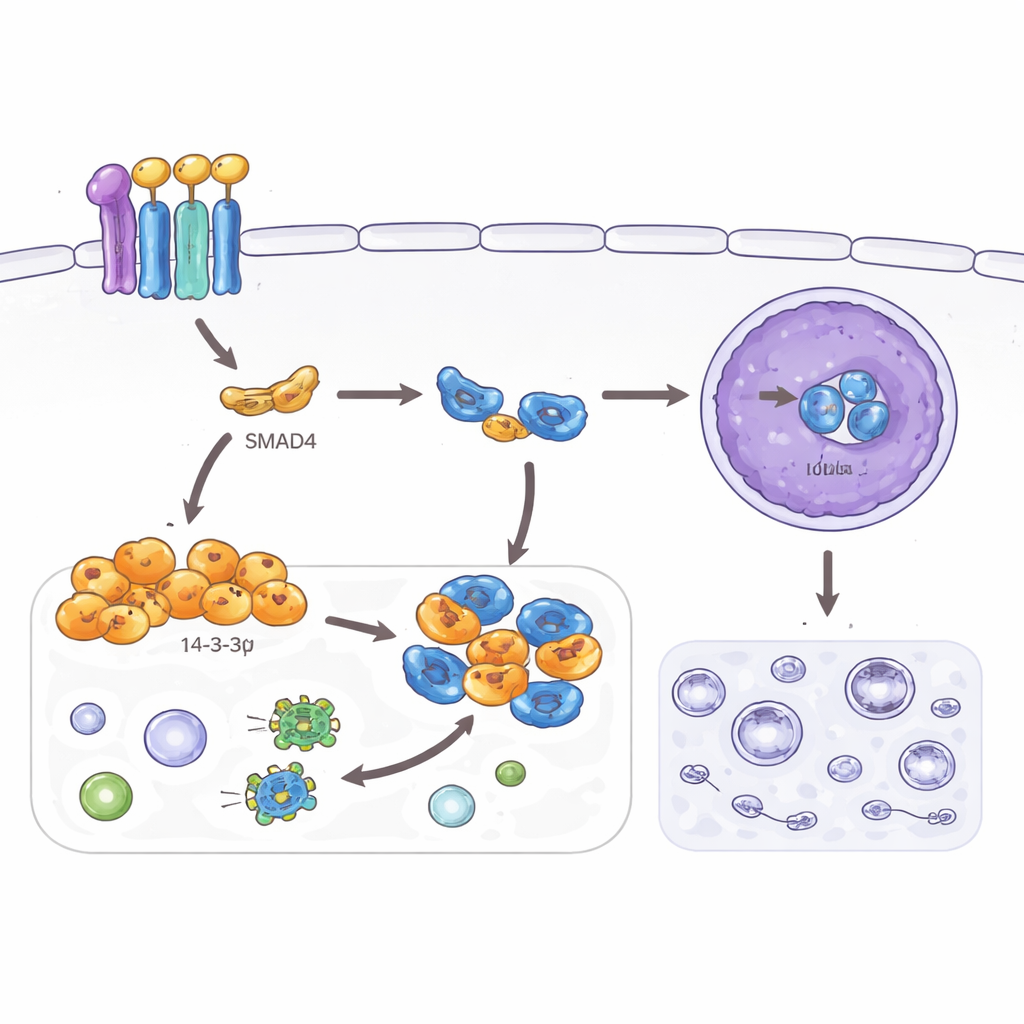
Lo studio ha anche esaminato l'autofagia, un programma di riciclaggio che aiuta le cellule a sopravvivere allo stress degradando componenti interni. Pur essendo utile nei tessuti normali, un'aumentata autofagia può aiutare le cellule tumorali a fronteggiare ambienti ostili e terapie. Gli autori hanno riscontrato che SMAD4 e 14‑3‑3σ abbassano entrambi i marcatori dell'autofagia nelle cellule di cancro colorettale e riducono il numero di vescicole di riciclaggio osservate al microscopio. Hanno ricondotto questo effetto a un'altra proteina, TFEB, un regolatore master dell'autofagia e dei lisosomi. Normalmente, quando TFEB entra nel nucleo attiva molti geni legati all'autofagia. Qui, 14‑3‑3σ indotto da SMAD4 lega TFEB nel compartimento citoplasmatico e ne impedisce l'accesso al nucleo, ma solo quando un sito specifico su TFEB è stato marcato chimicamente. Quando questo sito è mutato, 14‑3‑3σ non può più trattenere TFEB, l'autofagia riprende e gli effetti inibitori su invasività e morfologia cellulare vengono attenuati.
Cosa significa per i pazienti
Complessivamente, i risultati delineano un asse protettivo lineare nell'intestino: TGF‑β attiva SMAD4, SMAD4 accende 14‑3‑3σ e 14‑3‑3σ intrappola TFEB fuori dal nucleo. Questa combinazione spinge le cellule del cancro colorettale verso uno stato più ordinato e meno mobile e smorza la loro macchina di auto‑pulizia, il che potrebbe renderle meno capaci di diffondersi e più vulnerabili ai trattamenti. Quando SMAD4 o 14‑3‑3σ vengono persi, TFEB diventa più attivo, potenzialmente aumentando sia la plasticità cellulare sia la resistenza allo stress. Sebbene siano necessari ulteriori studi in animali vivi e su campioni clinici, la via qui rivelata mette in luce nuovi punti molecolari dove future terapie potrebbero rafforzare le difese endogene contro il cancro colorettale metastatico.
Citazione: Chen, X., Winter, M., Rokavec, M. et al. TGF-β/SMAD4/14-3-3σ/TFEB axis promotes mesenchymal-epithelial transition and inhibits autophagy in colorectal cancer. Cell Death Dis 17, 397 (2026). https://doi.org/10.1038/s41419-026-08733-x
Parole chiave: cancro colorettale, metastasi, autofagia, plasticità epiteliale, TFEB