Clear Sky Science · pt
Eixo TGF-β/SMAD4/14-3-3σ/TFEB promove a transição mesenquimal-epitelial e inibe a autofagia no câncer colorretal
Por que este estudo importa para o câncer de cólon
O câncer colorretal é uma das principais causas de morte por câncer porque as células tumorais frequentemente se espalham do intestino para órgãos distantes. Este estudo revela um circuito de segurança previamente não reconhecido dentro das células intestinais que pode conter esse espalhamento. Ao mapear como várias moléculas se comunicam, os pesquisadores mostram como sinais normais no intestino podem empurrar as células cancerosas de volta para um estado mais ordenado e cortar um dos seus truques de sobrevivência, um processo de auto‑limpeza chamado autofagia.
Uma mensagem protetora no intestino
Nosso intestino está constantemente exposto a alimentos, bactérias e estresse mecânico, portanto as células do intestino dependem de sistemas de controle fortes para manter o equilíbrio entre crescimento e reparo. Um grande sinal, chamado TGF‑β, normalmente atua como um freio no desenvolvimento inicial do tumor. Ele age por meio de uma proteína chamada SMAD4, que se desloca para o núcleo celular e liga ou desliga genes. Nos cânceres colorretais, o SMAD4 é frequentemente perdido, e pacientes cujos tumores carecem dessa proteína tendem a ter mais metástases e pior sobrevida. Os autores buscaram entender quais genes específicos o SMAD4 controla que poderiam explicar sua capacidade de bloquear invasão e disseminação.
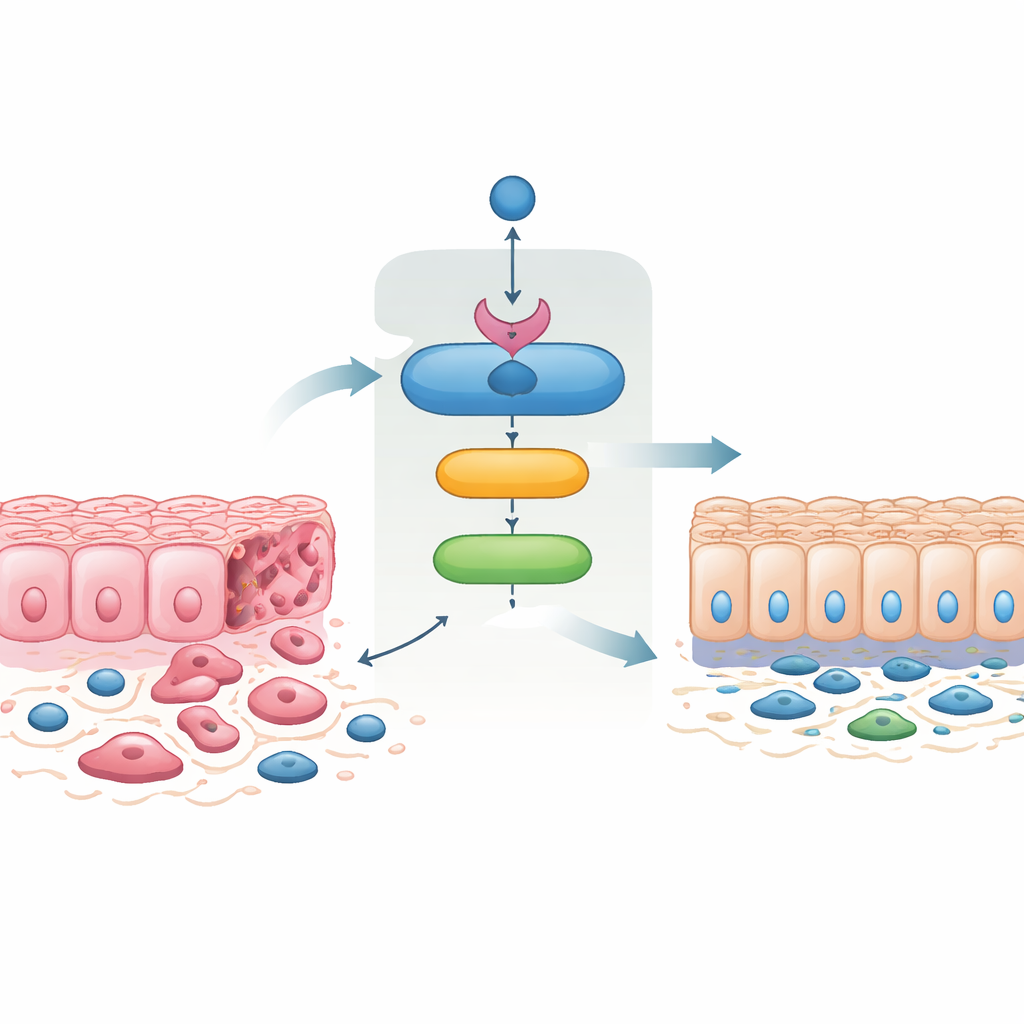
Uma cadeia de guardiões dentro das células tumorais
A equipe descobriu que o SMAD4 ativa diretamente um gene chamado 14‑3‑3σ, conhecido há muito tempo como supressor tumoral. Usando linhagens humanas de câncer colorretal, mini‑tumores derivados de pacientes cultivados em laboratório e modelos murinos, eles mostraram que ativar o SMAD4 aumenta de forma confiável os níveis de 14‑3‑3σ, enquanto remover o SMAD4 impede esse aumento. Eles localizaram sítios de ancoragem para o SMAD4 na região reguladora do 14‑3‑3σ e confirmaram que o SMAD4 ocupa fisicamente esses sítios, estabelecendo firmemente o 14‑3‑3σ como um alvo direto tanto em células intestinais humanas quanto de camundongos. No intestino normal de camundongo, o 14‑3‑3σ é especialmente abundante nas pontas das vilosidades, mas esse padrão desaparece quando Smad4 é deletado, ressaltando o quão estreitamente os dois estão ligados durante a diferenciação tecidual.
Reposicionando as células cancerosas rumo à ordem
As células cancerosas frequentemente passam por uma "transição epitelial‑mesenquimal", mudando de células fortemente conectadas, em folhas, para formas mais móveis e fusiformes que invadem e formam metástases com mais facilidade. O processo inverso, transição mesenquimal‑epitelial, restaura contatos celulares apertados e reduz a invasividade. Quando os pesquisadores reintroduziram o SMAD4 em células agressivas de câncer colorretal que normalmente o têm ausente, as células mudaram para uma aparência mais epitelial, recuperaram proteínas de adesão na membrana e perderam características associadas à mobilidade e invasão. Essas células com SMAD4 restaurado migraram menos, invadiram menos através de membranas artificiais e formaram menos colônias. Notavelmente, forçar a expressão apenas do 14‑3‑3σ produziu mudanças muito semelhantes, e bloquear o 14‑3‑3σ eliminou em grande parte os efeitos do SMAD4. Isso mostra que o 14‑3‑3σ não é apenas um espectador, mas um mediador chave da capacidade do SMAD4 de domesticar o comportamento invasivo.
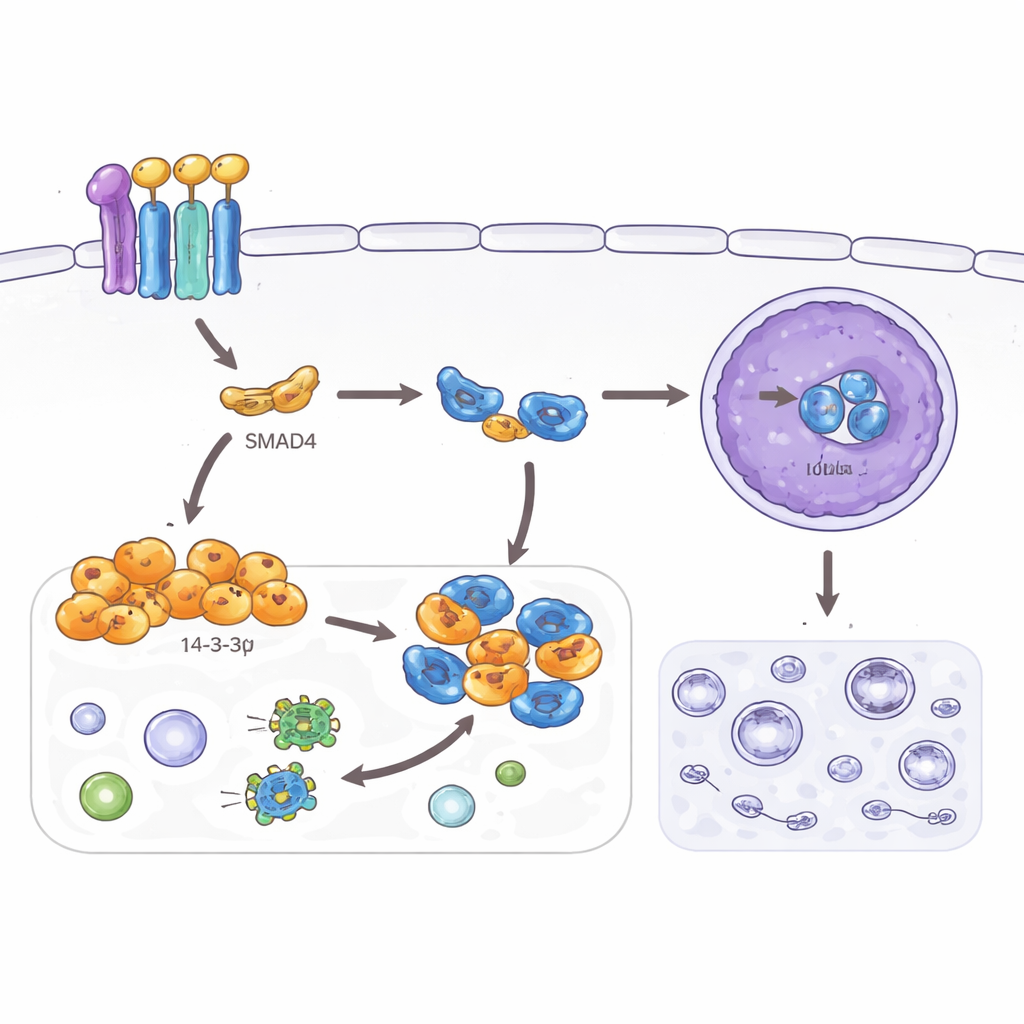
Desligando uma via de sobrevivência
O estudo também examinou a autofagia, um programa de reciclagem que ajuda as células a sobreviver ao estresse ao degradar componentes internos. Embora útil em tecidos normais, a autofagia aumentada pode ajudar células tumorais a lidar com ambientes hostis e tratamentos. Os autores descobriram que SMAD4 e 14‑3‑3σ reduzem marcadores de autofagia em células de câncer colorretal e diminuem o número de vesículas de reciclagem observadas ao microscópio. Eles atribuíram esse efeito a outra proteína, TFEB, um controlador mestre da autofagia e dos lisossomos. Normalmente, quando o TFEB entra no núcleo, ele ativa muitos genes relacionados à autofagia. Aqui, o 14‑3‑3σ induzido por SMAD4 se liga ao TFEB no compartimento citoplasmático e impede sua entrada no núcleo, mas somente quando um sítio específico no TFEB foi quimicamente modificado. Quando esse sítio é mutado, o 14‑3‑3σ não consegue mais reter o TFEB, a autofagia é retomada e os efeitos supressores sobre invasão e morfologia celular são enfraquecidos.
O que isso significa para os pacientes
Em conjunto, os achados delineiam um eixo protetor linear no intestino: TGF‑β ativa o SMAD4, o SMAD4 liga o 14‑3‑3σ, e o 14‑3‑3σ aprisiona o TFEB fora do núcleo. Essa combinação impulsiona as células de câncer colorretal para um estado mais ordenado e menos móvel e atenua sua maquinaria de auto‑limpeza, o que pode torná‑las menos capazes de se espalhar e mais vulneráveis ao tratamento. Quando o SMAD4 ou o 14‑3‑3σ são perdidos, o TFEB se torna mais ativo, potencialmente aumentando tanto a plasticidade celular quanto a resistência ao estresse. Embora sejam necessários mais estudos em animais vivos e amostras clínicas, a via revelada aqui destaca novos pontos moleculares onde futuros fármacos poderiam reforçar as defesas naturais do organismo contra o câncer colorretal metastático.
Citação: Chen, X., Winter, M., Rokavec, M. et al. TGF-β/SMAD4/14-3-3σ/TFEB axis promotes mesenchymal-epithelial transition and inhibits autophagy in colorectal cancer. Cell Death Dis 17, 397 (2026). https://doi.org/10.1038/s41419-026-08733-x
Palavras-chave: câncer colorretal, metástase, autofagia, plasticidade epitelial, TFEB