Clear Sky Science · de
TGF-β/SMAD4/14-3-3σ/TFEB-Achse fördert die mesenchymal-epitheliale Transition und hemmt Autophagie beim kolorektalen Karzinom
Warum diese Studie für Darmkrebs wichtig ist
Kolorektales Karzinom gehört zu den führenden krebsbedingten Todesursachen, weil Tumorzellen häufig aus dem Darm in entfernte Organe streuen. Diese Studie deckt einen bislang unbekannten Schutzmechanismus in Darmzellen auf, der diese Streuung einschränken kann. Indem die Forschenden nachzeichnen, wie mehrere Moleküle miteinander kommunizieren, zeigen sie, wie normale Signale im Darm Krebszellen zurück in einen geordneteren Zustand drängen und einen ihrer Überlebensmechanismen — einen Selbstreinigungsprozess namens Autophagie — unterbinden können.
Eine schützende Botschaft im Darm
Unsere Därme sind ständig Nahrungsbestandteilen, Bakterien und mechanischem Stress ausgesetzt, daher verlassen sich die Darmzellen auf robuste Kontrollsysteme, um Wachstum und Reparatur im Gleichgewicht zu halten. Ein wichtiges Signal, TGF‑β genannt, wirkt meist als Bremse in frühen Tumorstadien. Es funktioniert über ein Protein namens SMAD4, das in den Zellkern wandert und Gene an- oder abschaltet. Bei kolorektalen Karzinomen geht SMAD4 häufig verloren, und Patientinnen und Patienten mit Tumoren ohne dieses Protein haben tendenziell mehr Metastasen und eine schlechtere Überlebensrate. Die Autoren wollten herausfinden, welche spezifischen Gene SMAD4 steuert, die seine Fähigkeit erklären könnten, Invasion und Ausbreitung zu verhindern.
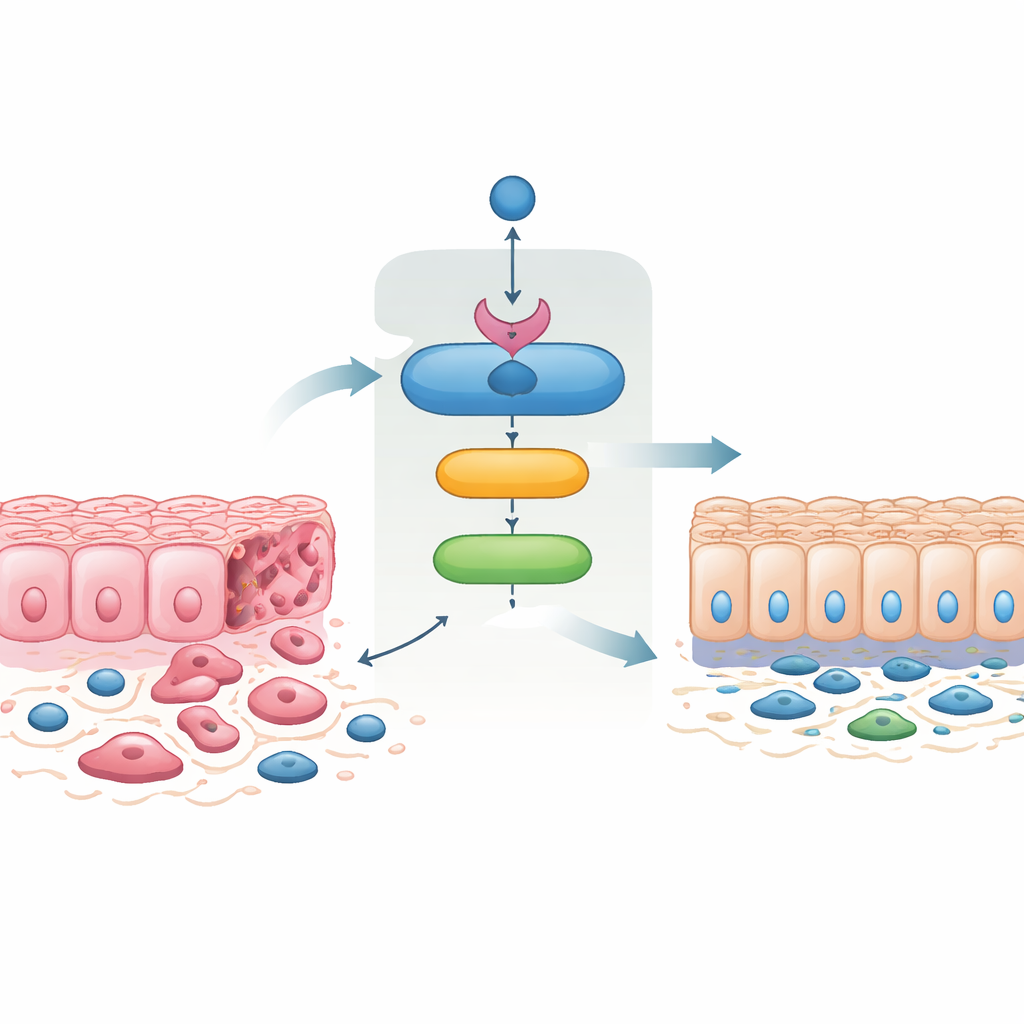
Eine Kette von Wächterproteinen in Krebszellen
Das Team entdeckte, dass SMAD4 das Gen 14‑3‑3σ direkt aktiviert, das lange als Tumorsuppressor bekannt ist. Anhand menschlicher kolorektaler Zelllinien, patientenabgeleiteter Mini‑Tumoren im Labor und Mausmodellen zeigten sie, dass die Aktivierung von SMAD4 zuverlässig 14‑3‑3σ‑Pegel erhöht, während das Entfernen von SMAD4 diese Zunahme verhindert. Sie identifizierten Bindungsstellen für SMAD4 in der Regulationsregion von 14‑3‑3σ und bestätigten, dass SMAD4 diese Stellen physisch besetzt — damit ist 14‑3‑3σ eindeutig ein direktes Zielgen in menschlichen und murinen Darmzellen. Im normalen Mausdarm kommt 14‑3‑3σ besonders an den Zipfeln der Zotten vor, doch dieses Muster verschwindet bei Deletion von Smad4, was die enge Verbindung der beiden Proteine während der Gewebedifferenzierung unterstreicht.
Krebszellen zurück in die Ordnung drängen
Krebszellen durchlaufen häufig eine epithelial‑mesenchymale Transition, bei der sie von dicht verbundenen, schichtartigen Zellen in beweglichere, spindelförmige Zellen übergehen, die leichter in umliegendes Gewebe eindringen und Metastasen bilden. Der umgekehrte Prozess, die mesenchymal‑epitheliale Transition, stellt enge Zell‑Zell‑Verbindungen wieder her und verringert die Invasivität. Wenn die Forschenden SMAD4 in aggressive kolorektale Krebszellen, die es normalerweise nicht haben, zurückbrachten, wandelten sich die Zellen zu einem epithelialen Erscheinungsbild, gewannen membrangebundenen Zelladhäsionsproteine zurück und verloren Merkmale, die mit Mobilität und Invasion assoziiert sind. Diese SMAD4‑rekonstituierten Zellen wanderten weniger, drangen weniger durch künstliche Membranen ein und bildeten weniger Kolonien. Bemerkenswerterweise erzeugte alleiniges Erzwingen der 14‑3‑3σ‑Expression sehr ähnliche Veränderungen, und die Blockade von 14‑3‑3σ hob die Effekte von SMAD4 größtenteils auf. Das zeigt, dass 14‑3‑3σ kein unbeteiligter Begleiter ist, sondern ein zentraler Mediator von SMAD4s Fähigkeit, invasives Verhalten zu zähmen.
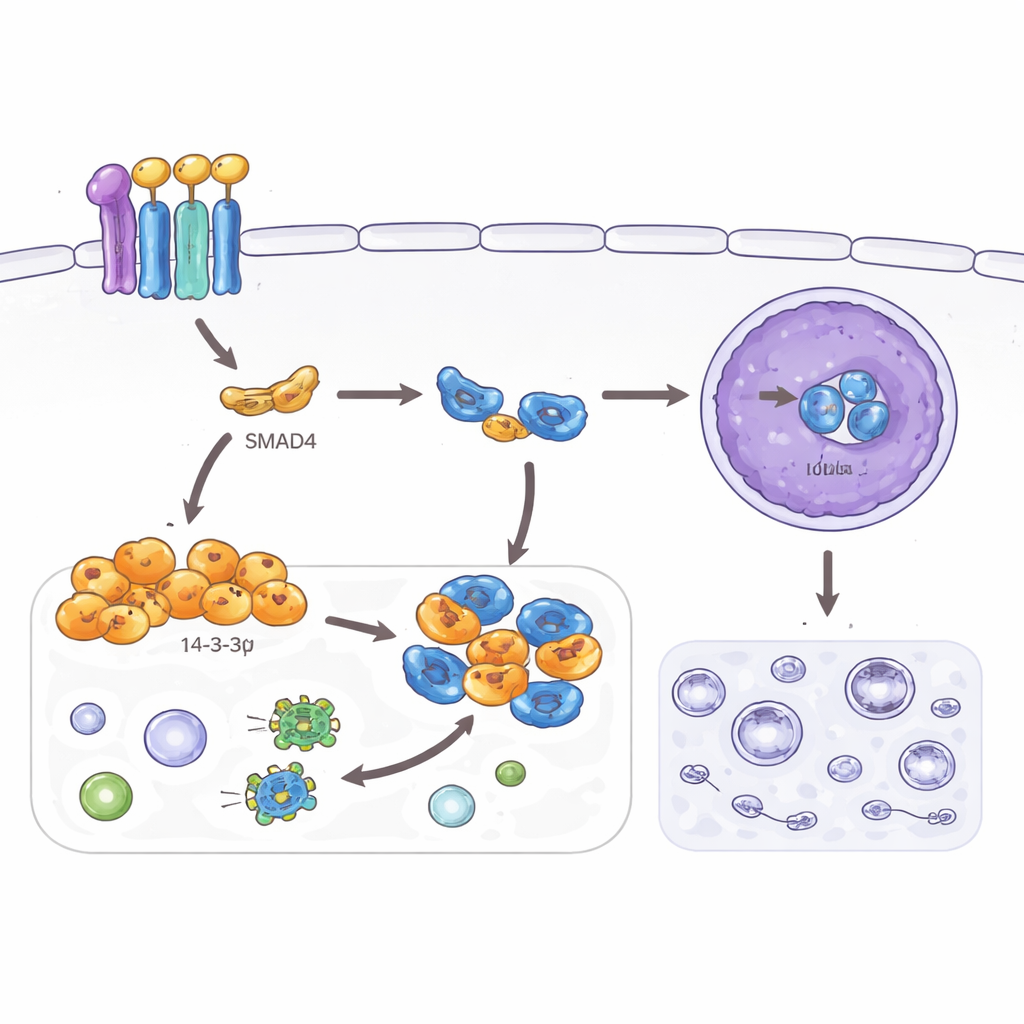
Abschalten eines Überlebenswegs
Die Studie untersuchte außerdem die Autophagie, ein Recyclingprogramm, das Zellen hilft, Stress zu überstehen, indem interne Bestandteile abgebaut werden. Während Autophagie in normalen Geweben nützlich ist, kann erhöhte Autophagie Krebszellen helfen, widrige Umgebungen und Therapien zu überstehen. Die Autoren fanden heraus, dass SMAD4 und 14‑3‑3σ in kolorektalen Krebszellen beide Autophagie‑Marker senken und die Anzahl der unter dem Mikroskop sichtbaren Recyclingvesikel reduzieren. Sie führten diesen Effekt auf ein weiteres Protein zurück: TFEB, einen Masterregulator von Autophagie und Lysosomen. Normalerweise aktiviert TFEB im Zellkern zahlreiche Autophagie‑Gene. Hier bindet das von SMAD4 induzierte 14‑3‑3σ TFEB im zytoplasmatischen Bereich und verhindert so dessen Eintritt in den Kern — allerdings nur wenn eine bestimmte Stelle auf TFEB chemisch markiert ist. Bei Mutation dieser Stelle kann 14‑3‑3σ TFEB nicht mehr zurückhalten, die Autophagie setzt wieder ein und die unterdrückenden Effekte auf Invasion und Zellgestalt werden abgeschwächt.
Was das für Patientinnen und Patienten bedeutet
Zusammengefasst zeichnen die Befunde eine lineare Schutzachse im Darm nach: TGF‑β aktiviert SMAD4, SMAD4 schaltet 14‑3‑3σ ein, und 14‑3‑3σ fängt TFEB außerhalb des Zellkerns ein. Diese Kombination treibt kolorektale Krebszellen in einen geordneteren, weniger mobilen Zustand und dämpft ihre Selbstreinigungsmechanismen, wodurch sie möglicherweise weniger metastasenfähig und anfälliger für Therapien werden. Gehen SMAD4 oder 14‑3‑3σ verloren, wird TFEB aktiver und könnte sowohl die Zellplastizität als auch die Stressresistenz erhöhen. Obwohl weitere Arbeiten in lebenden Tieren und an klinischen Proben nötig sind, hebt der hier beschriebene Signalweg neue molekulare Ansatzpunkte hervor, an denen zukünftige Medikamente die körpereigenen Abwehrmechanismen gegen metastasiertes kolorektales Karzinom verstärken könnten.
Zitation: Chen, X., Winter, M., Rokavec, M. et al. TGF-β/SMAD4/14-3-3σ/TFEB axis promotes mesenchymal-epithelial transition and inhibits autophagy in colorectal cancer. Cell Death Dis 17, 397 (2026). https://doi.org/10.1038/s41419-026-08733-x
Schlüsselwörter: kolorektales Karzinom, Metastasen, Autophagie, epitheliale Plastizität, TFEB