Clear Sky Science · ru
Ось TGF-β/SMAD4/14-3-3σ/TFEB стимулирует мезенхимально-эпителиальный переход и ингибирует аутофагию при колоректальном раке
Почему это исследование важно для рака толстой кишки
Колоректальный рак является одной из ведущих причин смерти от онкологических заболеваний, поскольку опухолевые клетки часто распространяются из кишечника в отдалённые органы. В этом исследовании обнаружен ранее не распознанный механизм внутри кишечных клеток, который может сдерживать это распространение. Проследив, как несколько молекул взаимодействуют между собой, авторы показывают, как нормальные сигналы в кишечнике способны вернуть раковые клетки к более упорядоченному состоянию и лишить их одного из приемов выживания — самоочищающего процесса, называемого аутофагией.
Защитное послание в кишечнике
Наш кишечник постоянно подвергается воздействию пищи, бактерий и механического стресса, поэтому кишечные клетки опираются на строгие регуляторные системы, чтобы поддерживать равновесие между ростом и ремонтом. Один из ключевых сигналов, называемый TGF‑β, обычно действует как тормоз на ранних этапах опухолевого развития. Он работает через белок SMAD4, который перемещается в ядро клетки и включает или выключает гены. При колоректальном раке SMAD4 часто теряется, и пациенты с опухолями без этого белка, как правило, имеют больше метастазов и хуже прогноз. Авторы поставили цель выяснить, какие конкретно гены контролирует SMAD4 и как это может объяснять его способность блокировать инвазию и распространение.
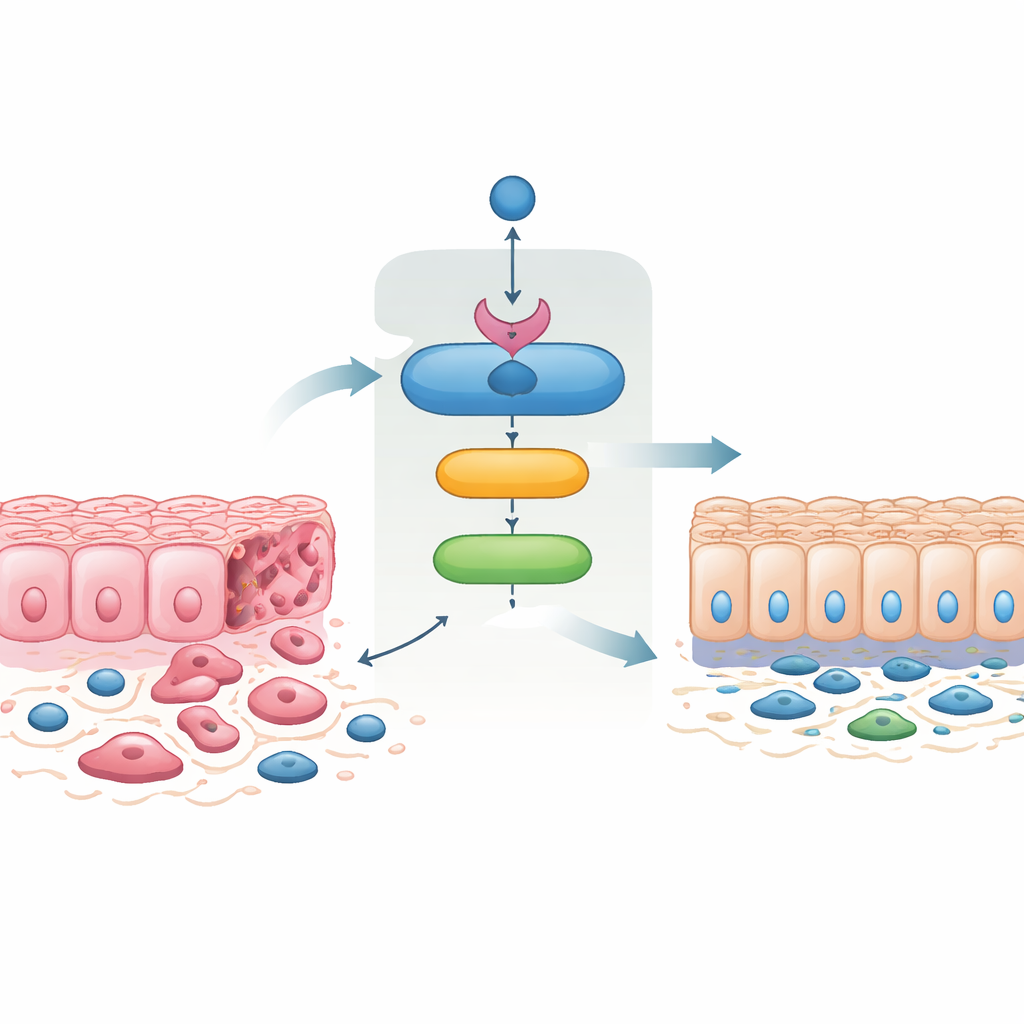
Цепочка защитников внутри раковых клеток
Исследователи обнаружили, что SMAD4 прямо активирует ген 14‑3‑3σ, который давно известен как супрессор опухолей. На моделях человеческих клеточных линий колоректального рака, в органоидах, полученных от пациентов, и в моделях на мышах они показали, что включение SMAD4 надежно повышает уровни 14‑3‑3σ, тогда как удаление SMAD4 предотвращает это повышение. Они выделили сайты связывания для SMAD4 в регуляторном участке гена 14‑3‑3σ и подтвердили, что SMAD4 физически занимает эти сайты, что убедительно устанавливает 14‑3‑3σ как прямую цель как в человеческих, так и в мышиных кишечных клетках. В нормальной мышиной кишечной ткани 14‑3‑3σ особенно обилен на кончиках ворсинок, однако этот рисунок исчезает при делеции Smad4, что подчеркивает тесную связь между ними в процессе дифференцировки ткани.
Возвращение раковых клеток к порядку
Раковые клетки часто претерпевают «эпителиально‑мезенхимальный переход», меняя форму от плотно связанных пластовидных клеток к более подвижным, веретенообразным, что облегчает инвазию и образование метастазов. Обратный процесс, мезенхимально‑эпителиальный переход, восстанавливает плотные клеточные контакты и снижает инвазивность. Когда исследователи восстановили экспрессию SMAD4 в агрессивных клетках колоректального рака, которые обычно его не имеют, клетки сместились в сторону эпителиального фенотипа: они вновь обрели мембранные белки адгезии и утратили признаки подвижности и инвазивности. Такие клетки мигрировали меньше, меньше вторгались через искусственные мембраны и образовывали меньше колоний. Поразительно, что принудительная экспрессия только 14‑3‑3σ вызвала очень похожие изменения, а блокировка 14‑3‑3σ в значительной степени устраняла эффекты SMAD4. Это показывает, что 14‑3‑3σ — не просто попутчик, а ключевой медиатор способности SMAD4 сдерживать инвазивное поведение.
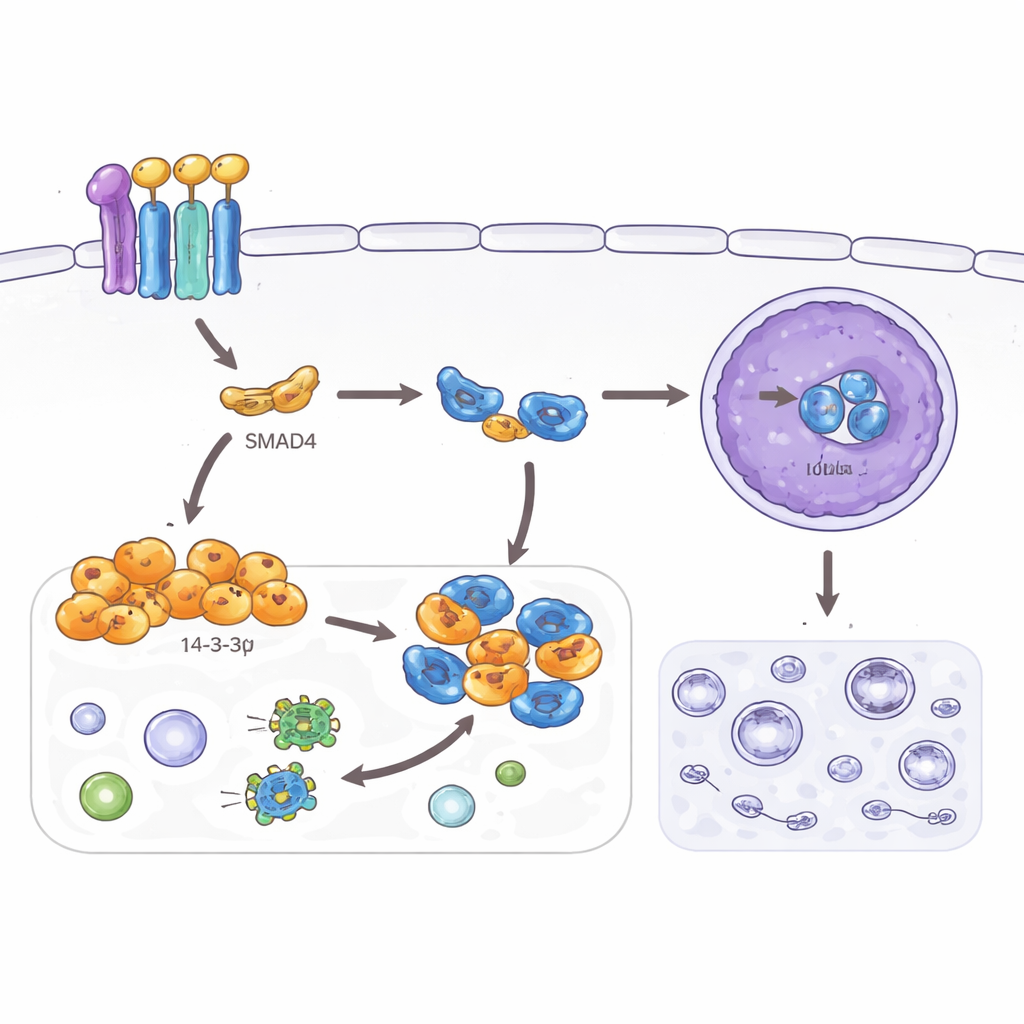
Выключение пути выживания
В работе также изучалась аутофагия — процесс утилизации, который помогает клеткам выживать при стрессе, расщепляя внутриклеточные компоненты. Хотя в нормальных тканях аутофагия полезна, её усиление может помогать раковым клеткам справляться со враждебной средой и лечением. Авторы показали, что SMAD4 и 14‑3‑3σ снижают маркеры аутофагии в клетках колоректального рака и уменьшают число везикул переработки, наблюдаемых под микроскопом. Они проследили этот эффект до другого белка, TFEB, главного регулятора аутофагии и лизосом. Обычно при попадании TFEB в ядро он активирует множество генов, связанных с аутофагией. В данном случае SMAD4‑опосредованная 14‑3‑3σ связывает TFEB в цитоплазме и не дает ему попасть в ядро, но лишь при наличии химической метки в определённой позиции TFEB. При мутации этого сайта 14‑3‑3σ уже не удерживает TFEB, аутофагия возобновляется, а супрессивные эффекты на инвазию и клеточную морфологию ослабевают.
Что это значит для пациентов
В совокупности результаты описывают линейную защитную ось в кишечнике: TGF‑β активирует SMAD4, SMAD4 включает 14‑3‑3σ, а 14‑3‑3σ удерживает TFEB за пределами ядра. Это сочетание толкает клетки колоректального рака к более упорядоченному, менее подвижному состоянию и подавляет их механизм самоочищения, что может снизить их способность к распространению и повысить чувствительность к лечению. При потере SMAD4 или 14‑3‑3σ TFEB становится более активным, что потенциально усиливает как клеточную пластичность, так и устойчивость к стрессу. Хотя необходимы дальнейшие исследования на животных и клинических образцах, выявленный здесь путь указывает новые молекулярные точки, где будущие препараты могли бы укрепить собственные защитные механизмы организма против метастатического колоректального рака.
Цитирование: Chen, X., Winter, M., Rokavec, M. et al. TGF-β/SMAD4/14-3-3σ/TFEB axis promotes mesenchymal-epithelial transition and inhibits autophagy in colorectal cancer. Cell Death Dis 17, 397 (2026). https://doi.org/10.1038/s41419-026-08733-x
Ключевые слова: колоректальный рак, метастазирование, аутофагия, эпителиальная пластичность, TFEB