Clear Sky Science · nl
TGF-β/SMAD4/14-3-3σ/TFEB-as neemt mesenchymale‑epitheliale transitie af en remt autofagie bij colorectale kanker
Waarom deze studie van belang is voor darmkanker
Colorectale kanker is een van de belangrijkste oorzaken van sterfte door kanker omdat tumorcellen vaak vanuit de darm naar verre organen uitzaaien. Deze studie onthult een eerder onopgemerkte beschermingsschakel binnen darmcellen die deze verspreiding kan afremmen. Door in kaart te brengen hoe meerdere moleculen met elkaar communiceren, laten de onderzoekers zien hoe normale signalen in de darm kankercellen kunnen terugduwen naar een meer ordelijke toestand en één van hun overlevingsstrategieën — een zelfreinigend proces genaamd autofagie — kunnen afsnijden.
Een beschermende boodschap in de darm
Onze darmen worden continu blootgesteld aan voedsel, bacteriën en mechanische stress, daarom vertrouwen de cellen in de darm op sterke controlesystemen om groei en herstel in balans te houden. Een belangrijk signaal, TGF‑β genoemd, werkt doorgaans als een rem op vroege tumorgroei. Het werkt via een eiwit genaamd SMAD4, dat naar de celkern gaat en genen aan- of uitzet. Bij colorectale kankers gaat SMAD4 vaak verloren, en patiënten van wie de tumoren dit eiwit missen hebben vaker metastasen en een slechtere overleving. De auteurs wilden begrijpen welke specifieke genen SMAD4 reguleert die zijn vermogen om invasie en verspreiding te blokkeren kunnen verklaren.
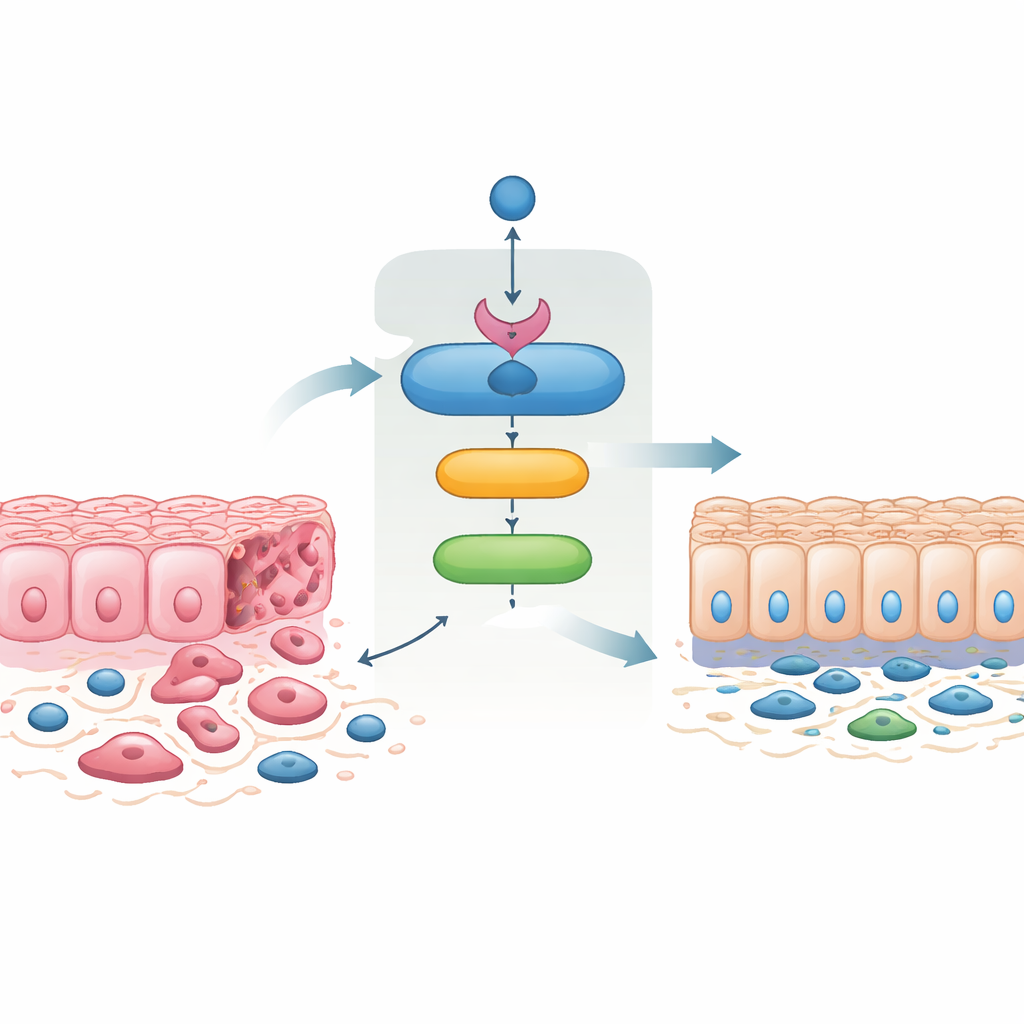
Een keten van beschermers in kankercellen
Het team ontdekte dat SMAD4 rechtstreeks een gen activeert dat 14‑3‑3σ heet, al lang bekend als een tumorsuppressor. Met menselijk colorectaalkanker-cel lijnen, patiënteigen mini‑tumoren gekweekt in het laboratorium, en muismodellen toonden ze aan dat het inschakelen van SMAD4 consequent 14‑3‑3σ‑niveaus verhoogt, terwijl het verwijderen van SMAD4 deze toename verhindert. Ze identificeerden bindingsplaatsen voor SMAD4 in het regelgebied van 14‑3‑3σ en bevestigden dat SMAD4 fysiek deze sites bezet, waarmee 14‑3‑3σ stevig als een direct doelwit in zowel menselijke als muizendarmcellen wordt vastgesteld. In de normale muisdarm is 14‑3‑3σ bijzonder overvloedig aan de top van de villi, maar dit patroon verdwijnt wanneer Smad4 wordt verwijderd, wat benadrukt hoe nauw de twee tijdens weefseldifferentiatie verbonden zijn.
Cankercellen terugduwen naar orde
Cankercellen ondergaan vaak een «epitheliale‑mesenchymale transitie», waarbij ze veranderen van hecht verbonden, velachtige cellen naar mobielere, spoelvormige cellen die makkelijker invasie en metastase veroorzaken. Het omgekeerde proces, mesenchymale‑epitheliale transitie, herstelt nauwe cel‑cel‑contacten en vermindert invasiviteit. Toen de onderzoekers SMAD4 opnieuw inbraken in agressieve colorectale kankercellen die het normaal missen, gingen de cellen meer epitheliale kenmerken vertonen, kregen ze membraangebonden adhesie-eiwitten terug en verloren kenmerken die bij mobiliteit en invasie horen. Deze SMAD4‑herstelde cellen migreerden minder, invadeerden minder door kunstmatige membranen en vormden minder kolonies. Opmerkelijk was dat het kunstmatig verhogen van 14‑3‑3σ alleen zeer vergelijkbare veranderingen teweegbracht, en het blokkeren van 14‑3‑3σ grotendeels de effecten van SMAD4 ongedaan maakte. Dit toont aan dat 14‑3‑3σ niet slechts een omstander is maar een sleutelspeler in SMAD4’s vermogen invasief gedrag te beteugelen.
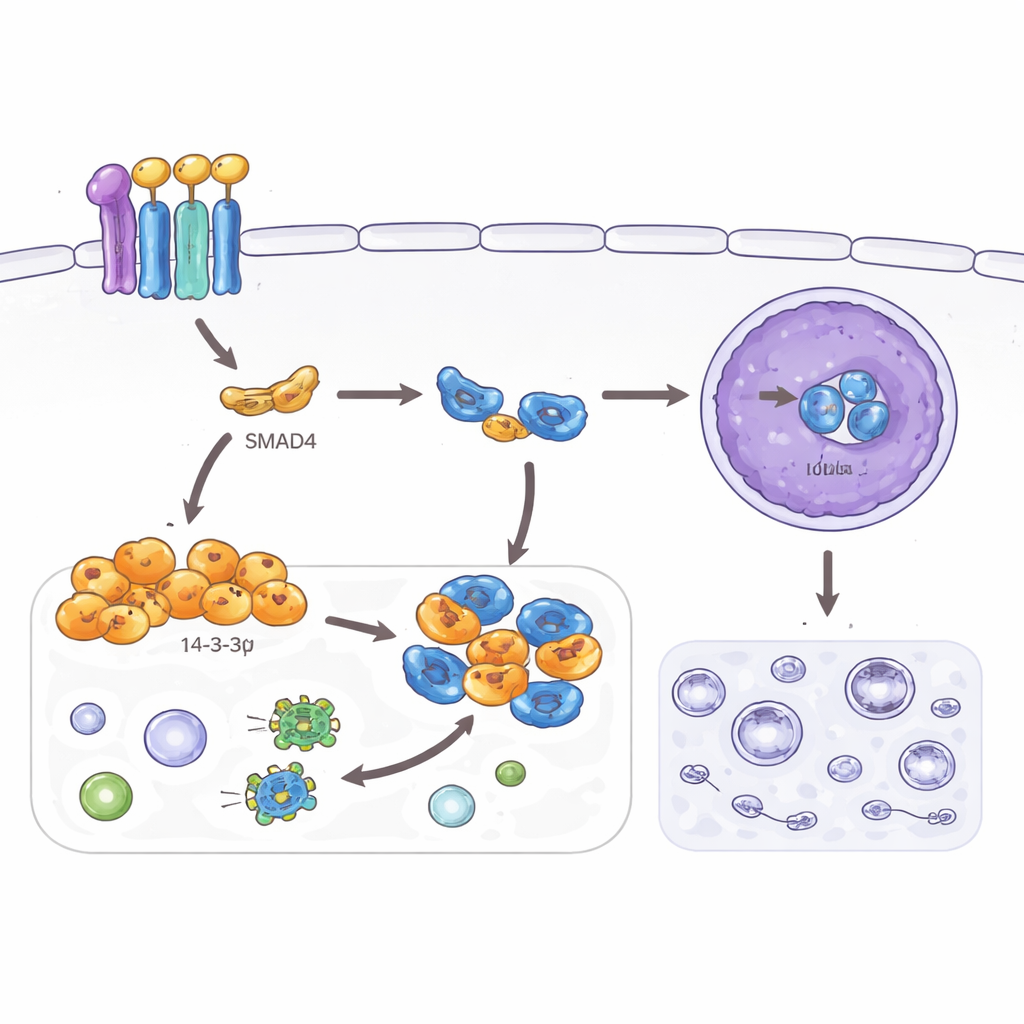
Een overlevingsweg uitschakelen
De studie onderzocht ook autofagie, een recycleprogramma dat cellen helpt te overleven onder stress door interne componenten af te breken. Hoewel nuttig in normale weefsels, kan verhoogde autofagie kankercellen helpen omgaan met vijandige omgevingen en behandelingen. De auteurs vonden dat zowel SMAD4 als 14‑3‑3σ markers van autofagie in colorectale kankercellen verlagen en het aantal recyclingvesikels dat onder de microscoop wordt waargenomen verminderen. Ze brachten dit effect terug tot een ander eiwit, TFEB, een hoofdregelaar van autofagie en lysosomen. Normaal gesproken activeert TFEB, wanneer het de kern binnengaat, veel autofagiegerelateerde genen. Hier bindt SMAD4‑gedreven 14‑3‑3σ TFEB in het buitenste compartiment van de cel en houdt het weg uit de kern, maar alleen wanneer een specifieke plaats op TFEB chemisch is gemarkeerd. Wanneer die plaats gemuteerd is, kan 14‑3‑3σ TFEB niet langer vasthouden, wordt autofagie hervat en verzwakken de remmende effecten op invasie en celvorm.
Wat dit betekent voor patiënten
Gezamenlijk schetsen de bevindingen een lineaire beschermende as in de darm: TGF‑β activeert SMAD4, SMAD4 zet 14‑3‑3σ aan, en 14‑3‑3σ houdt TFEB buiten de kern gevangen. Deze combinatie drijft colorectale kankercellen naar een meer ordelijke, minder mobiele toestand en dempt hun zelfreinigende machinerie, wat ze mogelijk minder in staat maakt uit te zaaien en gevoeliger voor behandeling maakt. Wanneer SMAD4 of 14‑3‑3σ verloren gaan, wordt TFEB actiever, wat zowel celplasticiteit als stressbestendigheid kan verhogen. Hoewel verder werk in levende dieren en klinische monsters nodig is, benadrukt het hier onthulde pad nieuwe moleculaire aanknopingspunten waar toekomstige geneesmiddelen de eigen verdedigingen van het lichaam tegen metastatische colorectale kanker zouden kunnen versterken.
Bronvermelding: Chen, X., Winter, M., Rokavec, M. et al. TGF-β/SMAD4/14-3-3σ/TFEB axis promotes mesenchymal-epithelial transition and inhibits autophagy in colorectal cancer. Cell Death Dis 17, 397 (2026). https://doi.org/10.1038/s41419-026-08733-x
Trefwoorden: colorectale kanker, metastase, autofagie, epitheliale plasticiteit, TFEB