Clear Sky Science · fr
L’axe TGF-β/SMAD4/14-3-3σ/TFEB favorise la transition mésenchymo-épithéliale et inhibe l’autophagie dans le cancer colorectal
Pourquoi cette étude est importante pour le cancer du côlon
Le cancer colorectal est l’une des principales causes de mortalité par cancer parce que les cellules tumorales se propagent souvent de l’intestin vers des organes distants. Cette étude met au jour un circuit de sécurité jusque-là méconnu au sein des cellules intestinales qui peut freiner cette dissémination. En cartographiant les interactions entre plusieurs molécules, les chercheurs montrent comment des signaux normaux de l’intestin peuvent repousser les cellules cancéreuses vers un état plus ordonné et couper l’un de leurs stratagèmes de survie : un processus d’auto-nettoyage appelé autophagie.
Un message protecteur dans l’intestin
Nos intestins sont constamment exposés aux aliments, aux bactéries et aux contraintes mécaniques ; les cellules intestinales s’appuient donc sur des systèmes de contrôle robustes pour maintenir l’équilibre entre croissance et réparation. Un signal majeur, appelé TGF‑β, joue généralement un rôle de frein au cours des premières étapes de la tumeur. Il agit via une protéine nommée SMAD4, qui migre dans le noyau cellulaire et active ou réprime des gènes. Dans les cancers colorectaux, SMAD4 est fréquemment perdu, et les patients dont les tumeurs sont dépourvues de cette protéine présentent en général davantage de métastases et un pronostic plus mauvais. Les auteurs ont cherché à identifier quels gènes spécifiques sont régulés par SMAD4 et pourraient expliquer sa capacité à bloquer l’invasion et la dispersion.
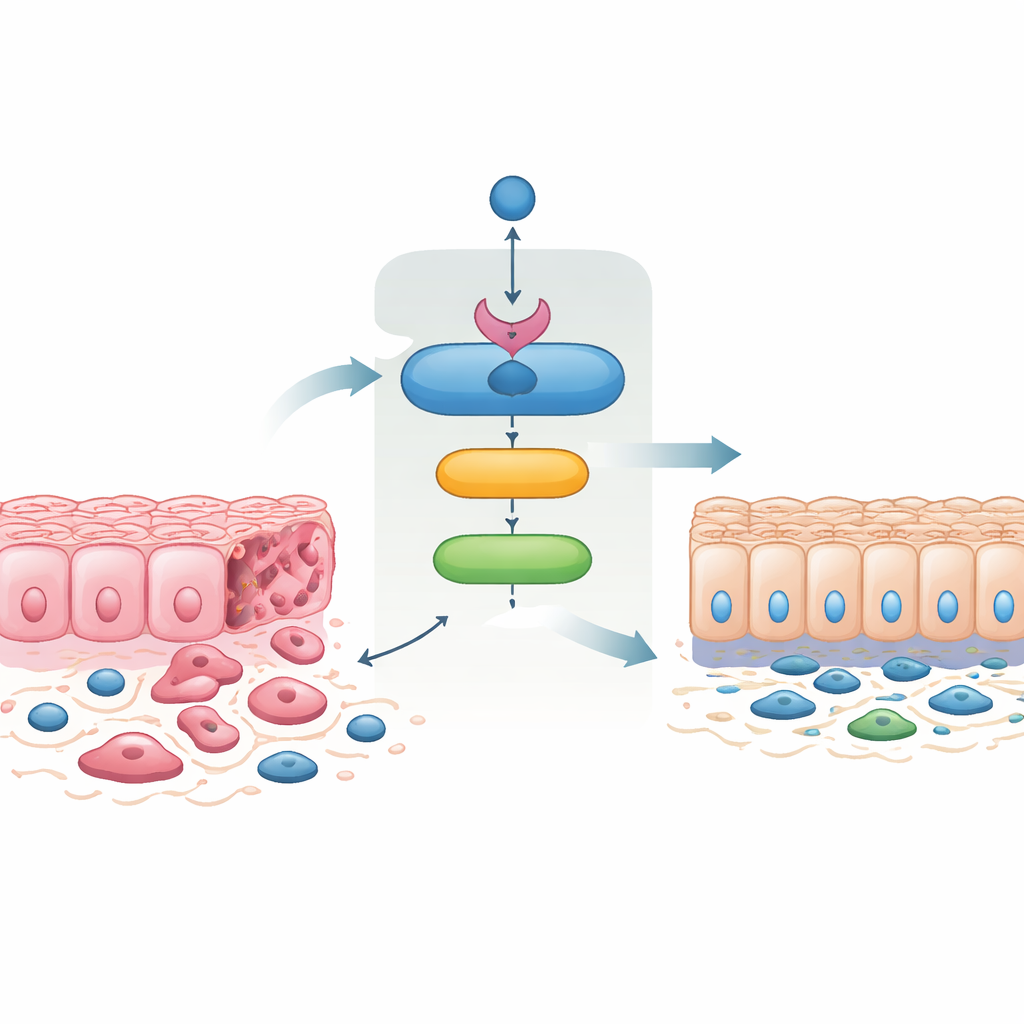
Une chaîne de sentinelles à l’intérieur des cellules cancéreuses
L’équipe a découvert que SMAD4 active directement un gène appelé 14‑3‑3σ, connu depuis longtemps comme un suppresseur de tumeur. En utilisant des lignées cellulaires humaines de cancer colorectal, des mini‑tumeurs dérivées de patients cultivées en laboratoire et des modèles murins, ils ont montré que l’expression de SMAD4 augmente systématiquement les niveaux de 14‑3‑3σ, tandis que la perte de SMAD4 empêche cette hausse. Ils ont identifié des sites d’ancrage pour SMAD4 dans la région de contrôle de 14‑3‑3σ et confirmé que SMAD4 occupe physiquement ces sites, établissant fermement 14‑3‑3σ comme une cible directe aussi bien dans les cellules intestinales humaines que murines. Dans l’intestin normal de la souris, 14‑3‑3σ est particulièrement abondant au sommet des villosités, mais ce schéma disparaît lorsque Smad4 est supprimé, soulignant l’étroite corrélation entre les deux lors de la différenciation tissulaire.
Ramener les cellules cancéreuses vers l’ordre
Les cellules cancéreuses subissent souvent une « transition épithélio‑mésenchymateuse », passant d’une organisation en feuillets serrés à des cellules plus mobiles en forme de fuseau, qui envahissent plus facilement et forment des métastases. Le processus inverse, la transition mésenchymo‑épithéliale, restaure des contacts cellule‑cellule serrés et réduit l’invasivité. Lorsque les chercheurs ont réintroduit SMAD4 dans des cellules de cancer colorectal agressives qui en sont dépourvues, les cellules ont adopté un aspect plus épithélial, ont retrouvé des protéines d’adhésion membranaires et ont perdu des caractéristiques liées à la mobilité et à l’invasion. Ces cellules restaurées par SMAD4 migraient moins, traversaient moins les membranes artificielles et formaient moins de colonies. De manière remarquable, forcer l’expression de 14‑3‑3σ seul produisait des changements très similaires, et bloquer 14‑3‑3σ annulait en grande partie les effets de SMAD4. Cela montre que 14‑3‑3σ n’est pas un simple spectateur mais un médiateur clé de la capacité de SMAD4 à maîtriser le comportement invasif.
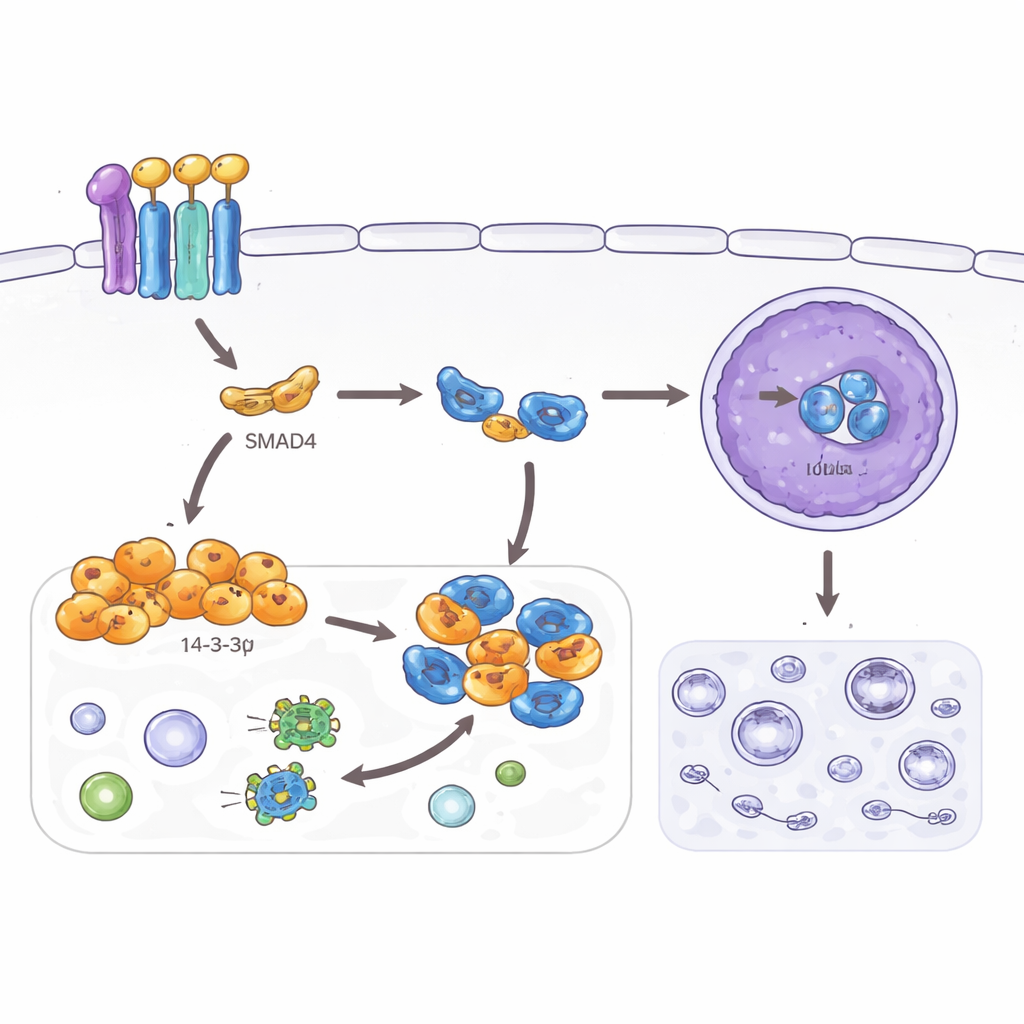
Éteindre une voie de survie
L’étude a également examiné l’autophagie, un programme de recyclage qui aide les cellules à survivre au stress en dégradant des composants internes. Si l’autophagie est utile dans les tissus normaux, son augmentation peut aider les cellules cancéreuses à faire face à des environnements hostiles et aux traitements. Les auteurs ont constaté que SMAD4 et 14‑3‑3σ réduisent tous deux des marqueurs d’autophagie dans les cellules de cancer colorectal et diminuent le nombre de vésicules de recyclage observées au microscope. Ils ont relié cet effet à une autre protéine, TFEB, un régulateur maître de l’autophagie et des lysosomes. Normalement, lorsque TFEB pénètre dans le noyau, il active de nombreux gènes liés à l’autophagie. Ici, 14‑3‑3σ induit par SMAD4 se lie à TFEB dans le compartiment cytoplasmique et l’empêche d’atteindre le noyau, mais seulement lorsque un site spécifique sur TFEB a été modifié chimiquement. Lorsque ce site est muté, 14‑3‑3σ ne peut plus retenir TFEB, l’autophagie reprend et les effets suppressifs sur l’invasion et la morphologie cellulaire sont affaiblis.
Ce que cela signifie pour les patients
Dans l’ensemble, ces résultats décrivent un axe protecteur linéaire dans l’intestin : TGF‑β active SMAD4, SMAD4 active 14‑3‑3σ, et 14‑3‑3σ piège TFEB à l’extérieur du noyau. Cette combinaison pousse les cellules de cancer colorectal vers un état plus ordonné et moins mobile et atténue leur machinerie d’auto‑nettoyage, ce qui peut réduire leur capacité à se disséminer et les rendre plus sensibles aux traitements. Lorsque SMAD4 ou 14‑3‑3σ sont perdus, TFEB devient plus actif, ce qui peut renforcer à la fois la plasticité cellulaire et la résistance au stress. Bien que des travaux complémentaires in vivo et sur des échantillons cliniques soient nécessaires, la voie révélée ici met en évidence de nouveaux points moléculaires où de futurs médicaments pourraient renforcer les défenses naturelles de l’organisme contre le cancer colorectal métastatique.
Citation: Chen, X., Winter, M., Rokavec, M. et al. TGF-β/SMAD4/14-3-3σ/TFEB axis promotes mesenchymal-epithelial transition and inhibits autophagy in colorectal cancer. Cell Death Dis 17, 397 (2026). https://doi.org/10.1038/s41419-026-08733-x
Mots-clés: cancer colorectal, métastase, autophagie, plasticité épithéliale, TFEB