Clear Sky Science · he
ציר TGF-β/SMAD4/14-3-3σ/TFEB מעודד מעבר מזנכימלי לאפיתלי ומעכב אוטופגיה בסרטן המעי הגס
מדוע המחקר הזה חשוב לסרטן המעי הגס
סרטן המעי הגס הוא אחד הגורמים המובילים לתמותה מסרטן מכיוון שתאי הגידול לעתים קרובות מתפשטים מהמעי לאיברים מרוחקים. מחקר זה חושף מעגל בקרה פנימי בתאי המעי שלא זוהה קודם, שיכול להגביל הפצה כזו. באמצעות שרטוט האינטראקציות בין מספר מולקולות, החוקרים מראים כיצד אותות רגילים במעי יכולים להחזיר תאי סרטן למצב מסודר יותר ולחתוך אחת מהטריקות שלהם להישרדות — תהליך ניקוי עצמי המכונה אוטופגיה.
מסר מגן במעי
המעיים שלנו חשופים כל הזמן למזון, לחיידקים וללחצים מכניים, ולכן התאים במעי מסתמכים על מערכות בקרה חזקות כדי לשמור על איזון בין גדילה ותיקון. אות מרכזי אחד, הנקרא TGF‑β, בדרך כלל פועל כבלם בשלבים המוקדמים של התפתחות גידול. הוא פועל דרך חלבון בשם SMAD4, שנע אל גרעין התא ומדליק או מכבה גנים. בסרטני המעי הגס לעתים קרובות יש אובדן של SMAD4, ומטופלים שלגידולים שלהם חסר חלבון זה נוטים לפתח יותר גרורות ולהישרד פחות טוב. המחברים שאפו להבין אילו גנים ספציפיים SMAD4 שולט בהם שעשויים להסביר את יכולתו לחסום פלישה והפצה.
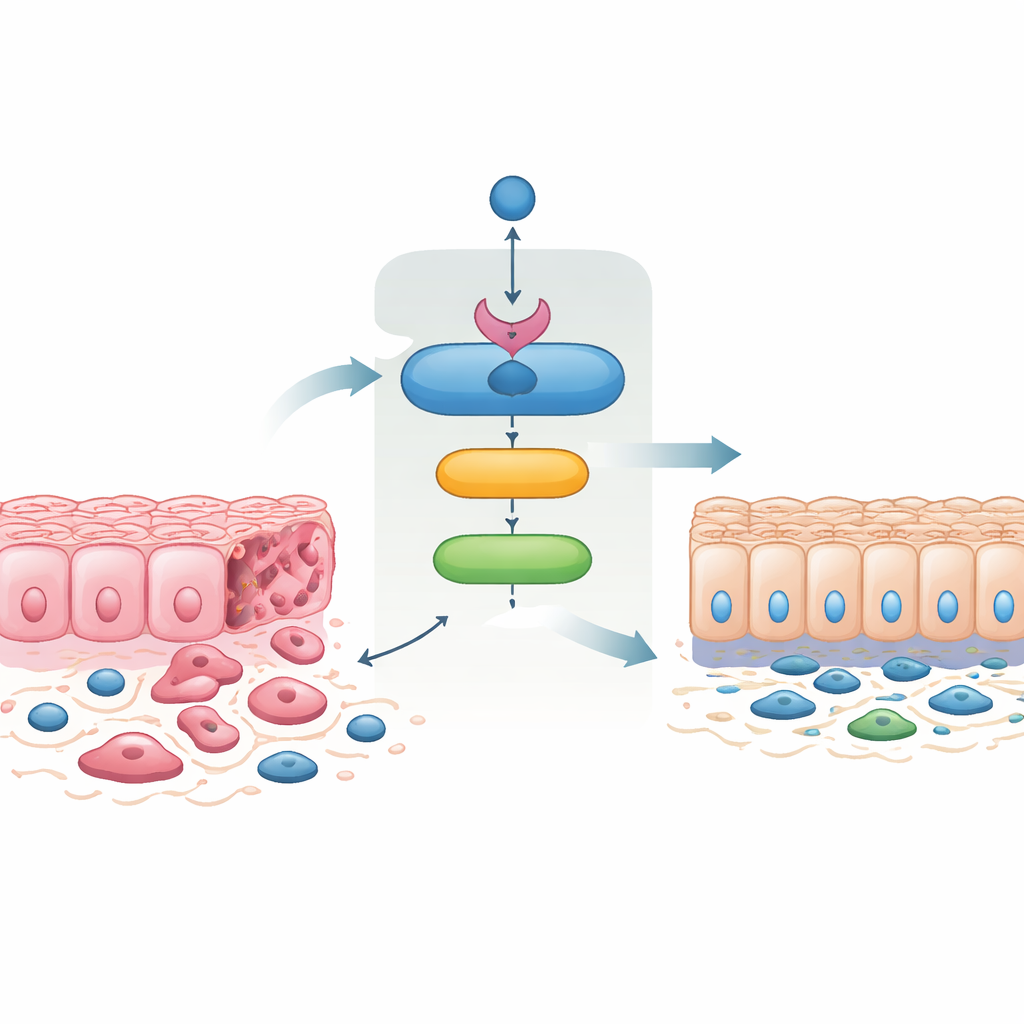
שרשרת מגינים בתוך תאי הסרטן
הצוות גילה כי SMAD4 מפעיל ישירות גן הנקרא 14‑3‑3σ, שנודע שנים רבות כמדכא גידולים. בעזרת קו־תאי סרטן המעי האנושי, גידולי מיני‑מטופל שמקורם בחולים שגודלו במעבדה, ומודלים עכבריים, הם הראו שהחזרת ביטוי של SMAD4 מעלה באופן אמין את רמות 14‑3‑3σ, בעוד שהסרת SMAD4 מונעת עלייה זו. הם זיהו אתרי עגינה ל‑SMAD4 באזור הבקרה של 14‑3‑3σ ואישרו ש‑SMAD4 תופס פיזית את האתרים הללו, ובכך קבעו באופן מוצק כי 14‑3‑3σ הוא יעד ישיר הן בתאי מעי אנושיים והן בעכברים. במעי עכבר תקין, 14‑3‑3σ רב במיוחד בקצות הוילי, אך דפוס זה נעלם כאשר Smad4 נמחק, מה שמדגיש כמה הם מקושרים במהלך ההבחנה הרקמתית.
דוחפים את תאי הסרטן חזרה לסדר
תאי סרטן עוברים לעתים קרובות "מעבר אפיתלי‑מזנכימלי", שבו הם משתנים מתאים דבוקים סדירים לצורת נדן ניידת יותר שמקלה על פלישה ויצירת גרורות. התהליך ההפוך, מעבר מזנכימלי‑אפיתלי, משחזר מגעים הדוקים בין התאים ומצמצם את הפלישות. כאשר החוקרים החזירו SMAD4 לתאי סרטן מעי אגרסיביים שהיו חסרי החלבון, התאים נטו לעבר מראה אפיתלי, החזירו חלבוני דבקות ממברנליים ולאחרו תכונות הקשורות לניידות ולפלישה. תאים שבהם הושבו SMAD4 נדדו פחות, חדרו פחות דרך ממברנות מלאכותיות ויצרו פחות קולוניות. באופן מרשים, אילוץ ביטוי של 14‑3‑3σ בלבד נתן שינויים דומים מאוד, וחסימת 14‑3‑3σ מוחקת ברובה את השפעות SMAD4. ממצא זה מראה ש‑14‑3‑3σ אינו רק תופעה לוואי אלא מתאם מרכזי ביכולתו של SMAD4 לרסן התנהגות פולשנית.
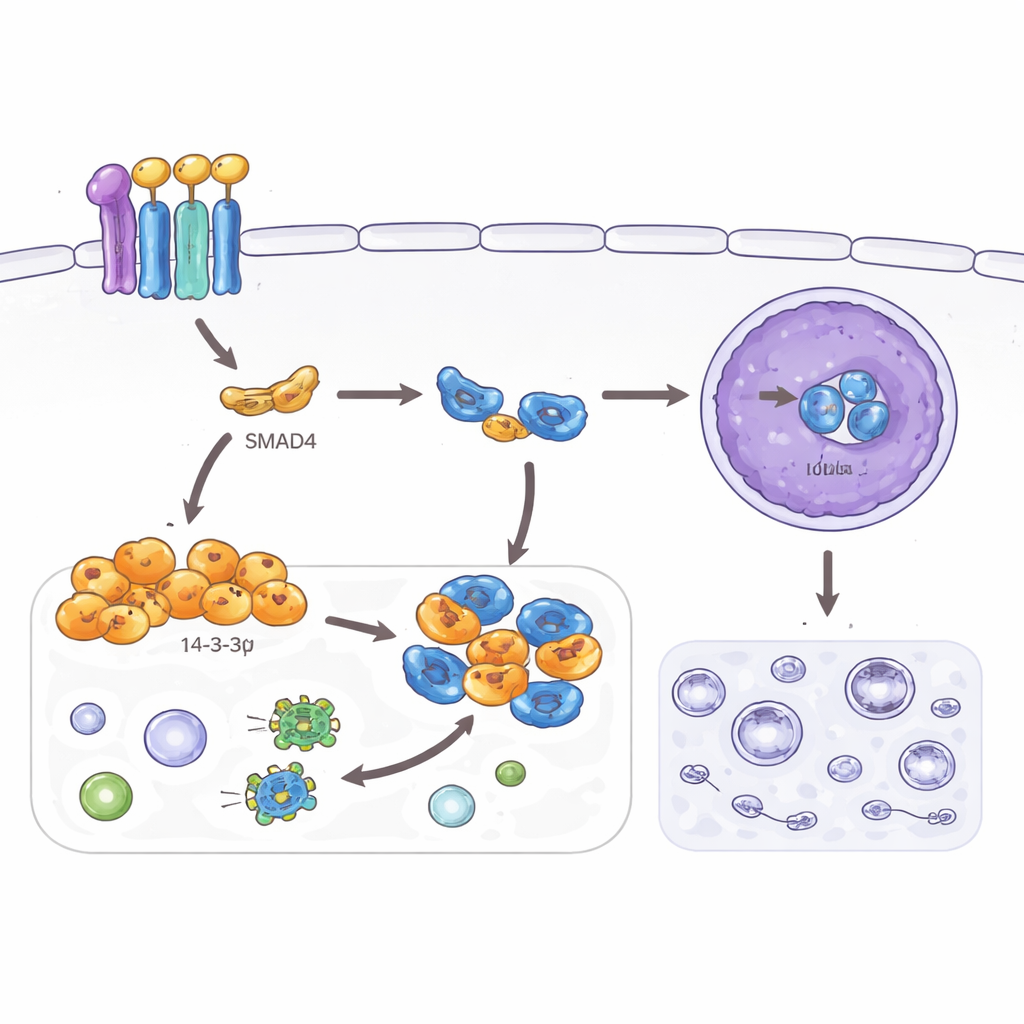
כיבוי מסלול הישרדות
המחקר בחן גם את האוטופגיה, תוכנית מיחזור המסייעת לתאים לשרוד לחץ על ידי פירוק רכיבים פנימיים. אף שחשובה ברקמות תקינות, אוטופגיה מוגברת יכולה לעזור לתאי סרטן להתמודד עם סביבות עוינות וטיפולים. המחברים גילו ש‑SMAD4 ו‑14‑3‑3σ שניהם מפחיתים סמן של אוטופגיה בתאי סרטן המעי ומקטינים את מספר הווסיקולות הממוחזרות הנצפות במיקרוסקופ. הם עקבו אחרי ההשפעה עד לחלבון נוסף, TFEB, בורר ראשי של אוטופגיה וליזוזומים. באופן רגיל, כאשר TFEB נכנס לגרעין הוא מפעיל גנים רבים הקשורים לאוטופגיה. כאן, 14‑3‑3σ שמופעל על ידי SMAD4 קושר את TFEB במצע הציטופלזמטי ומונע ממנו להגיע לגרעין, אך רק כאשר אתר ספציפי על TFEB מסומן כימית. כאשר אתר זה מוטנטי, 14‑3‑3σ כבר לא יכול לעצור את TFEB, האוטופגיה חוזרת וההשפעות המדכאות על פלישה וצורת התא נחלשות.
מה המשמעות עבור מטופלים
בצירוף ממצאים אלו, התוצאות מרשימות ציר מגן ליניארי במעי: TGF‑β מפעיל את SMAD4, SMAD4 מדליק את 14‑3‑3σ, ו‑14‑3‑3σ כלוא את TFEB מחוץ לגרעין. שילוב זה דוחף תאי סרטן המעי הגס לעבר מצב מסודר ופחות נייד וממנע את מכונת הניקוי העצמית שלהם, מה שעשוי להפחית את יכולתם להתפשט ולהגביר את הרגישות שלהם לטיפול. כאשר SMAD4 או 14‑3‑3σ נאבדים, TFEB פעיל יותר, מה שעשוי להגביר הן את הגמישות התאית והן את עמידות ללחץ. אף שדרושות עבודות נוספות בחיות ובמדגמי קליניים, הנתיב המתואר כאן מדלל נקודות מולקולריות חדשות שבהן תרופות עתידיות עשויות לחזק את ההגנות הטבעיות של הגוף נגד סרטן המעי הגס הממאיר והגרורתי.
ציטוט: Chen, X., Winter, M., Rokavec, M. et al. TGF-β/SMAD4/14-3-3σ/TFEB axis promotes mesenchymal-epithelial transition and inhibits autophagy in colorectal cancer. Cell Death Dis 17, 397 (2026). https://doi.org/10.1038/s41419-026-08733-x
מילות מפתח: סרטן המעי הגס, גרורות, אוטופגיה, גמישות אפיתלית, TFEB