Clear Sky Science · zh
拮抗性的 SMAD2/3 对肌成纤维细胞中 TIMP-1、VEGF-A 与缺氧信号的控制塑造肺癌组织学类型特异性的血管生成
为何肺肿瘤中的血管很重要
肺癌并非单一疾病,不同组织学类型的患者常对相同药物有截然不同的反应。本研究提出了一个简单但关键的问题:为何某些常见的肺肿瘤能够建立起丰富的血管网络,而另一些则在低氧区域受限——围绕肿瘤的瘢痕样组织如何决定这一结果?理解癌细胞、支持细胞与血管之间这种隐秘的对话,有助于指导更精准的治疗并提升化疗与免疫疗法的疗效。
两种常见肺癌,两个血管格局
作者将注意力集中在两种主要的非小细胞肺癌:通常出现在肺外侧的腺癌,以及更常在中央气道附近形成的鳞状细胞癌。通过分析来自大型公共数据库的数千例患者样本与影像,他们发现腺癌通常血供更丰富,血管通道更宽、与血管生长相关基因的活性更强。相反,鳞癌更常显示血供不足的特征,包括大量坏死组织和高表达的缺氧标志物,表明氧气匮乏。这种血管学差异在考虑年龄、肿瘤分期和吸烟史等临床变量后仍然存在。 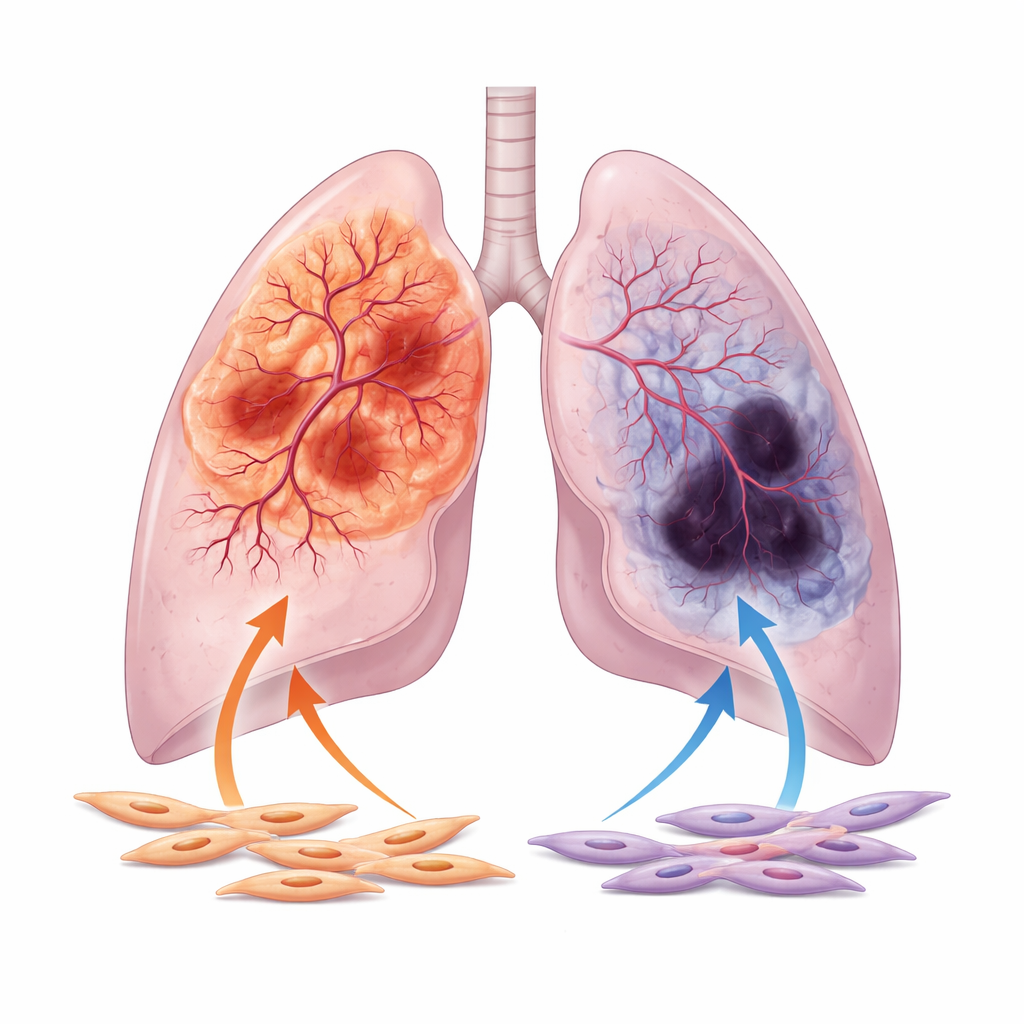
肿瘤成纤维细胞的低调力量
随后研究聚焦于肿瘤相关成纤维细胞——这些具收缩性的肌成纤维样细胞围绕并浸润肺肿瘤。它们以产生瘢痕组织而闻名,同时分泌许多可促进或抑制血管生长的物质。通过单细胞 RNA 测序,研究者发现腺癌中的成纤维细胞与邻近内皮细胞(血管的构建模块)之间的相互作用比鳞癌中的更为强烈。在体外实验中,从腺癌成纤维细胞收集的培养上清使内皮细胞迁移并形成致密、相互交织的毛细血管样网络,而来自鳞癌成纤维细胞的上清则诱导出更弱、更稀疏的结构。
关键信使:VEGF、TIMP-1 与分子开关
为找出负责信号分子,研究团队分析了数十种分泌因子。腺癌成纤维细胞特别高表达 VEGF-A——新生血管的经典驱动因子——以及 TIMP-1,一种通常被视为抑制组织降解酶的蛋白。在此情境下,TIMP-1 展现出不同面貌:在受控实验中,加入 TIMP-1 能增加内皮网络的分支复杂度,形成肿瘤血管典型的纠结结构。从腺癌成纤维细胞中去除 TIMP-1 会显著降低体外的血管分支,并在小鼠体内减少血管密度和肿瘤生长。关键是,这种分支效应依赖于基础水平的 VEGF 信号,提示 VEGF 为油门,而 TIMP-1 则微调最终血管结构的混乱程度。
生长与缺氧的相对调控
在这些差异的背后,是成纤维细胞内一枚分子“开关”,平衡两种相关蛋白 SMAD2 与 SMAD3,它们负责转导来自生长因子 TGF-β 的信号。腺癌成纤维细胞偏向于 SMAD3,高 SMAD3 对 SMAD2 的比率驱动 VEGF-A、TIMP-1 及其他促血管因子的过度产生。当研究者在这些细胞中下调 SMAD3 时,它们刺激内皮细胞迁移、分支和肿瘤血管化的能力崩溃。鳞癌成纤维细胞则常受吸烟诱导的表观遗传改变影响,呈现相反模式:SMAD3 被沉默而 SMAD2 上调。这一状态提高了与缺氧相关的基因及低氧反应主控因子 HIF-1α,但矛盾地并未转化为强烈的 VEGF-A 产出。因此,这类肿瘤仍保持较高的缺氧与坏死,尽管内部有强烈的“低氧”警报,却缺乏对新血管的有力支持。 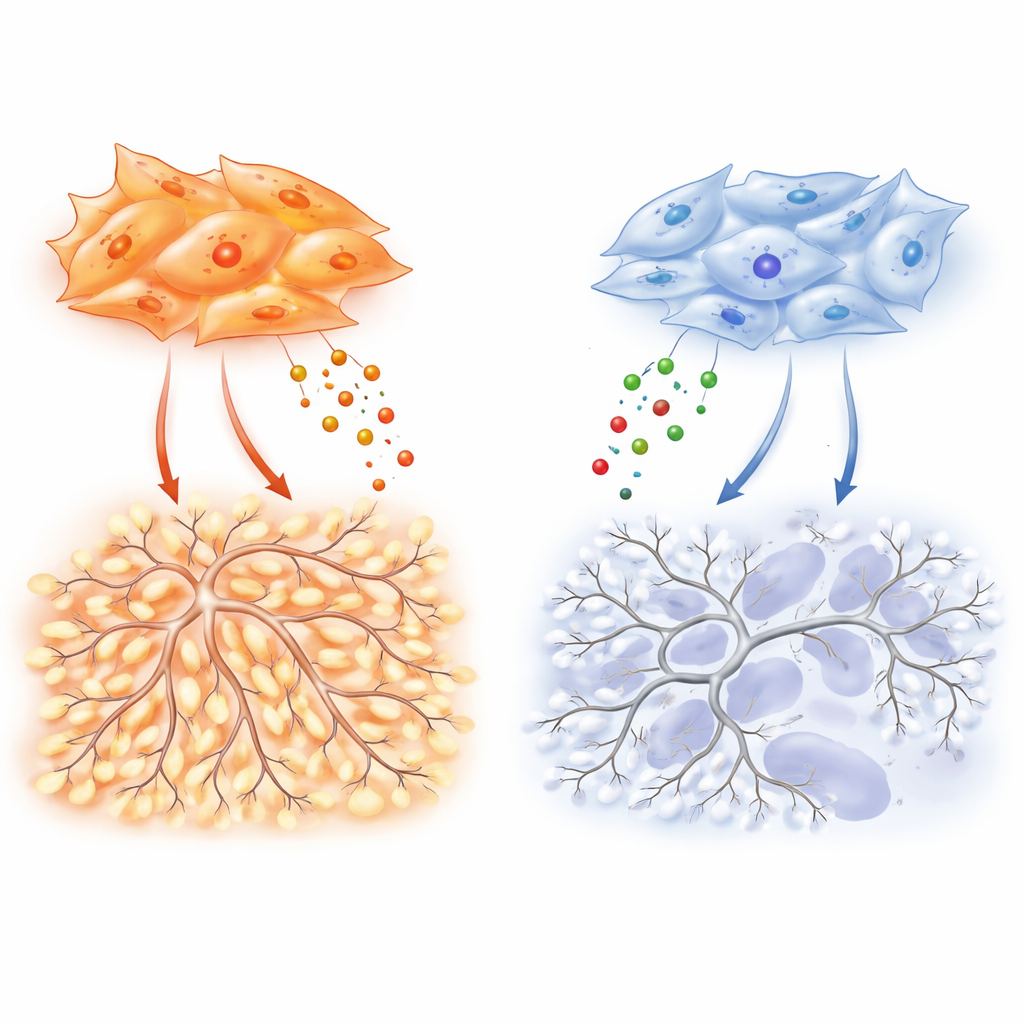
对患者与未来疗法的意义
将血管行为与每种肿瘤类型中成纤维细胞的程序联系起来,有助于解释为何抗血管生成药物在腺癌中比在鳞癌中更有效。在腺癌中,针对 SMAD3–VEGF–TIMP-1 轴既可能使异常血管正态化,又可能缓解局部免疫抑制,从而提高免疫检查点抑制疗法的效能。在鳞癌中,成纤维细胞营造的是一种严酷、缺氧且酸性更强的环境,而非强烈的血管生长,因此缓解缺氧、中和酸性或阻断特定炎症信号的疗法,可能比传统的抗血管生成策略更有希望。对患者而言,这项研究强调了血管与免疫靶向治疗的成功,不仅取决于癌细胞本身,还受那片默默指挥肿瘤血供的纤维基质影响。
引用: Díaz-Valdivia, N., Duch, P., Ikemori, R. et al. Antagonistic SMAD2/3 control of TIMP-1, VEGF-A, and hypoxia signaling in myofibroblasts shapes histotype-specific angiogenesis in lung cancer. Cell Death Dis 17, 431 (2026). https://doi.org/10.1038/s41419-026-08677-2
关键词: 肺癌血管生成, 肿瘤相关成纤维细胞, VEGF 与 TIMP-1, 肿瘤微环境, SMAD 信号传导