Clear Sky Science · fr
Contrôle antagoniste par SMAD2/3 de TIMP-1, VEGF-A et de la signalisation hypoxique dans les myofibroblastes façonnant l’angiogenèse histotype-spécifique dans le cancer du poumon
Pourquoi les vaisseaux sanguins dans les tumeurs pulmonaires comptent
Le cancer du poumon n’est pas une seule maladie, et des patients porteurs de tumeurs de types différents répondent souvent très différemment aux mêmes traitements. Cette étude pose une question simple mais cruciale : pourquoi certaines tumeurs pulmonaires courantes développent-elles des réseaux vasculaires abondants tandis que d’autres s’asphyxient dans des poches à faible oxygène — et comment le tissu cicatriciel environnant contribue-t-il à décider du résultat ? Comprendre cette conversation cachée entre cellules cancéreuses, cellules de soutien et vaisseaux sanguins pourrait orienter des traitements plus précis et améliorer le succès à la fois de la chimiothérapie et de l’immunothérapie.
Deux cancers pulmonaires courants, deux paysages vasculaires
Les auteurs se concentrent sur les deux formes majeures de cancer du poumon non à petites cellules : l’adénocarcinome, qui apparaît souvent en périphérie du poumon, et le carcinome épidermoïde, qui tend à se former plus près des voies aériennes centrales. En analysant des milliers d’échantillons de patients et d’images issues de grandes bases de données publiques, ils montrent que les adénocarcinomes sont généralement mieux vascularisés, avec des canaux vasculaires plus larges et une activité plus forte des gènes liés à la croissance des vaisseaux. En revanche, les tumeurs épidermoïdes présentent plus souvent des signes de mauvaise irrigation sanguine, notamment des nécroses étendues et des niveaux élevés de marqueurs d’hypoxie, témoignant d’un manque d’oxygène. Cette dichotomie du comportement vasculaire persiste même après prise en compte de variables cliniques telles que l’âge, le stade tumoral et les antécédents tabagiques. 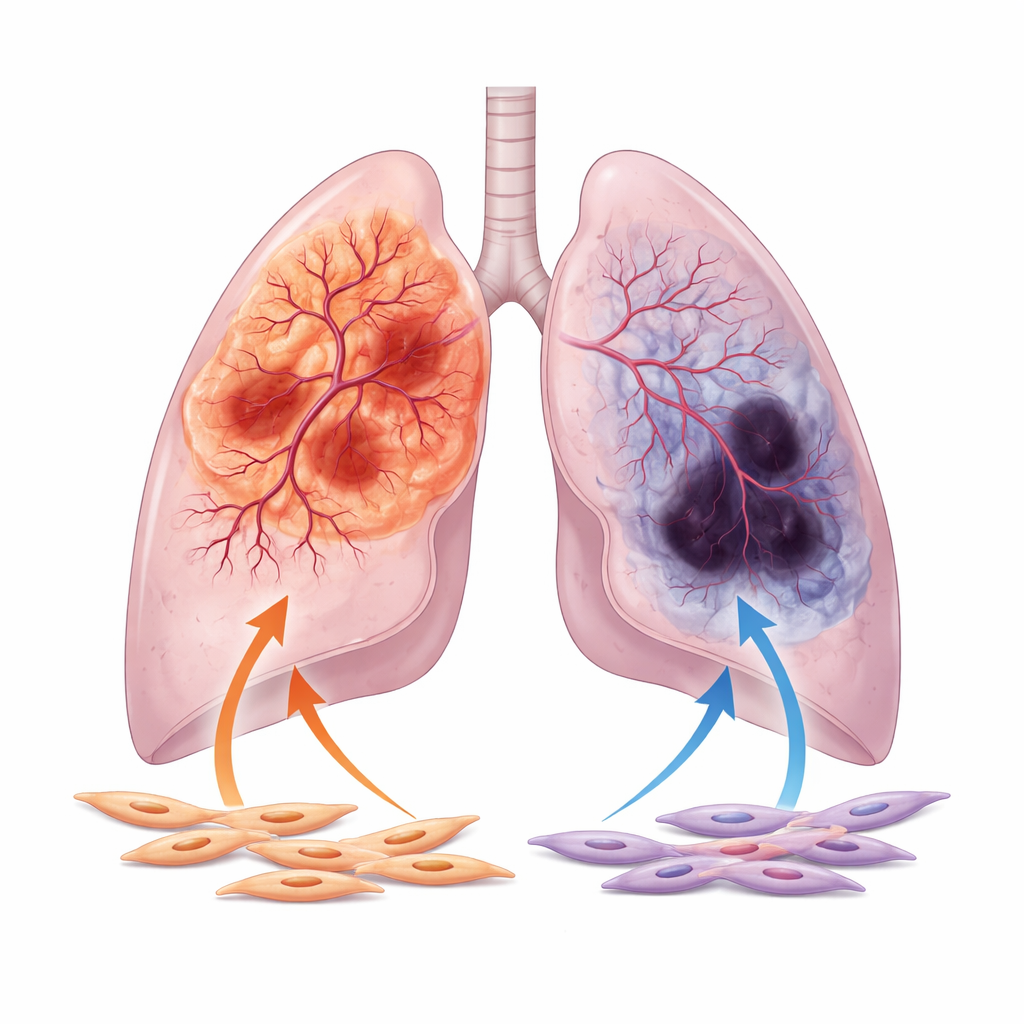
Le pouvoir discret des fibroblastes tumoraux
L’attention se tourne ensuite vers les fibroblastes associés aux tumeurs, ces cellules contractiles de type myofibroblaste qui entourent et infiltrent les tumeurs pulmonaires. Ces cellules, mieux connues pour produire du tissu cicatriciel, sécrètent aussi de nombreuses substances pouvant soit encourager soit freiner la croissance vasculaire. Grâce au séquençage ARN unicellulaire, les chercheurs constatent que les fibroblastes dans l’adénocarcinome interagissent plus intensément avec les cellules endothéliales voisines, éléments constitutifs des vaisseaux sanguins, que ceux présents dans les tumeurs épidermoïdes. En culture, le milieu conditionné par les fibroblastes d’adénocarcinome pousse les cellules endothéliales à migrer et à former des réseaux capillaires denses et entrelacés, tandis que le milieu issu des fibroblastes épidermoïdes induit des structures beaucoup plus faibles et clairsemées.
Messagers clés : VEGF, TIMP-1 et un interrupteur moléculaire
Pour identifier les signaux en jeu, l’équipe profile des dizaines de facteurs sécrétés. Les fibroblastes d’adénocarcinome produisent des niveaux particulièrement élevés de VEGF-A, un moteur classique de la néovascularisation, et de TIMP-1, une protéine mieux connue comme frein des enzymes dégradant la matrice. Ici, TIMP-1 révèle un autre visage : dans des expériences contrôlées, l’ajout de TIMP-1 augmente la complexité des ramifications des réseaux endothéliaux, générant les architectures emmêlées typiques des vaisseaux tumoraux. L’élimination de TIMP-1 chez les fibroblastes d’adénocarcinome réduit fortement le branchement des vaisseaux en culture et diminue la densité vasculaire ainsi que la croissance tumorale chez la souris. Crucialement, cet effet de branchement dépend d’un niveau basal de signalisation VEGF, ce qui suggère que le VEGF joue le rôle d’accélérateur tandis que TIMP-1 ajuste la façon dont la vascularisation résultante devient chaotique.
Contrôles opposés de la croissance versus l’hypoxie
À la base de ces différences se trouve un « interrupteur » moléculaire à l’intérieur des fibroblastes qui équilibre deux protéines apparentées, SMAD2 et SMAD3, qui relaient les signaux du facteur de croissance TGF-β. Les fibroblastes d’adénocarcinome favorisent SMAD3, et ce rapport élevé SMAD3/SMAD2 entraîne la surproduction de VEGF-A, TIMP-1 et d’autres facteurs promoteurs de vaisseaux. Lorsque les chercheurs diminuent SMAD3 dans ces cellules, leur capacité à stimuler la migration endothéliale, le branchement et la vascularisation tumorale s’effondre. Les fibroblastes épidermoïdes, souvent modelés par des altérations épigénétiques liées au tabagisme, montrent le schéma inverse : SMAD3 est silencé et SMAD2 est augmenté. Cet état stimule les gènes liés à l’hypoxie et HIF-1α, un régulateur maître des réponses au faible oxygène, mais paradoxalement ne se traduit pas par une forte production de VEGF-A. En conséquence, ces tumeurs restent plus hypoxiques et nécrotiques, avec un soutien plus faible à la néovascularisation malgré une forte alarme interne de « manque d’oxygène ». 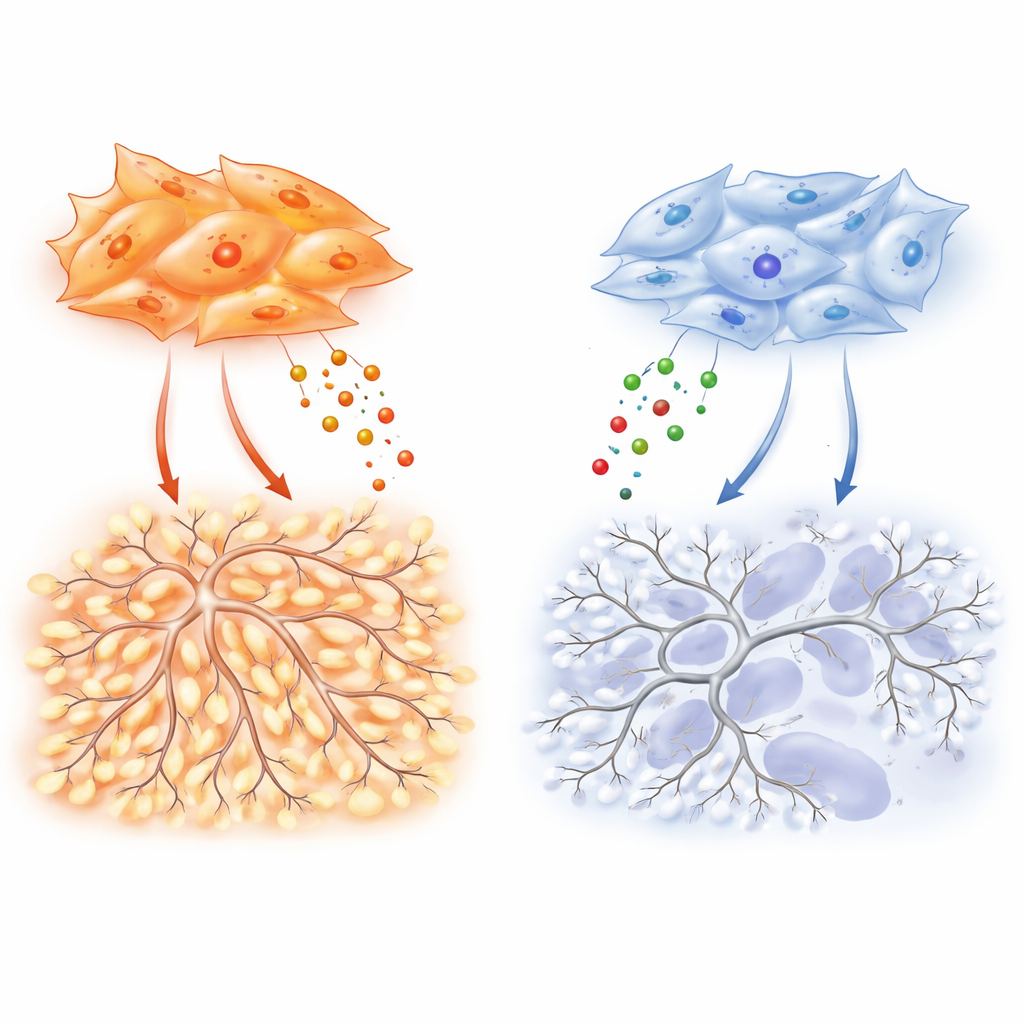
Ce que cela signifie pour les patients et les thérapies futures
En reliant le comportement des vaisseaux aux programmes des fibroblastes propres à chaque type tumoral, l’étude aide à expliquer pourquoi les médicaments anti-angiogéniques ont été plus efficaces dans l’adénocarcinome que dans le cancer pulmonaire épidermoïde. Dans l’adénocarcinome, cibler l’axe SMAD3–VEGF–TIMP-1 pourrait à la fois normaliser la vascularisation anormale et alléger l’immunosuppression locale, rendant les immunothérapies par inhibition de points de contrôle plus efficaces. Dans les tumeurs épidermoïdes, où les fibroblastes favorisent un environnement rude, pauvre en oxygène et acide plutôt qu’une forte néovascularisation, des thérapies qui soulagent l’hypoxie, neutralisent l’acidité ou bloquent des signaux inflammatoires spécifiques pourraient être plus prometteuses que les approches anti-angiogéniques classiques. Pour les patients, ce travail souligne que le succès des traitements ciblant la vascularisation et l’immunité dépend non seulement des cellules cancéreuses, mais aussi du stroma fibreux qui orchestre discrètement l’approvisionnement sanguin de la tumeur.
Citation: Díaz-Valdivia, N., Duch, P., Ikemori, R. et al. Antagonistic SMAD2/3 control of TIMP-1, VEGF-A, and hypoxia signaling in myofibroblasts shapes histotype-specific angiogenesis in lung cancer. Cell Death Dis 17, 431 (2026). https://doi.org/10.1038/s41419-026-08677-2
Mots-clés: angiogenèse du cancer du poumon, fibroblastes associés aux tumeurs, VEGF et TIMP-1, microenvironnement tumoral, signalisation SMAD