Clear Sky Science · nl
Antagonistische SMAD2/3-regulatie van TIMP-1, VEGF-A en hypoxiesignalen in myofibroblasten bepaalt histotype-specifieke angiogenese bij longkanker
Waarom bloedvaten in longtumoren ertoe doen
Longkanker is geen eenduidige ziekte; patiënten met verschillende tumortypen reageren vaak heel verschillend op dezelfde geneesmiddelen. Deze studie stelt een eenvoudige maar cruciale vraag: waarom ontwikkelen sommige veelvoorkomende longtumoren rijke netwerken van bloedvaten terwijl andere wegkwijnen in zuurstofarme zones — en hoe helpt het omliggende littekenachtige weefsel bij het bepalen van die uitkomst? Inzicht in dit verborgen gesprek tussen kankercellen, ondersteunende cellen en bloedvaten kan leiden tot meer gerichte behandelingen en het succes van zowel chemotherapie als immunotherapie verbeteren.
Twee veelvoorkomende longkankers, twee vasculaire landschappen
De auteurs richten zich op de twee belangrijkste vormen van niet-kleincellige longkanker: adenocarcinoom, dat vaak in het buitenste deel van de long ontstaat, en plaveiselcelcarcinoom, dat vaker dicht bij de centrale luchtwegen voorkomt. Door duizenden patiëntmonsters en beelden uit grote openbare databanken te analyseren, tonen ze aan dat adenocarcinomen over het algemeen beter van bloedvaten worden voorzien, met wijdere vatkanalen en sterkere activiteit van genen die met vaatgroei samenhangen. Daarentegen vertonen plaveiselceltumoren vaker tekenen van slechte bloedtoevoer, waaronder uitgebreide necrose en hoge niveaus van hypoxiemarkers die zuurstofgebrek signaleren. Dit onderscheid in vasculair gedrag blijft bestaan, zelfs na correctie voor klinische variabelen zoals leeftijd, tumoorstadium en rookgeschiedenis. 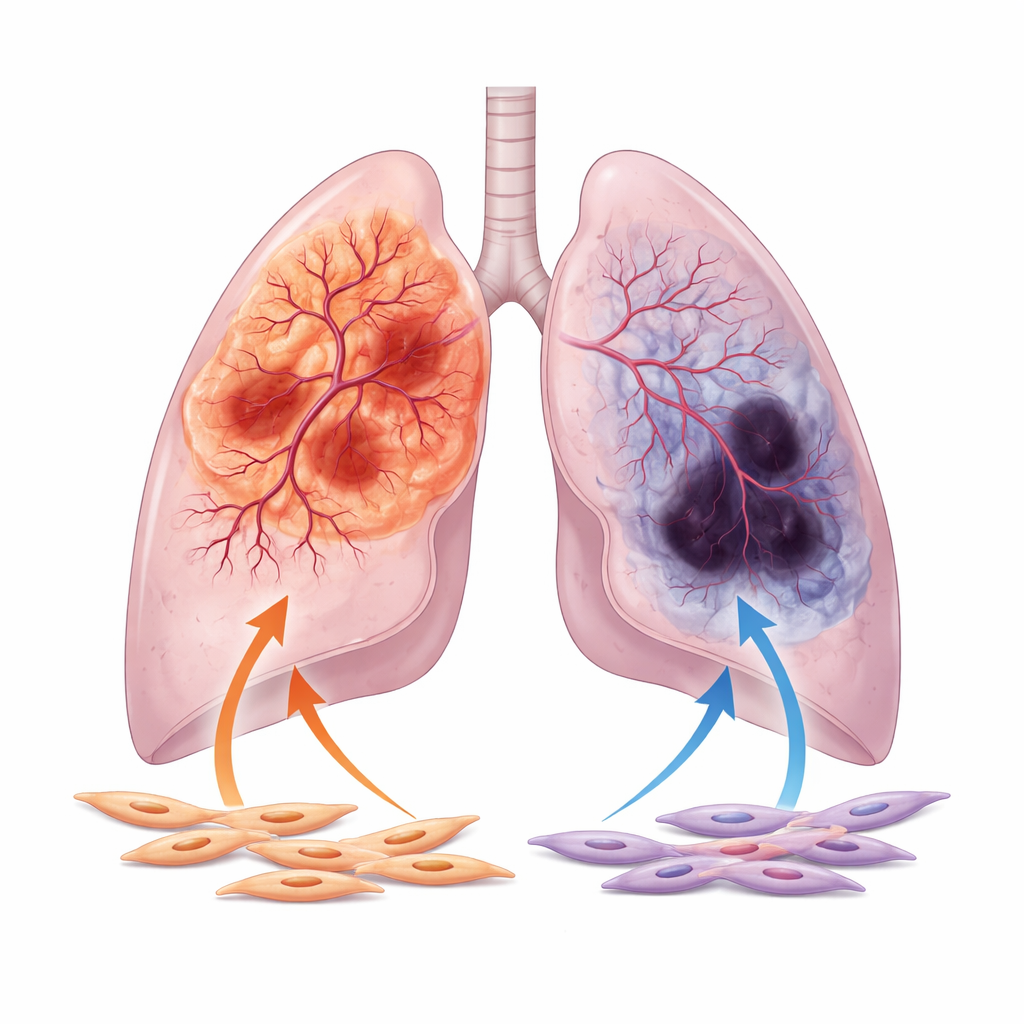
De stille kracht van tumorfibroblasten
De aandacht verschuift vervolgens naar tumor-geassocieerde fibroblasten, de contractiele cellen met myofibroblast-achtige eigenschappen die longtumoren omringen en infiltreren. Deze cellen, beter bekend om hun rol in littekenvorming, scheiden ook veel stoffen uit die vaatgroei ofwel kunnen bevorderen of remmen. Met single-cell RNA-sequencing vinden de onderzoekers dat fibroblasten in adenocarcinomen intensiever communiceren met nabijgelegen endotheelcellen, de bouwstenen van bloedvaten, dan fibroblasten in plaveiselceltumoren. In laboratoriumschotels zorgt vloeistof verzameld van adenocarcinoom-fibroblasten ervoor dat endotheelcellen migreren en dichte, verstrengelde capillaire-achtige netwerken vormen, terwijl vocht van plaveiselcelfibroblasten veel zwakkere en schaarser vertakte structuren opwekt.
Belangrijke boodschappers: VEGF, TIMP-1 en een moleculaire schakelaar
Om te achterhalen welke signalen verantwoordelijk zijn, profileert het team tientallen uitgescheiden factoren. Adenocarcinoom-fibroblasten produceren bijzonder hoge niveaus van VEGF-A, een klassieke aanjager van nieuwe vaatgroei, en TIMP-1, een eiwit dat doorgaans bekendstaat als rem op weefsel-afbrekende enzymen. Hier toont TIMP-1 een andere kant: in gecontroleerde experimenten verhoogt toevoeging van TIMP-1 de vertakkingscomplexiteit van endotheelnetwerken en creëert het de verwarde architecturen die kenmerkend zijn voor tumorbloedvaten. Het verwijderen van TIMP-1 uit adenocarcinoom-fibroblasten vermindert in cultuur scherp de vaatvertakking en reduceert de bloedvatdichtheid en tumorprogressie in muismodellen. Cruciaal is dat dit vertakkende effect afhangt van een basisniveau van VEGF-signaaltransductie, wat suggereert dat VEGF als het gaspedaal fungeert terwijl TIMP-1 fijnregelt hoe chaotisch de resulterende vasculatuur wordt.
Tegengestelde regulatie van groei versus hypoxie
Aan deze verschillen ligt een moleculaire "schakelaar" in fibroblasten ten grondslag die twee verwante eiwitten in balans houdt: SMAD2 en SMAD3, die signalen van de groeifactor TGF-β doorgeven. Adenocarcinoom-fibroblasten geven de voorkeur aan SMAD3; een hoge SMAD3/SMAD2-ratio stuurt de overproductie van VEGF-A, TIMP-1 en andere vaatbevorderende factoren aan. Wanneer de onderzoekers SMAD3 in deze cellen naar beneden halen, stort hun vermogen om endotheelmigratie, vertakking en tumorvascularisatie te stimuleren in. Plaveiselcel-fibroblasten, vaak gevormd door rook-geïnduceerde epigenetische veranderingen, tonen het omgekeerde patroon: SMAD3 is gesilenced en SMAD2 is verhoogd. Deze toestand versterkt hypoxie-gerelateerde genen en HIF-1α, een hoofdregelaar van lage-zuurstofreacties, maar vertaalt zich paradoxaal genoeg niet in sterke VEGF-A-productie. Als gevolg blijven deze tumoren meer hypoxisch en necrotisch, met zwakkere ondersteuning voor nieuwe vaten ondanks een krachtig intern "lage zuurstof"-alarm. 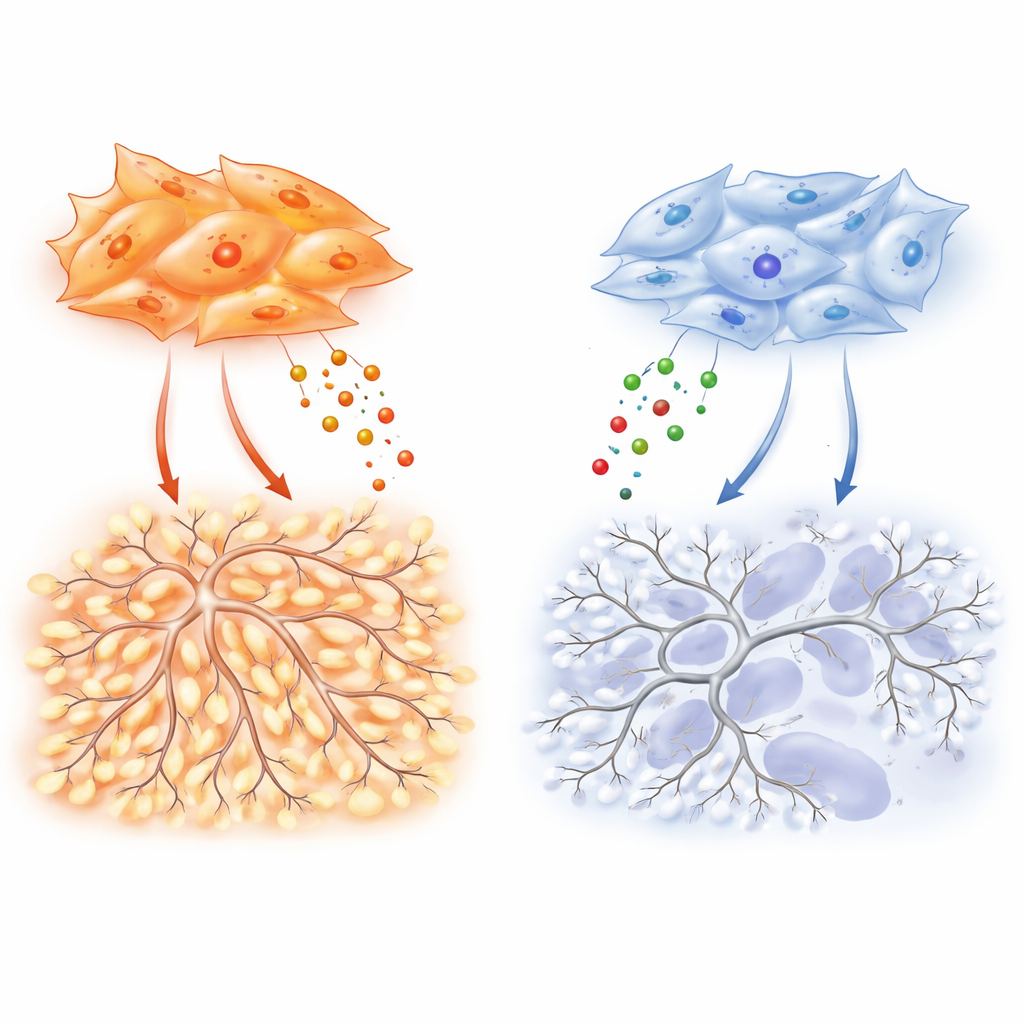
Wat dit betekent voor patiënten en toekomstige therapieën
Door het gedrag van bloedvaten te koppelen aan fibroblastprogramma’s in elk tumortype, helpt de studie verklaren waarom anti-angiogene middelen beter hebben gewerkt bij adenocarcinoom dan bij plaveiselcel-longkanker. Bij adenocarcinoom zou het richten op de SMAD3–VEGF–TIMP-1-as zowel de afwijkende vasculatuur kunnen normaliseren als de lokale immuunsuppressie verminderen, waardoor checkpoint-remmende immunotherapieën effectiever worden. Bij plaveiselceltumoren, waar fibroblasten eerder een vijandige, zuurstofarme en zure omgeving creëren dan sterke vaatgroei, kunnen therapieën die hypoxie verlichten, zuurtegraad neutraliseren of specifieke ontstekingssignalen blokkeren veelbelovender zijn dan klassieke anti-angiogene benaderingen. Voor patiënten onderstreept dit werk dat het succes van vaat- en immuungerichte behandelingen niet alleen afhangt van kankercellen, maar ook van het vezelige stroma dat stilletjes de bloedvoorziening van de tumor orkestreert.
Bronvermelding: Díaz-Valdivia, N., Duch, P., Ikemori, R. et al. Antagonistic SMAD2/3 control of TIMP-1, VEGF-A, and hypoxia signaling in myofibroblasts shapes histotype-specific angiogenesis in lung cancer. Cell Death Dis 17, 431 (2026). https://doi.org/10.1038/s41419-026-08677-2
Trefwoorden: angiogenese bij longkanker, tumor-geassocieerde fibroblasten, VEGF en TIMP-1, tumormicro-omgeving, SMAD-signaaltransductie