Clear Sky Science · pl
Antagonistyczna kontrola przez SMAD2/3 nad TIMP-1, VEGF-A i sygnalizacją niedotlenienia w miofibroblastach kształtuje histotypowo specyficzną angiogenezę w raku płuca
Dlaczego naczynia krwionośne w guzach płuca mają znaczenie
Rak płuca to nie jedna choroba — pacjenci z różnymi typami nowotworu często reagują zupełnie odmiennie na te same leki. W tym badaniu postawiono proste, ale kluczowe pytanie: dlaczego niektóre powszechne nowotwory płuca rozwijają bogate sieci naczyń krwionośnych, podczas gdy inne duszą się w strefach o niskiej zawartości tlenu — i jak otaczająca tkanka bliznowata współdecyduje o wyniku? Zrozumienie tej ukrytej rozmowy między komórkami nowotworowymi, komórkami wspierającymi i naczyniami może ukierunkować bardziej precyzyjne leczenie i poprawić skuteczność zarówno chemioterapii, jak i immunoterapii.
Dwa powszechne nowotwory płuca, dwa krajobrazy naczyniowe
Autorzy skupiają się na dwóch głównych postaciach niedrobnokomórkowego raka płuca: gruczolakoraku, który często powstaje w obwodowych partiach płuca, oraz raka płaskonabłonkowego, mającego tendencję do formowania się bliżej centralnych dróg oddechowych. Analizując tysiące próbek pacjentów i obrazów z dużych publicznych baz danych, wykazują, że gruczolakoraki są zazwyczaj lepiej ukrwione, z szerszymi kanałami naczyniowymi i silniejszą aktywnością genów związanych z tworzeniem naczyń. Natomiast guzy płaskonabłonkowe częściej wykazują oznaki niedostatecznego ukrwienia, w tym rozległe obszary martwicy i wysokie poziomy markerów niedotlenienia, sygnalizujących brak tlenu. Ten podział w zachowaniu naczyniowym utrzymuje się nawet po uwzględnieniu zmiennych klinicznych, takich jak wiek, stadium choroby i historia palenia. 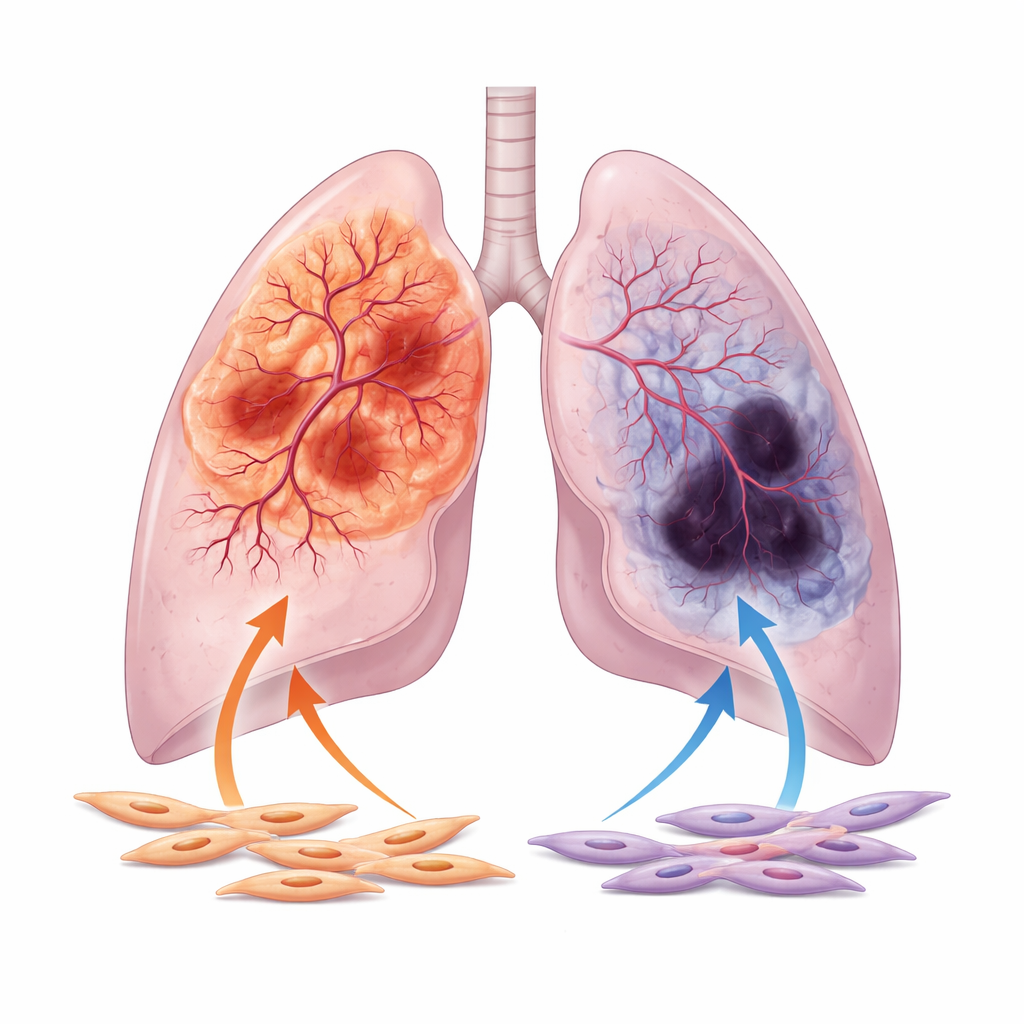
Cicha siła fibroblastów nowotworowych
Uwagę zwrócono następnie na fibroblasty związane z guzem — komórki kontraktilne przypominające miofibroblasty, które otaczają i infiltrują guzy płuca. Komórki te, znane głównie z wytwarzania tkanki bliznowatej, wydzielają również wiele substancji, które mogą pobudzać lub hamować rozwój naczyń. Dzięki analizie pojedynczych komórek metodą RNA-seq badacze odkryli, że fibroblasty w gruczolakoraku intensywniej oddziałują z pobliskimi komórkami śródbłonka, budulcem naczyń, niż fibroblasty w nowotworach płaskonabłonkowych. W hodowlach laboratoryjnych płyn pozyskany od fibroblastów z gruczolakoraka powoduje migrację komórek śródbłonka i tworzenie gęstych, splecionych sieci przypominających kapilary, podczas gdy płyn od fibroblastów płaskonabłonkowych wywołuje znacznie słabsze i rzadsze struktury.
Kluczowe przekaźniki: VEGF, TIMP-1 i molekularny przełącznik
Aby ustalić, które sygnały są odpowiedzialne, zespół przeanalizował dziesiątki czynników wydzielanych przez komórki. Fibroblasty z gruczolakoraka wytwarzają szczególnie wysokie poziomy VEGF-A, klasycznego promotora powstawania naczyń, oraz TIMP-1, białka znanego raczej jako hamulec dla enzymów rozkładających tkanki. W tym kontekście TIMP-1 ukazuje inną twarz: w kontrolowanych eksperymentach dodanie TIMP-1 zwiększa złożoność rozgałęzień sieci śródbłonka, tworząc poplątane architektury typowe dla naczyń nowotworowych. Usunięcie TIMP-1 z fibroblastów gruczolakoraka gwałtownie zmniejsza rozgałęzienia naczyń w hodowlach i obniża gęstość naczyń oraz wzrost guza u myszy. Kluczowe jest to, że efekt rozgałęzień zależy od podstawowego poziomu sygnalizacji VEGF, co sugeruje, że VEGF działa jak pedał gazu, podczas gdy TIMP-1 dopracowuje, jak chaotyczna staje się powstała sieć naczyń.
Przeciwstawne regulacje wzrostu i niedotlenienia
U podstaw tych różnic leży molekularny „przełącznik” wewnątrz fibroblastów, równoważący dwie spokrewnione białka, SMAD2 i SMAD3, które przekazują sygnały od czynnika wzrostu TGF-β. Fibroblasty z gruczolakoraka preferują SMAD3, a wysoki stosunek SMAD3 do SMAD2 napędza nadprodukcję VEGF-A, TIMP-1 i innych czynników sprzyjających naczyniom. Gdy badacze obniżyli poziom SMAD3 w tych komórkach, ich zdolność do stymulowania migracji śródbłonka, rozgałęzień i unaczynienia guza zawaliła się. Fibroblasty z raka płaskonabłonkowego, często ukształtowane przez epigenetyczne zmiany związane z paleniem, wykazują odwrotny wzorzec: SMAD3 jest wyciszony, a SMAD2 podwyższony. Ten stan wzmacnia geny związane z niedotlenieniem i HIF-1α, głównego regulatora odpowiedzi na niski poziom tlenu, ale paradoksalnie nie przekłada się na silne wydzielanie VEGF-A. W rezultacie te guzy pozostają bardziej niedotlenione i martwicze, z słabszym wsparciem dla tworzenia nowych naczyń pomimo silnego wewnętrznego „alarmu” niskiego tlenu. 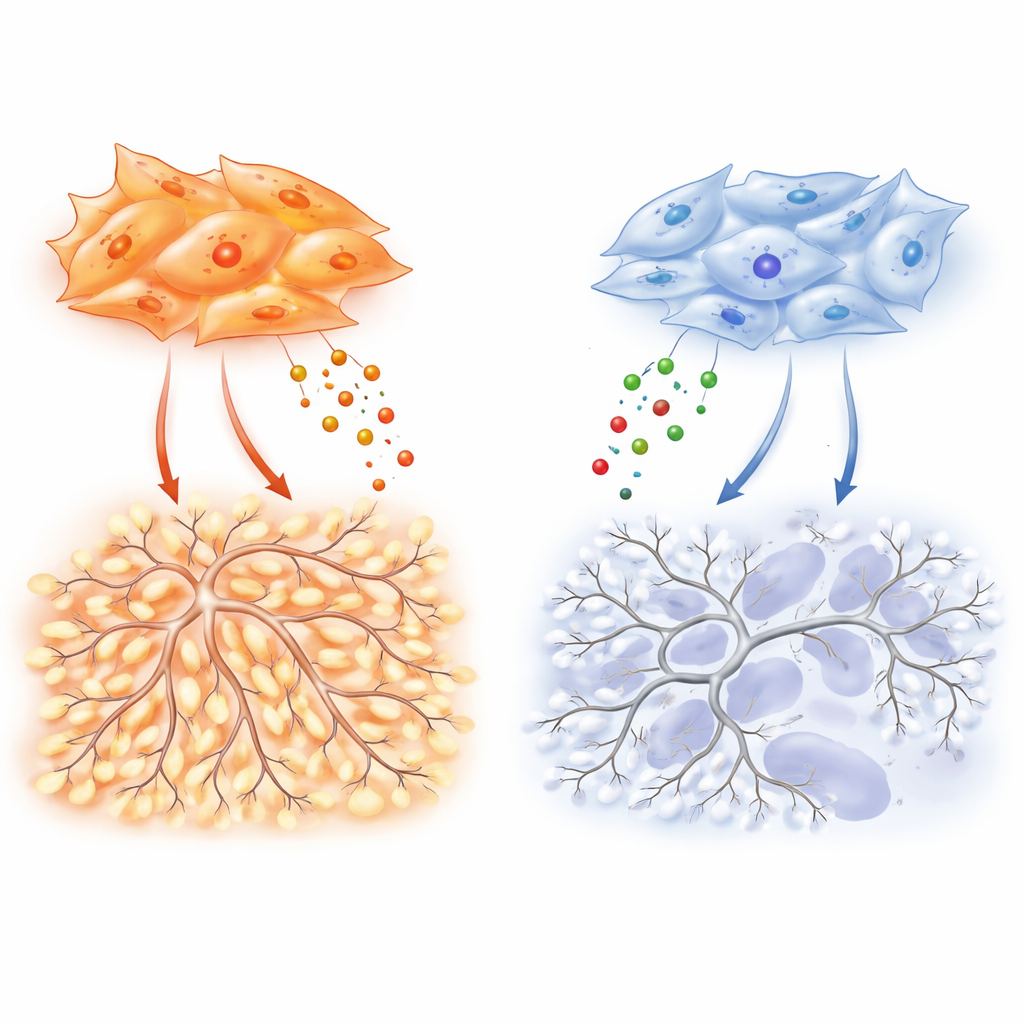
Co to oznacza dla pacjentów i przyszłych terapii
Łącząc zachowanie naczyń z programami fibroblastów w każdej odmianie guza, badanie pomaga wyjaśnić, dlaczego leki antyangiogenne działały lepiej w gruczolakoraku niż w raku płaskonabłonkowym płuca. W gruczolakoraku ukierunkowanie osi SMAD3–VEGF–TIMP-1 mogłoby zarówno znormalizować nieprawidłowe unaczynienie, jak i złagodzić lokalne tłumienie odpowiedzi immunologicznej, zwiększając skuteczność terapii z blokadą punktów kontrolnych. W guzach płaskonabłonkowych, gdzie fibroblasty kreują surowe, ubogie w tlen i kwaśne środowisko zamiast silnego wzrostu naczyń, bardziej obiecujące mogą być terapie łagodzące niedotlenienie, neutralizujące kwasowość lub blokujące konkretne sygnały zapalne niż klasyczne podejścia antyangiogenne. Dla pacjentów praca ta podkreśla, że powodzenie terapii ukierunkowanych na naczynia i układ odpornościowy zależy nie tylko od komórek nowotworowych, lecz także od włóknistego zrębu, który cicho orkiestruje zaopatrzenie guza w krew.
Cytowanie: Díaz-Valdivia, N., Duch, P., Ikemori, R. et al. Antagonistic SMAD2/3 control of TIMP-1, VEGF-A, and hypoxia signaling in myofibroblasts shapes histotype-specific angiogenesis in lung cancer. Cell Death Dis 17, 431 (2026). https://doi.org/10.1038/s41419-026-08677-2
Słowa kluczowe: angiogeneza w raku płuca, fibroblasty związane z guzem, VEGF i TIMP-1, mikrośrodowisko guza, sygnalizacja SMAD