Clear Sky Science · tr
Antagonistik SMAD2/3 kontrolünün myofibroblastlarda TIMP-1, VEGF-A ve hipoksi sinyalini düzenlemesi, akciğer kanserinde histotipe özgü anjiyogeneziyi şekillendirir
Akciğer tümörlerindeki kan damarlarının önemi
Akciğer kanseri tek bir hastalık değildir ve farklı tümör türlerine sahip hastalar aynı ilaçlara çok farklı yanıtlar verebilir. Bu çalışma basit ama kritik bir soru soruyor: neden bazı yaygın akciğer tümörleri zengin damar ağları geliştirirken diğerleri oksijen yetersizliği bölgelerinde boğuluyor ve çevresindeki yara benzeri doku bu sonucu nasıl belirliyor? Kanser hücreleri, destek hücreleri ve kan damarları arasındaki bu gizli iletişimi anlamak, daha hassas tedavilere yol gösterebilir ve hem kemoterapi hem de immünoterapinin başarısını artırabilir.
İki yaygın akciğer kanseri, iki damar manzarası
Yazarlar, küçük hücre dışı akciğer kanserinin iki ana formuna odaklanıyor: genellikle akciğerin dış kısımlarında ortaya çıkan adenokarsinom ve merkezi hava yollarına daha yakın oluşma eğiliminde olan skuamöz hücreli karsinom. Binlerce hasta örneği ve büyük kamu veri tabanlarındaki görüntüleri analiz ederek, adenokarsinomların genel olarak daha iyi damar beslemesine sahip olduğunu; daha geniş damar kanalları ve damar büyümesiyle ilişkilendirilen genlerin daha güçlü etkinliğini gösterdiklerini ortaya koyuyorlar. Buna karşılık, skuamöz tümörler daha sık kötü kanlanma işaretleri gösteriyor; yaygın ölü doku ve oksijen eksikliğini gösteren yüksek düzeyde hipoksi belirteçleri gibi. Klinik değişkenler (yaş, tümör evresi, sigara öyküsü vb.) hesaba katıldıktan sonra bile bu damar davranışı ayrımı devam ediyor. 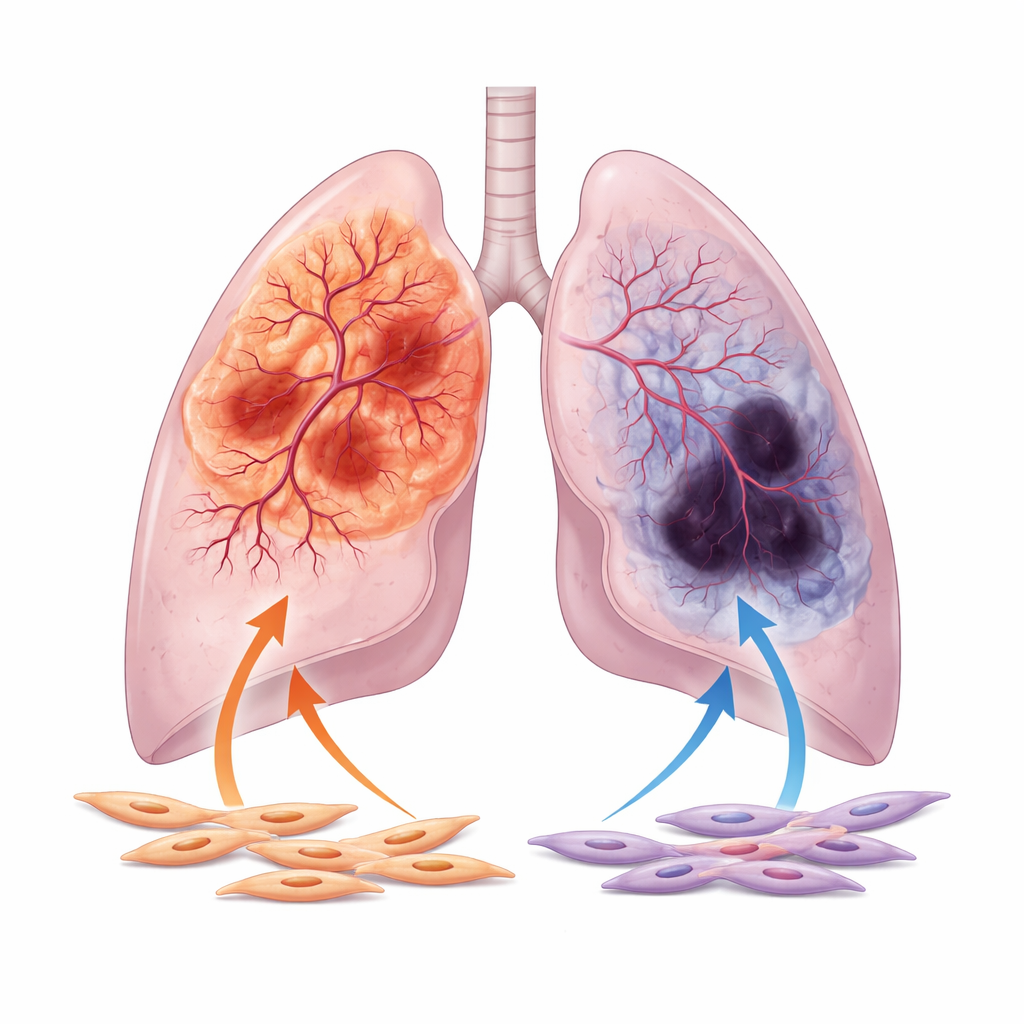
Tümör fibroblastlarının sessiz gücü
Dikkat daha sonra tümörlere eşlik eden fibroblastlara, yani çevreleyen ve tümör içine sızan kasılı, myofibroblast benzeri hücrelere çevriliyor. Genellikle yara dokusu üreten hücreler olarak bilinen bu hücreler, damar büyümesini teşvik edebilen veya sınırlayabilen birçok madde de salgılar. Tek hücre RNA dizilemesi kullanarak, araştırmacılar adenokarsinomlardaki fibroblastların, damarların yapıtaşları olan endotel hücreleriyle skuamöz tümörlerdeki fibroblastlardan daha yoğun etkileştiğini buluyorlar. Laboratuvar ortamında, adenokarsinom fibroblastlarından toplanan sıvı endotel hücrelerin göç etmesine ve yoğun, birbirine dolanmış kılcal benzeri ağlar oluşturmasına neden olurken, skuamöz fibroblast sıvısı çok daha zayıf ve seyrek yapılar tetikliyor.
Ana elçiler: VEGF, TIMP-1 ve moleküler bir düğme
Hangi sinyallerin sorumlu olduğunu keşfetmek için ekip onlarca salgılanan faktörü profilliyor. Adenokarsinom fibroblastları özellikle VEGF-A düzeylerinde yüksek üretim gösteriyor; bu, yeni damar büyümesinin klasik sürücüsüdür, ayrıca doku parçalanmasını durduran bir fren olarak bilinen TIMP-1’i de yüksek düzeyde üretiyorlar. Burada TIMP-1 farklı bir rol sergiliyor: kontrollü deneylerde TIMP-1 eklenmesi endotel ağlarının dallanma karmaşıklığını artırıyor ve tümör damarlarına özgü dolaşıklık yaratan mimarileri oluşturuyor. Adenokarsinom fibroblastlarından TIMP-1 alınması, kültürde damar dallanmasını keskin biçimde azaltıyor ve farelerde damar yoğunluğunu ve tümör büyümesini düşürüyor. Kritik olarak, bu dallanma etkisi VEGF sinyalinin bir temel düzeyine bağlı; bu da VEGF’in gaz pedalı, TIMP-1’in ise ortaya çıkan vaskülatürün ne kadar kaotik olacağını ince ayarlayan eleman olduğunu düşündürüyor.
Büyüme ile hipoksinin karşıt kontrolü
Bu farklılıkların altında fibroblastlar içinde, büyüme faktörü TGF-β’den sinyalleri ileten SMAD2 ve SMAD3 adlı iki ilgili proteini dengeleyen moleküler bir "düğme" yatıyor. Adenokarsinom fibroblastları SMAD3’ü tercih ediyor ve bu yüksek SMAD3/SMAD2 oranı VEGF-A, TIMP-1 ve diğer damar destekleyici faktörlerin aşırı üretimini sürüklüyor. Araştırmacılar bu hücrelerde SMAD3’ü azaltınca, endotel göçü, dallanma ve tümör vaskülarizasyonunu uyarmadaki yetenekleri çöktü. Sigara kaynaklı epigenetik değişikliklerle şekillenen skuamöz fibroblastlar ise ters paterni gösteriyor: SMAD3 susturulmuş ve SMAD2 artmış durumda. Bu durum hipoksi ile ilişkili genleri ve düşük oksijen tepkilerinin ana düzenleyicisi HIF-1α’yı yükseltiyor, ancak paradoksal olarak güçlü bir VEGF-A çıktısına dönüşmüyor. Sonuç olarak, bu tümörler daha hipoksik ve nekrotik kalıyor; güçlü içsel bir "düşük oksijen" alarmına rağmen yeni damarlar için zayıf destek sağlanıyor. 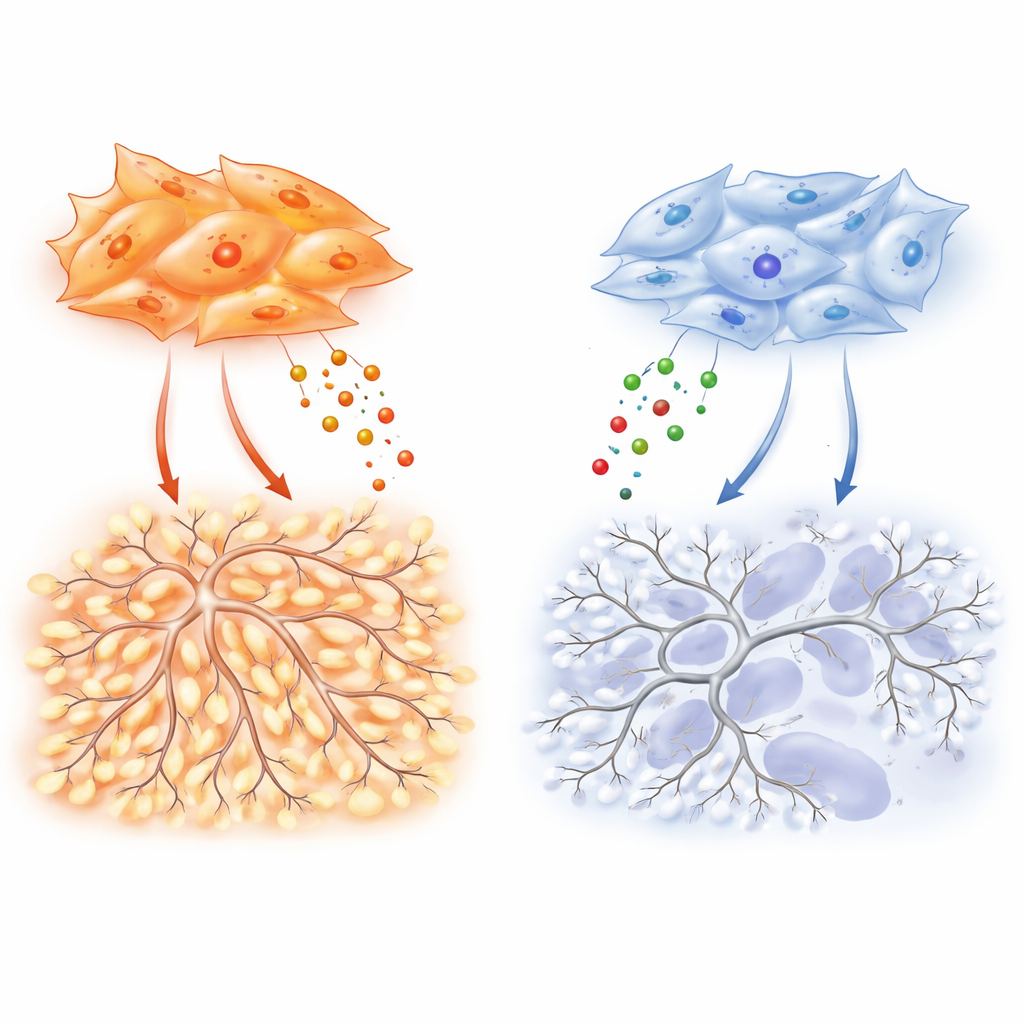
Hastalar ve gelecekteki tedaviler için anlamı
Kan damarlarının davranışını her tümör tipindeki fibroblast programlarına bağlayarak, çalışma neden anti-anjiyogenik ilaçların adenokarsinomda skuamöz akciğer kanserine kıyasla daha iyi çalıştığını açıklamaya yardımcı oluyor. Adenokarsinomda SMAD3–VEGF–TIMP-1 eksenini hedeflemek, anormal vaskülatürü normalize edebilir ve yerel immün baskıyı hafifleterek kontrol noktası engelleyen immünoterapilerin etkinliğini artırabilir. Skuamöz tümörlerde ise fibroblastların güçlü damar büyümesi yerine sert, oksijen fakiri ve asidik bir çevre oluşturması nedeniyle, hipoksiyi hafifleten, asiditeyi nötralize eden veya belirli inflamatuar sinyalleri bloke eden tedaviler klasik anti-anjiyogenik yaklaşımlardan daha umut verici olabilir. Hastalar için bu çalışma; vasküler ve immün hedefli tedavilerin başarısının yalnızca kanser hücrelerine değil, tümörün kan tedarikini sessizce düzenleyen lifli stroma’ ya da bağlı olduğunu vurguluyor.
Atıf: Díaz-Valdivia, N., Duch, P., Ikemori, R. et al. Antagonistic SMAD2/3 control of TIMP-1, VEGF-A, and hypoxia signaling in myofibroblasts shapes histotype-specific angiogenesis in lung cancer. Cell Death Dis 17, 431 (2026). https://doi.org/10.1038/s41419-026-08677-2
Anahtar kelimeler: akciğer kanseri anjiyogenezi, tümöre eşlik eden fibroblastlar, VEGF ve TIMP-1, tümör mikroçevresi, SMAD sinyal iletimi