Clear Sky Science · de
Antagonistische SMAD2/3-Steuerung von TIMP-1, VEGF-A und Hypoxie-Signalen in Myofibroblasten formt histotyp-spezifische Angiogenese beim Lungenkrebs
Warum Blutgefäße in Lungentumoren wichtig sind
Lungenkrebs ist keine einheitliche Krankheit, und Patientinnen und Patienten mit unterschiedlichen Tumortypen sprechen oft sehr unterschiedlich auf dieselben Therapien an. Diese Studie stellt eine einfache, aber entscheidende Frage: Warum entwickeln einige häufige Lungentumoren dichte Netzwerke von Blutgefäßen, während andere in sauerstoffarmen Bereichen ersticken — und wie beeinflusst das umliegende narbenartige Gewebe dieses Ergebnis? Das Verständnis dieses verborgenen Dialogs zwischen Krebszellen, Stützzellen und Blutgefäßen könnte präzisere Behandlungsstrategien ermöglichen und den Erfolg von Chemotherapie und Immuntherapie verbessern.
Zwei häufige Lungenkrebsarten, zwei Gefäßlandschaften
Die Autorinnen und Autoren konzentrieren sich auf die beiden Hauptformen des nicht-kleinzelligen Lungenkarzinoms: Adenokarzinom, das häufig in den äußeren Lungenbereichen entsteht, und Plattenepithelkarzinom, das eher in der Nähe der zentralen Atemwege auftritt. Durch die Analyse tausender Patientenproben und Bilder aus großen öffentlichen Datenbanken zeigen sie, dass Adenokarzinome im Allgemeinen besser mit Blutgefäßen versorgt sind, mit breiteren Gefäßkanälen und stärkerer Aktivität von Genen, die mit Gefäßwachstum verbunden sind. Im Gegensatz dazu zeigen Plattenepithelkarzinome häufiger Anzeichen schlechter Durchblutung, einschließlich weit verbreiteter Nekrosen und hoher Spiegel von Hypoxie-Markern, die Sauerstoffmangel signalisieren. Diese Aufspaltung im Gefäßverhalten bleibt bestehen, auch nachdem klinische Variablen wie Alter, Tumorstadium und Rauchgeschichte berücksichtigt wurden. 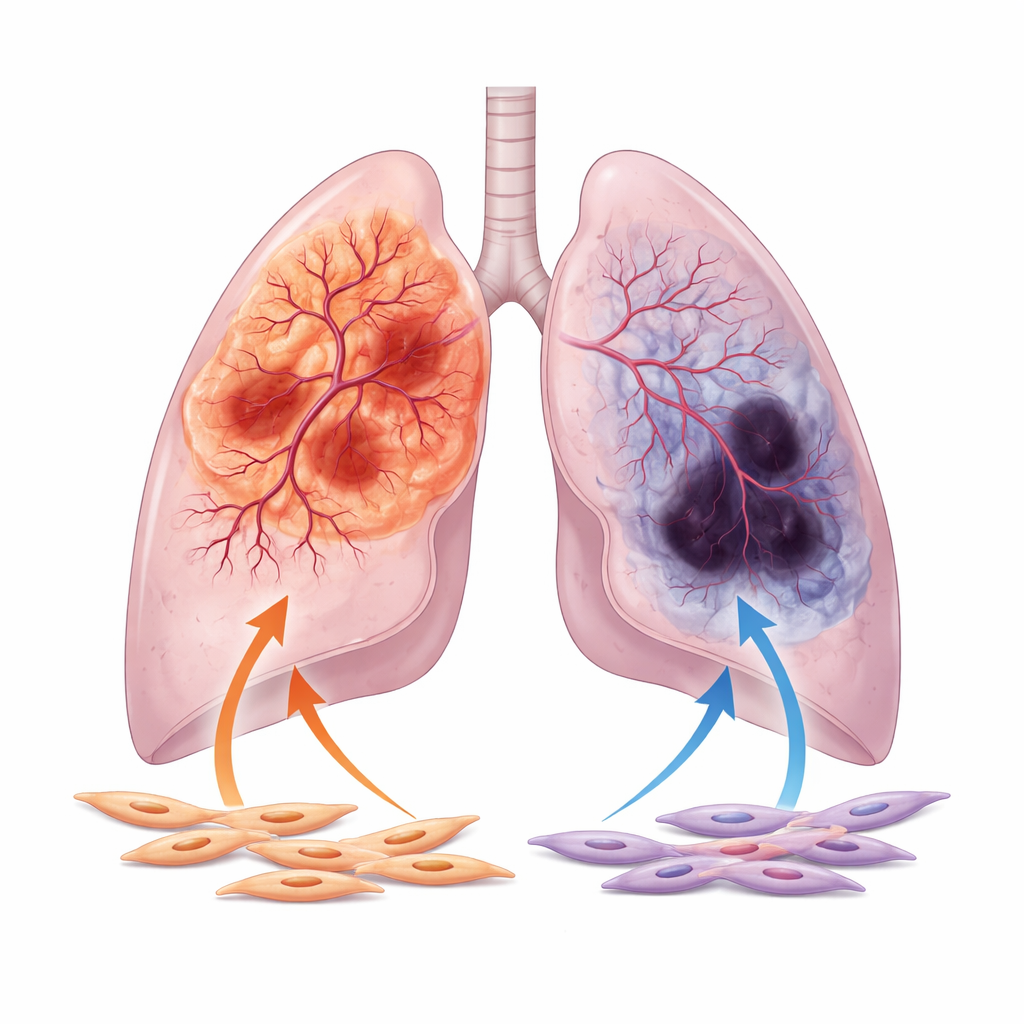
Die stille Macht der Tumorfibroblasten
Der Blick richtet sich auf tumorassoziierte Fibroblasten, die kontraktilen, myofibroblastenähnlichen Zellen, die Tumoren in der Lunge umgeben und infiltrieren. Diese Zellen, die vor allem für die Bildung von Narbengewebe bekannt sind, sezernieren auch zahlreiche Faktoren, die das Gefäßwachstum entweder fördern oder hemmen können. Mithilfe von Einzelzell-RNA-Sequenzierung finden die Forschenden heraus, dass Fibroblasten in Adenokarzinomen intensiver mit benachbarten Endothelzellen, den Bausteinen der Blutgefäße, interagieren als Fibroblasten in Plattenepithelkarzinomen. Im Reagenzglas führt Flüssigkeit, die von Adenokarzinom-Fibroblasten gesammelt wurde, dazu, dass Endothelzellen wandern und dichte, ineinander verflochtene kapillarähnliche Netzwerke bilden, während Flüssigkeit von Plattenepithel-Fibroblasten deutlich schwächere und spärlichere Strukturen hervorruft.
Wichtige Botenstoffe: VEGF, TIMP-1 und ein molekularer Schalter
Um die verantwortlichen Signale zu identifizieren, untersucht das Team Dutzende sekretierter Faktoren. Adenokarzinom-Fibroblasten produzieren besonders hohe Mengen an VEGF-A, einem klassischen Treiber der Neubildung von Gefäßen, und TIMP-1, einem Protein, das eher als Bremse für gewebeabbauende Enzyme bekannt ist. Hier zeigt TIMP-1 ein anderes Gesicht: In kontrollierten Experimenten erhöht die Zugabe von TIMP-1 die Verzweigungskomplexität von Endothel-Netzwerken und erzeugt die verwinkelten Architekturen, die für Tumorblutgefäße typisch sind. Die Entfernung von TIMP-1 aus Adenokarzinom-Fibroblasten reduziert in Kultur die Gefäßverzweigung deutlich und verringert in Mäusen die Gefäßdichte und das Tumorwachstum. Entscheidend ist, dass dieser Verzweigungseffekt von einem Grundniveau der VEGF-Signalgebung abhängt, was nahelegt, dass VEGF das Gaspedal darstellt, während TIMP-1 die chaotische Ausformung der Gefäßstruktur feinjustiert.
Gegensätzliche Steuerung von Wachstum vs. Hypoxie
Dem zugrunde liegt ein molekularer „Schalter“ in Fibroblasten, der zwei verwandte Proteine ausbalanciert: SMAD2 und SMAD3, die Signale des Wachstumsfaktors TGF-β weiterleiten. Adenokarzinom-Fibroblasten bevorzugen SMAD3, und dieses hohe Verhältnis von SMAD3 zu SMAD2 treibt die Überproduktion von VEGF-A, TIMP-1 und anderen gefäßfördernden Faktoren an. Wenn die Forschenden SMAD3 in diesen Zellen herunterregulieren, bricht ihre Fähigkeit, Endothelwanderung, Verzweigung und Tumorvascularisierung zu stimulieren, zusammen. Plattenepithel-Fibroblasten, häufig geprägt von rauchinduzierten epigenetischen Veränderungen, zeigen das umgekehrte Muster: SMAD3 ist stillgelegt und SMAD2 erhöht. Dieser Zustand fördert Hypoxie-assoziierte Gene und HIF-1α, einen zentralen Regulator der Reaktion auf Sauerstoffmangel, führt aber paradoxerweise nicht zu einer starken VEGF-A-Produktion. Infolgedessen bleiben diese Tumoren hypoxischer und nekrotischer, mit schwächerer Unterstützung für neue Gefäße trotz eines starken inneren „Niedriger-Sauerstoff“-Alarms. 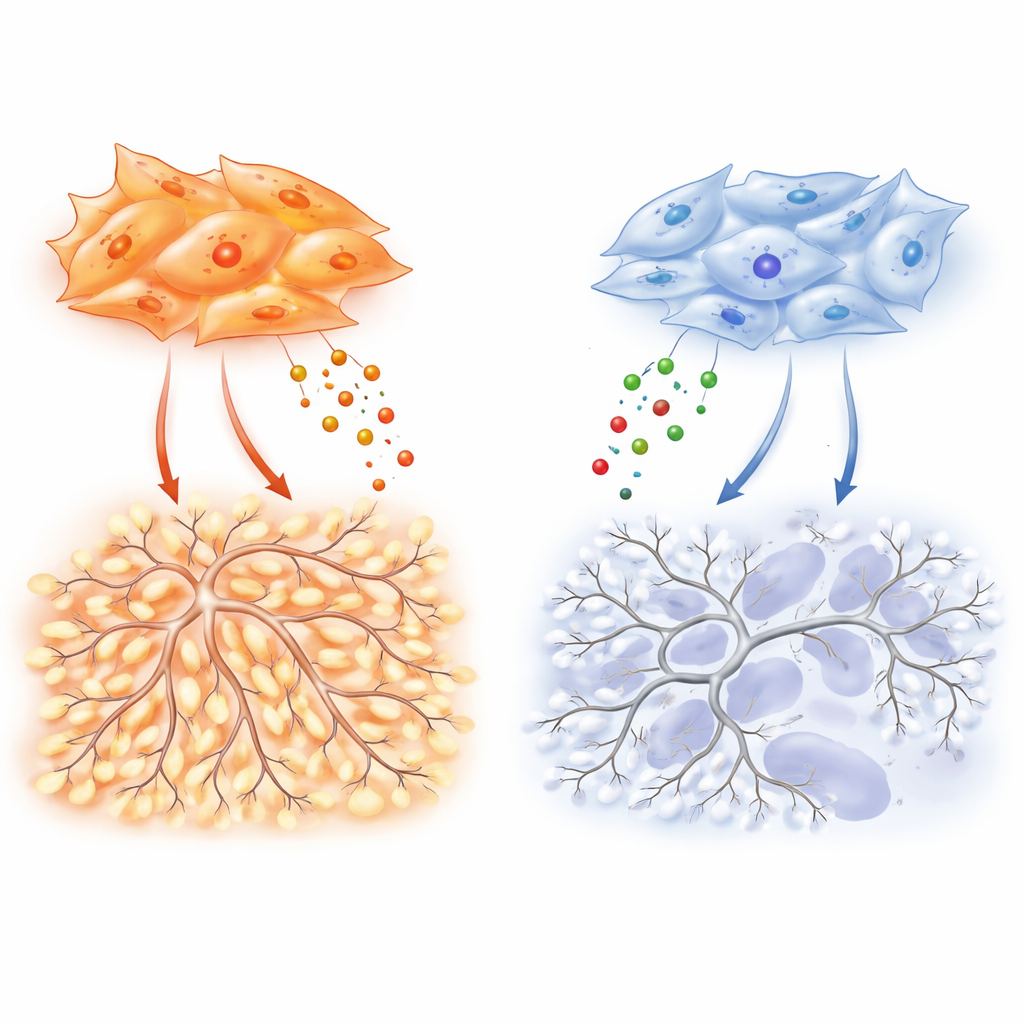
Was das für Patientinnen und Patienten und zukünftige Therapien bedeutet
Indem die Studie das Verhalten von Blutgefäßen mit Fibroblastenprogrammen in den einzelnen Tumortypen verknüpft, trägt sie dazu bei zu erklären, warum anti-angiogene Medikamente bei Adenokarzinomen besser gewirkt haben als beim Plattenepithelkarzinom der Lunge. Beim Adenokarzinom könnte das gezielte Eingreifen in die SMAD3–VEGF–TIMP-1-Achse sowohl die abnorme Gefäßstruktur normalisieren als auch die lokale Immunsuppression lindern und so die Wirksamkeit von Checkpoint-Blocker-Immuntherapien verbessern. Bei Plattenepithel-Tumoren, in denen Fibroblasten eine harsche, sauerstoffarme und saure Umgebung fördern statt ausgeprägten Gefäßwuchs, könnten Therapien, die Hypoxie lindern, Säure neutralisieren oder spezifische entzündliche Signale blockieren, vielversprechender sein als klassische anti-angiogene Ansätze. Für Patientinnen und Patienten unterstreicht diese Arbeit, dass der Erfolg vaskulärer und immun‑gerichteter Behandlungen nicht nur von Krebszellen abhängt, sondern auch vom fibrösen Stroma, das still die Blutversorgung des Tumors orchestriert.
Zitation: Díaz-Valdivia, N., Duch, P., Ikemori, R. et al. Antagonistic SMAD2/3 control of TIMP-1, VEGF-A, and hypoxia signaling in myofibroblasts shapes histotype-specific angiogenesis in lung cancer. Cell Death Dis 17, 431 (2026). https://doi.org/10.1038/s41419-026-08677-2
Schlüsselwörter: Angiogenese bei Lungenkrebs, tumorassoziierte Fibroblasten, VEGF und TIMP-1, tumormikroumgebung, SMAD-Signalgebung