Clear Sky Science · ru
Антагонистический контроль SMAD2/3 над TIMP-1, VEGF-A и гипоксическим сигналингом в миофибробластах формирует гистотип‑специфическую ангиогенезу при раке легкого
Почему кровеносные сосуды в опухолях легкого важны
Рак легкого — не одно единственное заболевание, и пациенты с разными типами опухолей часто по‑разному реагируют на одни и те же препараты. В этом исследовании поставлен простой, но ключевой вопрос: почему одни распространенные легочные опухоли развивают разветвленные сети сосудов, тогда как другие испытывают кислородный голод и гибнут в зонах с низким содержанием кислорода — и как окружающая рубцеобразная ткань влияет на этот выбор? Понимание «скрытого разговора» между раковыми клетками, поддерживающими клетками и сосудами может помочь точнее подобрать лечение и повысить эффективность как химио-, так и иммунотерапии.
Два распространенных рака легкого — два сосудистых ландшафта
Авторы сосредоточились на двух основных формах немелкоклеточного рака легкого: аденокарциноме, которая чаще развивается в периферической части легкого, и плоскоклеточном раке, склонном образовываться ближе к центральным дыхательным путям. Проанализировав тысячи образцов пациентов и изображения из крупных общедоступных баз данных, они показали, что аденокарциномы, как правило, лучше снабжены кровью: у них более широкие просветы сосудов и более выражена активность генов, связанных с ростом сосудов. Напротив, плоскоклеточные опухоли чаще демонстрируют признаки плохого кровоснабжения, включая обширные очаги некроза и высокие уровни маркеров гипоксии, указывающих на недостаток кислорода. Это расхождение в сосудистом поведении сохраняется даже после учета клинических переменных, таких как возраст, стадия опухоли и курение. 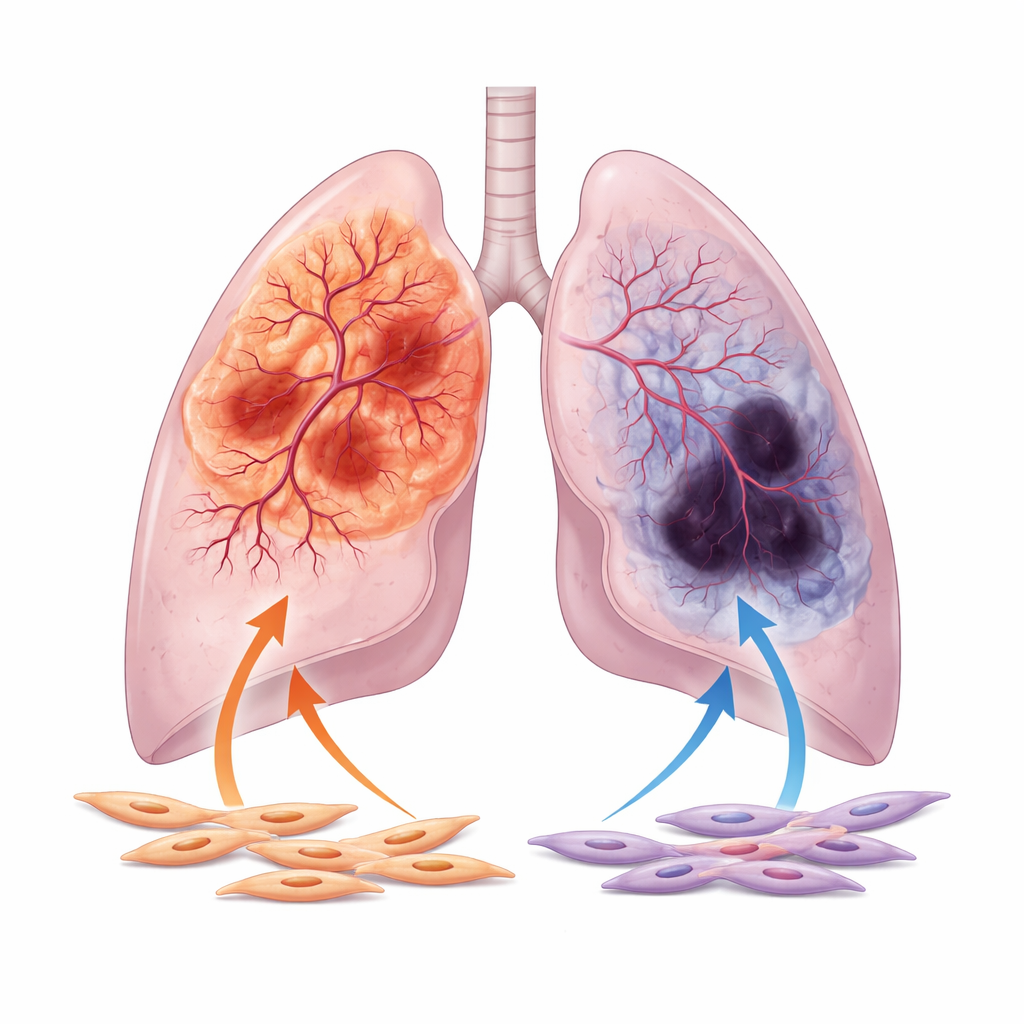
Тихая сила опухолевых фибробластов
Далее внимание переключается на фибробласты, ассоциированные с опухолью — сократительные клетки, напоминающие миофибробласты, которые окружают и проникают в легочные опухоли. Эти клетки, более известные как производители рубцовой ткани, также секретируют множество веществ, которые могут либо поощрять, либо сдерживать рост сосудов. С помощью одно‑клеточного РНК‑секвенирования исследователи обнаружили, что фибробласты в аденокарциномах интенсивнее взаимодействуют с соседними эндотелиальными клетками — строительными блоками сосудов — чем фибробласты в плоскоклеточных опухолях. В пробирках среда, собранная от фибробластов аденокарциномы, заставляет эндотелиальные клетки мигрировать и формировать плотные, переплетенные капилляроподобные сети, тогда как среда от плоскоклеточных фибробластов вызывает гораздо более слабые и редкие структуры.
Ключевые мессенджеры: VEGF, TIMP‑1 и молекулярный переключатель
Чтобы выяснить, какие сигналы отвечают за это, команда профилировала десятки секретируемых факторов. Фибробласты аденокарциномы продуцируют особенно высокие уровни VEGF‑A, классического стимулирующего фактора неоваскуляризации, и TIMP‑1 — белка, известного как «тормоз» для ферментов, разрушающих ткань. Здесь TIMP‑1 проявляет другой эффект: в контролируемых экспериментах добавление TIMP‑1 повышает разветвленность эндотелиальных сетей, создавая запутанную архитектуру, типичную для опухолевых сосудов. Удаление TIMP‑1 из фибробластов аденокарциномы резко снижало ветвление сосудов в культуре и уменьшало плотность сосудов и рост опухолей у мышей. Важно, что этот эффект ветвления зависит от базового уровня VEGF‑сигналинга, что указывает на то, что VEGF действует как педаль газа, а TIMP‑1 тонко настраивает, насколько хаотичной станет сеть сосудов.
Противоположные регуляторы роста и гипоксии
Основой этих различий является молекулярный «переключатель» внутри фибробластов, балансирующий две родственные белковые формы — SMAD2 и SMAD3, которые передают сигналы от фактора роста TGF‑β. Фибробласты аденокарциномы склоняются в сторону SMAD3, и высокое соотношение SMAD3 к SMAD2 стимулирует перепроизводство VEGF‑A, TIMP‑1 и других факторов, способствующих сосудам. Когда исследователи понижали уровень SMAD3 в этих клетках, их способность стимулировать миграцию эндотелия, ветвление и васкуляризацию опухоли резко падала. Фибробласты плоскоклеточных опухолей, часто перестроенные эпигенетическими изменениями, вызванными курением, демонстрируют обратный профиль: SMAD3 выключен, а SMAD2 повышен. Такое состояние усиливает экспрессию генов, связанных с гипоксией, и HIF‑1α — мастер‑регулятор низкооксигенных ответов, — но парадоксально не приводит к высокому уровню VEGF‑A. В результате эти опухоли остаются более гипоксическими и некротическими, при слабой поддержке неоваскуляризации, несмотря на сильный внутренний «сигнал о нехватке кислорода». 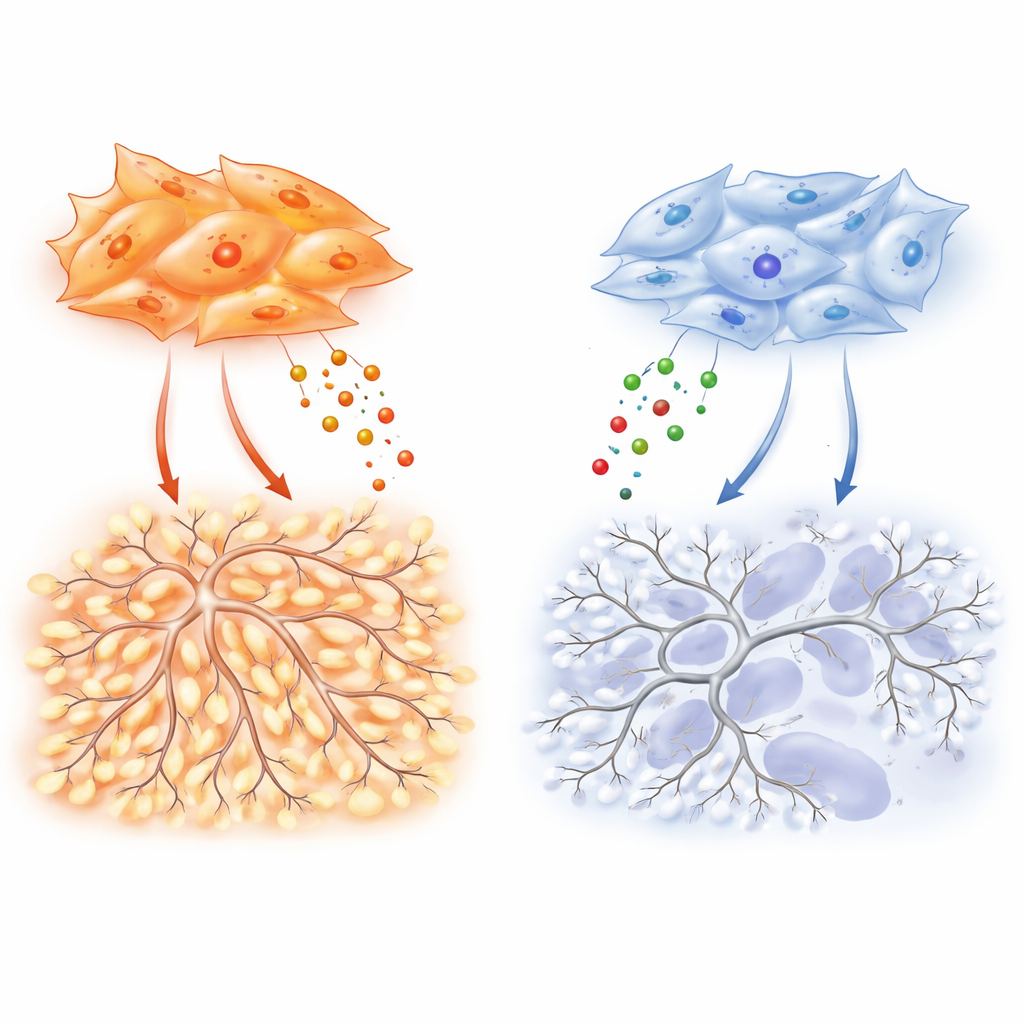
Что это значит для пациентов и будущих терапий
Связав поведение сосудов с программами фибробластов в каждом типе опухоли, исследование помогает объяснить, почему антиангиогенные препараты оказались более эффективными при аденокарциноме, чем при плоскоклеточном раке легкого. При аденокарциноме нацеленность на ось SMAD3–VEGF–TIMP‑1 может нормализовать аномальную васкулятуру и ослабить местную иммунную супрессию, делая ингибиторы контрольных точек иммунной терапии более эффективными. В плоскоклеточных опухолях, где фибробласты формируют жесткую, бедную по кислороду и кислую среду, а не стимулируют мощный сосудистый рост, более перспективными могут быть подходы, снижающие гипоксию, нейтрализующие кислотность или блокирующие специфические воспалительные сигналы, а не классическая антиангиогенная терапия. Для пациентов эта работа подчеркивает, что успех сосудисто‑ и иммунно‑таргетных лечений зависит не только от раковых клеток, но и от фиброзного стромального компонента, который тихо оркестрирует кровоснабжение опухоли.
Цитирование: Díaz-Valdivia, N., Duch, P., Ikemori, R. et al. Antagonistic SMAD2/3 control of TIMP-1, VEGF-A, and hypoxia signaling in myofibroblasts shapes histotype-specific angiogenesis in lung cancer. Cell Death Dis 17, 431 (2026). https://doi.org/10.1038/s41419-026-08677-2
Ключевые слова: ангиогенез при раке легкого, фибробласты, ассоциированные с опухолью, VEGF и TIMP‑1, опухолевая микросреда, SMAD‑сигналинг