Clear Sky Science · pt
Controle antagônico de SMAD2/3 sobre TIMP-1, VEGF-A e sinalização de hipóxia em miofibroblastos molda a angiogênese histotipo‑específica no câncer de pulmão
Por que os vasos sanguíneos em tumores pulmonares importam
O câncer de pulmão não é uma única doença, e pacientes com diferentes tipos tumorais frequentemente respondem de maneiras muito distintas aos mesmos medicamentos. Este estudo faz uma pergunta simples, mas crucial: por que alguns tumores pulmonares comuns desenvolvem redes ricas de vasos sanguíneos enquanto outros sufocam em bolsões de baixo oxigênio — e como o tecido cicatricial ao redor ajuda a decidir esse desfecho? Entender essa conversa oculta entre células cancerosas, células de suporte e vasos sanguíneos pode orientar tratamentos mais precisos e melhorar o sucesso tanto da quimioterapia quanto da imunoterapia.
Dois cânceres pulmonares comuns, duas paisagens vasculares
Os autores concentram-se nas duas formas principais de câncer de pulmão não pequenas células: adenocarcinoma, que frequentemente surge nas regiões periféricas do pulmão, e carcinoma de células escamosas, que tende a se formar mais próximo das vias aéreas centrais. Ao analisar milhares de amostras de pacientes e imagens de grandes bancos de dados públicos, mostram que adenocarcinomas são geralmente melhor supridos por vasos sanguíneos, com canais vasculares mais amplos e maior atividade de genes ligados ao crescimento vascular. Em contraste, tumores escamosos apresentam com mais frequência sinais de pobre suprimento sanguíneo, incluindo extensa necrose e altos níveis de marcadores de hipóxia, que indicam falta de oxigênio. Essa divisão no comportamento vascular persiste mesmo após ajustar por variáveis clínicas como idade, estágio tumoral e histórico de tabagismo. 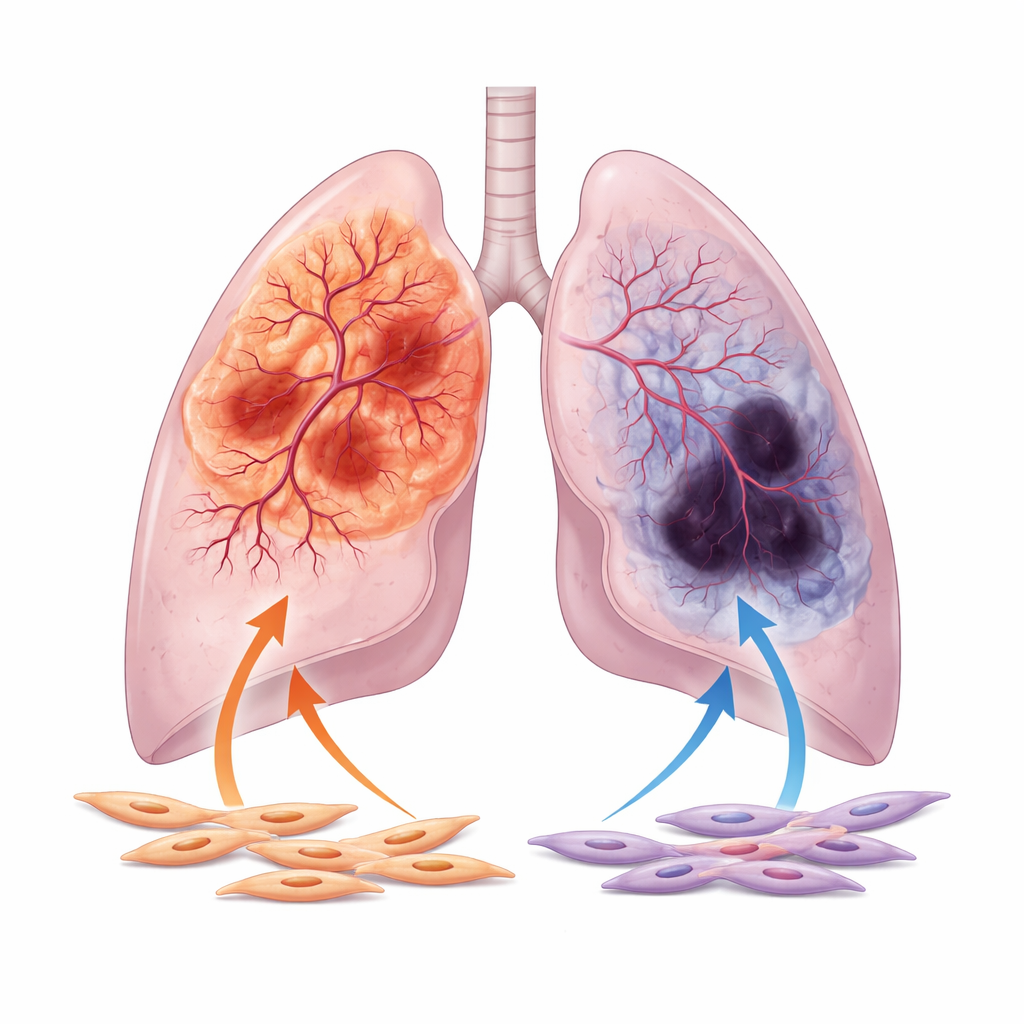
O poder silencioso dos fibroblastos tumorais
O foco volta-se então para os fibroblastos associados ao tumor, células contráteis semelhantes a miofibroblastos que circundam e infiltram os tumores pulmonares. Essas células, mais conhecidas por produzirem tecido cicatricial, também secretam muitas substâncias que podem tanto incentivar quanto restringir o crescimento de vasos. Usando sequenciamento de RNA de célula única, os pesquisadores constataram que os fibroblastos em adenocarcinoma interagem com mais intensidade com células endoteliais próximas, os blocos de construção dos vasos sanguíneos, do que os fibroblastos em tumores escamosos. Em placas de cultura, o fluido coletado de fibroblastos de adenocarcinoma faz com que células endoteliais migrem e formem redes capilares densas e entrelaçadas, enquanto o fluido de fibroblastos escamosos desencadeia estruturas muito mais fracas e esparsas.
Mensageiros-chave: VEGF, TIMP-1 e um interruptor molecular
Para descobrir quais sinais são responsáveis, a equipe perfilou dezenas de fatores secretados. Fibroblastos de adenocarcinoma produzem níveis particularmente altos de VEGF-A, um motor clássico da formação de novos vasos, e de TIMP-1, uma proteína mais conhecida por inibir enzimas que degradam o tecido. Aqui, o TIMP-1 mostra outro lado: em experimentos controlados, a adição de TIMP-1 aumenta a complexidade de ramificação das redes endoteliais, criando as arquiteturas emaranhadas típicas dos vasos tumorais. Remover o TIMP-1 de fibroblastos de adenocarcinoma reduz fortemente a ramificação vascular em cultura e diminui a densidade de vasos sanguíneos e o crescimento tumoral em camundongos. Crucialmente, esse efeito de ramificação depende de um nível basal de sinalização por VEGF, sugerindo que o VEGF atua como pedal de aceleração enquanto o TIMP-1 ajusta quão caótica a vasculatura resultante se torna.
Controles opostos de crescimento versus hipóxia
Por trás dessas diferenças está um “interruptor” molecular dentro dos fibroblastos que equilibra duas proteínas relacionadas, SMAD2 e SMAD3, que transmitem sinais do fator de crescimento TGF‑β. Fibroblastos de adenocarcinoma favorecem SMAD3, e essa alta razão SMAD3/SMAD2 impulsiona a superprodução de VEGF-A, TIMP-1 e outros fatores pró‑vasculares. Quando os pesquisadores reduzem SMAD3 nessas células, a capacidade delas de estimular migração endotelial, ramificação e vascularização tumoral colapsa. Fibroblastos escamosos, muitas vezes modelados por alterações epigenéticas induzidas pelo tabagismo, mostram o padrão oposto: SMAD3 é silenciado e SMAD2 está aumentado. Esse estado aumenta genes relacionados à hipóxia e HIF‑1α, um regulador mestre das respostas a baixo oxigênio, mas paradoxalmente não se traduz em forte produção de VEGF‑A. Como resultado, esses tumores permanecem mais hipóxicos e necróticos, com suporte mais fraco para novos vasos apesar de um forte alarme interno de “baixo oxigênio”. 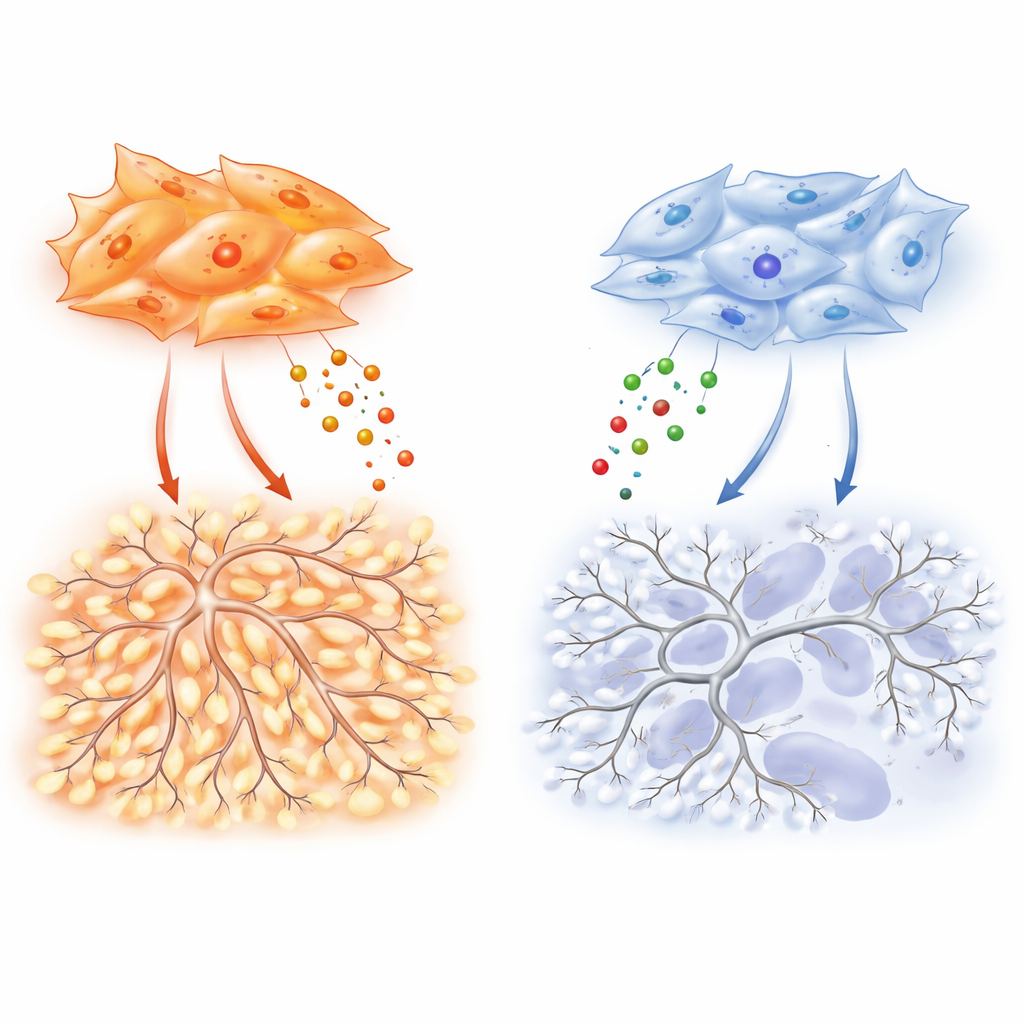
O que isso significa para pacientes e terapias futuras
Ao vincular o comportamento dos vasos aos programas dos fibroblastos em cada tipo tumoral, o estudo ajuda a explicar por que drogas antiangiogênicas funcionaram melhor em adenocarcinoma do que em câncer de pulmão escamoso. No adenocarcinoma, mirar no eixo SMAD3–VEGF–TIMP‑1 pode tanto normalizar a vasculatura anormal quanto aliviar a supressão imune local, tornando terapias que bloqueiam pontos de verificação imunológica mais eficazes. Em tumores escamosos, onde fibroblastos promovem um ambiente severo, pobre em oxigênio e ácido em vez de forte crescimento vascular, terapias que reduzam a hipóxia, neutralizem a acidez ou bloqueiem sinais inflamatórios específicos podem ser mais promissoras do que abordagens antiangiogênicas clássicas. Para os pacientes, este trabalho ressalta que o sucesso de tratamentos direcionados à vasculatura e ao sistema imune depende não apenas das células cancerosas, mas do estroma fibrótico que silenciosamente orquestra o suprimento sanguíneo do tumor.
Citação: Díaz-Valdivia, N., Duch, P., Ikemori, R. et al. Antagonistic SMAD2/3 control of TIMP-1, VEGF-A, and hypoxia signaling in myofibroblasts shapes histotype-specific angiogenesis in lung cancer. Cell Death Dis 17, 431 (2026). https://doi.org/10.1038/s41419-026-08677-2
Palavras-chave: angiogênese no câncer de pulmão, fibroblastos associados ao tumor, VEGF e TIMP-1, microambiente tumoral, sinalização SMAD