Clear Sky Science · es
Control antagónico de SMAD2/3 sobre TIMP-1, VEGF-A y la señalización por hipoxia en miofibroblastos modela la angiogénesis histotipo-específica en cáncer de pulmón
Por qué importan los vasos sanguíneos en los tumores de pulmón
El cáncer de pulmón no es una sola enfermedad, y los pacientes con distintos tipos tumorales suelen responder de forma muy diferente a los mismos fármacos. Este estudio plantea una pregunta sencilla pero crucial: ¿por qué algunos tumores pulmonares comunes desarrollan redes abundantes de vasos sanguíneos mientras otros se asfixian en bolsillos con bajo oxígeno, y cómo contribuye el tejido cicatricial circundante a decidir ese desenlace? Comprender esta conversación oculta entre las células cancerosas, las células de soporte y los vasos sanguíneos podría orientar tratamientos más precisos y mejorar el éxito tanto de la quimioterapia como de la inmunoterapia.
Dos cánceres de pulmón comunes, dos paisajes vasculares
Los autores se centran en las dos formas principales de cáncer de pulmón no microcítico: adenocarcinoma, que suele surgir en la periferia del pulmón, y carcinoma escamoso, que tiende a formarse más cerca de las vías respiratorias centrales. Al analizar miles de muestras de pacientes e imágenes de grandes bases de datos públicas, muestran que los adenocarcinomas suelen estar mejor vascularizados, con conductos vasculares más anchos y mayor actividad de genes vinculados al crecimiento vascular. En contraste, los tumores escamosos muestran con más frecuencia signos de mala perfusión, incluyendo extensas áreas de tejido necrótico y altos niveles de marcadores de hipoxia, que indican falta de oxígeno. Esta divergencia en el comportamiento vascular persiste incluso al ajustar por variables clínicas como edad, estadio tumoral e historial de tabaquismo. 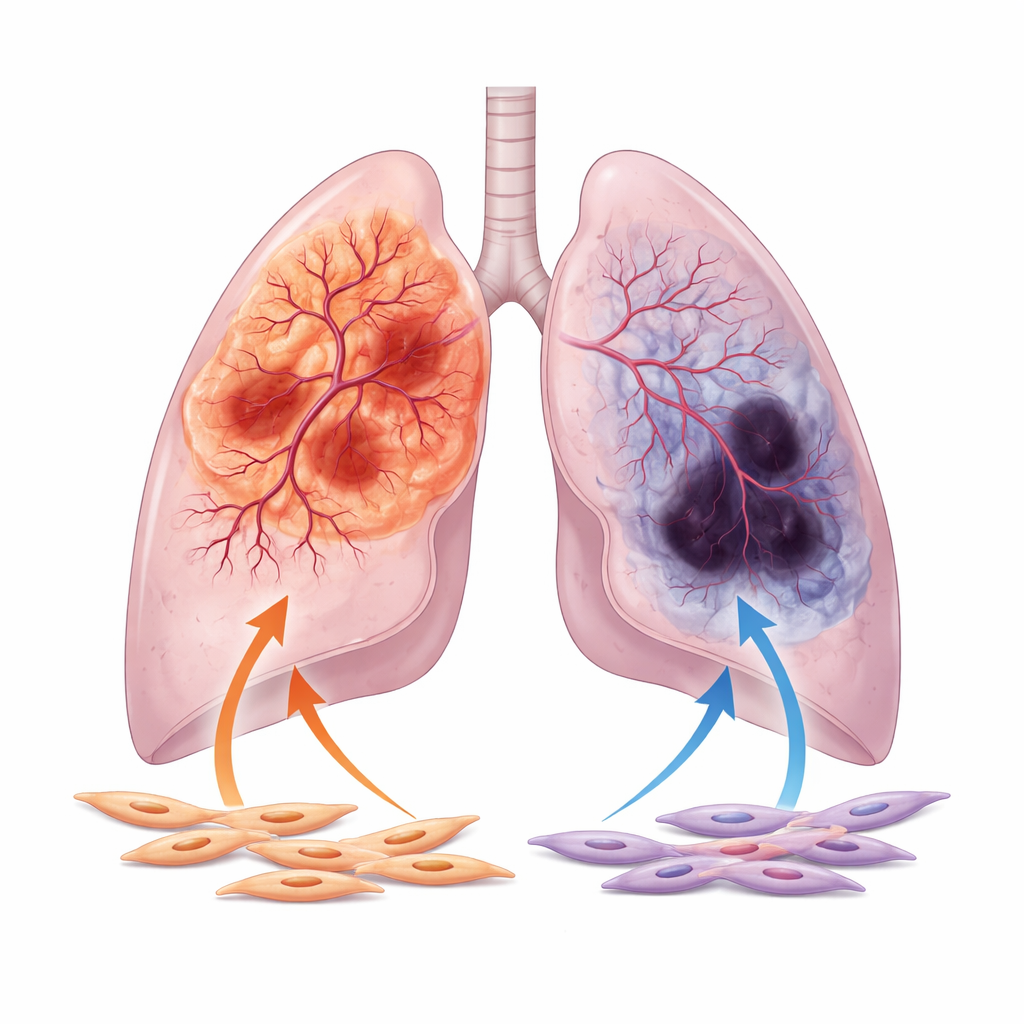
El poder silencioso de los fibroblastos tumorales
La atención se dirige entonces a los fibroblastos asociados al tumor, las células contráctiles, de tipo miofibroblasto, que rodean e infiltran los tumores pulmonares. Estas células, más conocidas por producir tejido cicatricial, también secretan muchas sustancias que pueden fomentar o frenar el crecimiento vascular. Usando secuenciación de ARN de célula única, los investigadores encuentran que los fibroblastos en adenocarcinoma interactúan más intensamente con las células endoteliales cercanas, los componentes de los vasos sanguíneos, que los fibroblastos en tumores escamosos. En platos de laboratorio, el medio recogido de fibroblastos de adenocarcinoma hace que las células endoteliales migren y formen redes capilares densas e entrelazadas, mientras que el medio de fibroblastos escamosos induce estructuras mucho más débiles y dispersas.
Mensajeros clave: VEGF, TIMP-1 y un interruptor molecular
Para identificar qué señales son responsables, el equipo perfila docenas de factores secretados. Los fibroblastos de adenocarcinoma producen niveles particularmente altos de VEGF-A, un impulsor clásico de la neoangiogénesis, y de TIMP-1, una proteína conocida como freno de las enzimas degradadoras de la matriz. Aquí, TIMP-1 muestra otra faceta: en experimentos controlados, añadir TIMP-1 aumenta la complejidad ramificada de las redes endoteliales, creando las arquitecturas enmarañadas típicas de los vasos tumorales. Eliminando TIMP-1 de fibroblastos de adenocarcinoma se reduce drásticamente la ramificación vascular en cultivo y disminuye la densidad de vasos y el crecimiento tumoral en ratones. Crucialmente, este efecto sobre la ramificación depende de un nivel basal de señalización por VEGF, lo que sugiere que VEGF hace de pedal de gas mientras TIMP-1 ajusta hasta qué punto se vuelve caótica la vasculatura resultante.
Controles opuestos del crecimiento frente a la hipoxia
Tras estas diferencias hay un "interruptor" molecular dentro de los fibroblastos que equilibra dos proteínas relacionadas, SMAD2 y SMAD3, que transmiten señales del factor de crecimiento TGF-β. Los fibroblastos de adenocarcinoma favorecen SMAD3, y esta alta proporción SMAD3/SMAD2 impulsa la sobreproducción de VEGF-A, TIMP-1 y otros factores promotores de vasos. Cuando los investigadores reducen SMAD3 en estas células, su capacidad para estimular la migración endotelial, la ramificación y la vascularización tumoral colapsa. Los fibroblastos escamosos, a menudo moldeados por cambios epigenéticos inducidos por el tabaquismo, muestran el patrón opuesto: SMAD3 está silenciado y SMAD2 aumentado. Este estado potencia genes relacionados con la hipoxia y HIF-1α, un regulador maestro de las respuestas a bajo oxígeno, pero paradójicamente no se traduce en una fuerte producción de VEGF-A. Como resultado, estos tumores permanecen más hipóxicos y necróticos, con un apoyo más débil para nuevos vasos a pesar de una alarmante señal interna de “bajo oxígeno”. 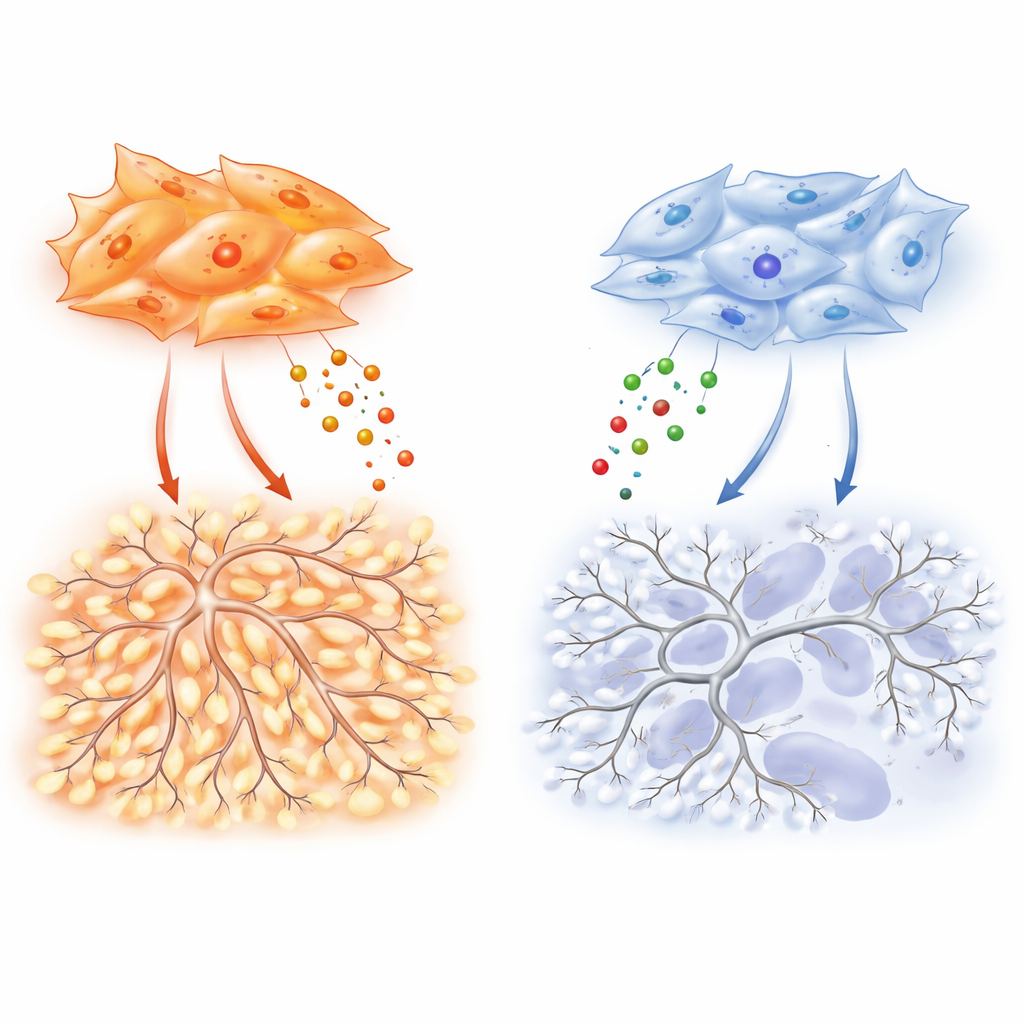
Qué significa esto para los pacientes y las terapias futuras
Al vincular el comportamiento de los vasos sanguíneos a los programas de los fibroblastos en cada tipo tumoral, el estudio ayuda a explicar por qué los fármacos antiangiogénicos han funcionado mejor en adenocarcinoma que en cáncer de pulmón escamoso. En el adenocarcinoma, dirigir el eje SMAD3–VEGF–TIMP-1 podría tanto normalizar la vasculatura anómala como aliviar la supresión inmune local, haciendo que las inmunoterapias basadas en bloqueo de puntos de control sean más efectivas. En los tumores escamosos, donde los fibroblastos promueven un entorno duro, pobre en oxígeno y ácido en lugar de un fuerte crecimiento vascular, las terapias que reduzcan la hipoxia, neutralicen la acidez o bloqueen señales inflamatorias específicas pueden ser más prometedoras que los enfoques antiangiogénicos clásicos. Para los pacientes, este trabajo subraya que el éxito de los tratamientos dirigidos a la vasculatura y al sistema inmune depende no solo de las células cancerosas, sino del estroma fibroso que organiza silenciosamente el suministro de sangre del tumor.
Cita: Díaz-Valdivia, N., Duch, P., Ikemori, R. et al. Antagonistic SMAD2/3 control of TIMP-1, VEGF-A, and hypoxia signaling in myofibroblasts shapes histotype-specific angiogenesis in lung cancer. Cell Death Dis 17, 431 (2026). https://doi.org/10.1038/s41419-026-08677-2
Palabras clave: angiogénesis en cáncer de pulmón, fibroblastos asociados al tumor, VEGF y TIMP-1, microambiente tumoral, señalización SMAD