Clear Sky Science · sv
Antagonistisk SMAD2/3-kontroll av TIMP-1, VEGF-A och hypoxisignalering i myofibroblaster formar histotyp-specifik angiogenes i lungcancer
Varför blodkärl i lungtumörer spelar roll
Lungcancer är inte en enda sjukdom, och patienter med olika tumörtyper svarar ofta mycket olika på samma läkemedel. Denna studie ställer en enkel men avgörande fråga: varför utvecklar vissa vanliga lungtumörer rika nätverk av blodkärl medan andra kvävs i syrerika lågfläckar – och hur bidrar det omgivande ärrliknande vävnadsskiktet till att avgöra utfallet? Att förstå denna dolda dialog mellan cancerceller, stödjeceller och blodkärl kan leda till mer precis behandling och förbättra både kemoterapi och immunoterapis effekt.
Två vanliga lungcancerformer, två vaskulära landskap
Forskarnas fokus ligger på de två stora formerna av icke-småcellig lungcancer: adenom och skivepitelcancer. Adenocarcinom uppstår ofta i lungans periferi, medan skivepitelcancer tenderar att bildas närmare de centrala luftvägarna. Genom att analysera tusentals patientsamples och bilder från stora offentliga databaser visar de att adenocarcinom generellt är bättre försörjda med blodkärl, med bredare kärlkanaler och starkare aktivitet i gener kopplade till kärltillväxt. I kontrast visar skivepitelstumörer oftare tecken på dålig blodtillförsel, inklusive utbredd nekros och höga nivåer av hypoximarkörer som signalerar syrebrist. Denna skillnad i vaskulärt beteende kvarstår även efter att man tagit hänsyn till kliniska variabler som ålder, tumörstadium och rökning.
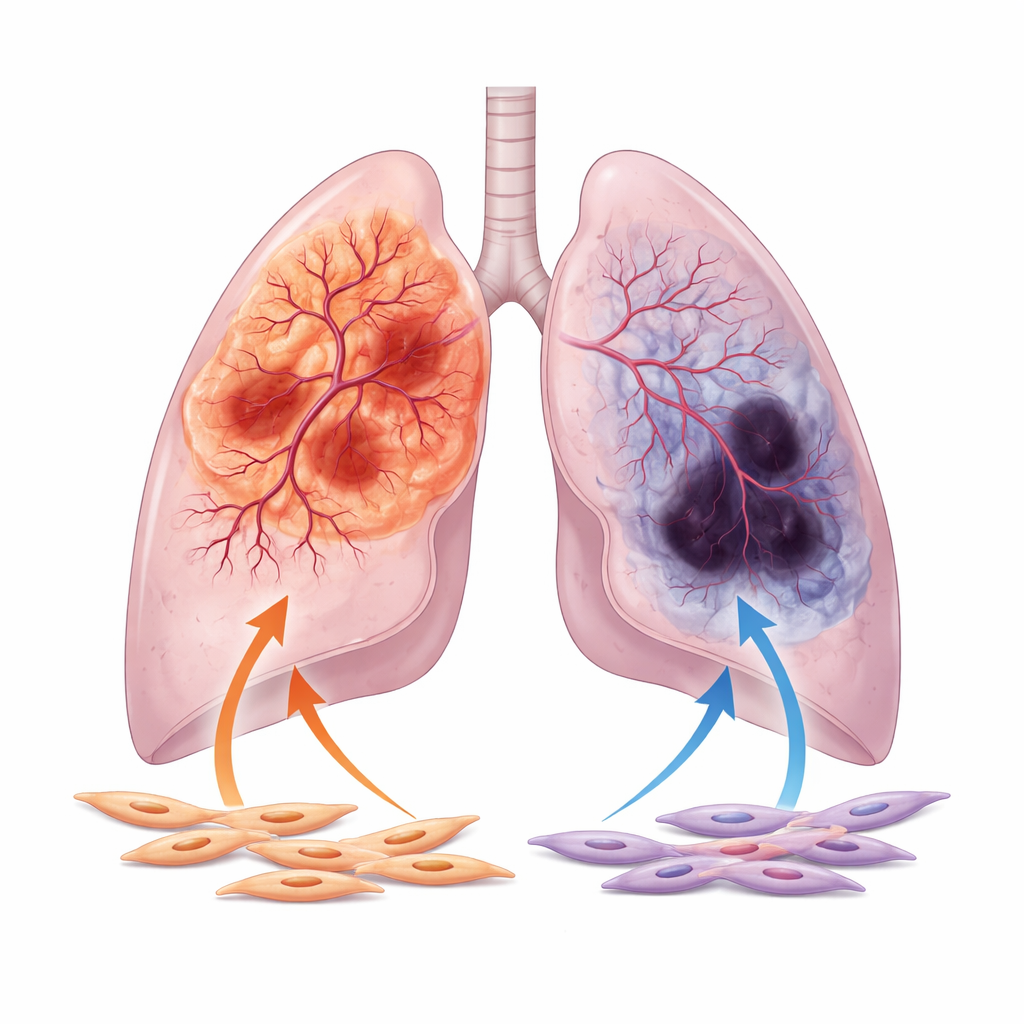
Den tysta kraften hos tumörfibroblaster
Uppmärksamheten skiftar sedan till tumörassocierade fibroblaster, de kontraktila, myofibroblastlika celler som omger och infiltrerar lungtumörer. Dessa celler, bättre kända för att producera ärrvävnad, utsöndrar också många ämnen som antingen kan främja eller hämma kärltillväxt. Med hjälp av enkelcells-RNA-sekvensering finner forskarna att fibroblaster i adenocarcinom interagerar mer intensivt med närliggande endotelceller, blodkärlens byggstenar, än fibroblaster i skivepitelstumörer. I laboratorieförsök gör vätska insamlad från adenocarcinom-fibroblaster att endotelceller migrerar och bildar täta, sammanflätade kapillärlika nätverk, medan vätska från skivepitelfibroblaster ger mycket svagare och glesare strukturer.
Nyckelbudbärare: VEGF, TIMP-1 och en molekylär brytare
För att ta reda på vilka signaler som är ansvariga profilerar teamet dussintals sekretoriska faktorer. Adenocarcinom-fibroblaster producerar särskilt höga nivåer av VEGF-A, en klassisk drivkraft för ny kärltillväxt, och TIMP-1, ett protein mer känt som en broms på vävnadsnedbrytande enzymer. Här visar TIMP-1 en annan sida: i kontrollerade experiment ökar tillsatt TIMP-1 förgreningskomplexiteten i endotel-nätverken och skapar de trassliga arkitekturer som är typiska för tumörkärl. Att ta bort TIMP-1 från adenocarcinom-fibroblaster minskar markant kärlgrenbildningen i kultur och reducerar kärltäthet och tumörtillväxt i möss. Avgörande är att denna förgreningseffekt beror på en basal nivå av VEGF-signalering, vilket tyder på att VEGF fungerar som gaspedalen medan TIMP-1 finjusterar hur kaotisk den resulterande vaskulaturen blir.
Motstående styrning av tillväxt respektive hypoxi
Bakom dessa olikheter finns en molekylär ”brytare” inne i fibroblasterna som balanserar två närbesläktade proteiner, SMAD2 och SMAD3, vilka förmedlar signaler från tillväxtfaktorn TGF-β. Adenocarcinom-fibroblaster favoriserar SMAD3, och detta höga förhållande SMAD3 till SMAD2 driver överproduktion av VEGF-A, TIMP-1 och andra kärlfrämjande faktorer. När forskarna dämpar SMAD3 i dessa celler kollapsar deras förmåga att stimulera endotelcellmigration, förgrening och tumörvaskularisering. Skivepitel-fibroblaster, ofta formade av rökrelaterade epigenetiska förändringar, visar det motsatta mönstret: SMAD3 tystas och SMAD2 ökar. Detta tillstånd stimulerar hypoxi-relaterade gener och HIF-1α, en huvudregulator för lågt syre, men paradoxalt nog översätts det inte till stark VEGF-A-produktion. Som följd förblir dessa tumörer mer hypoxiska och nekrotiska, med svagare stöd för nybildade kärl trots en stark intern ”lågt syre”-alarm.
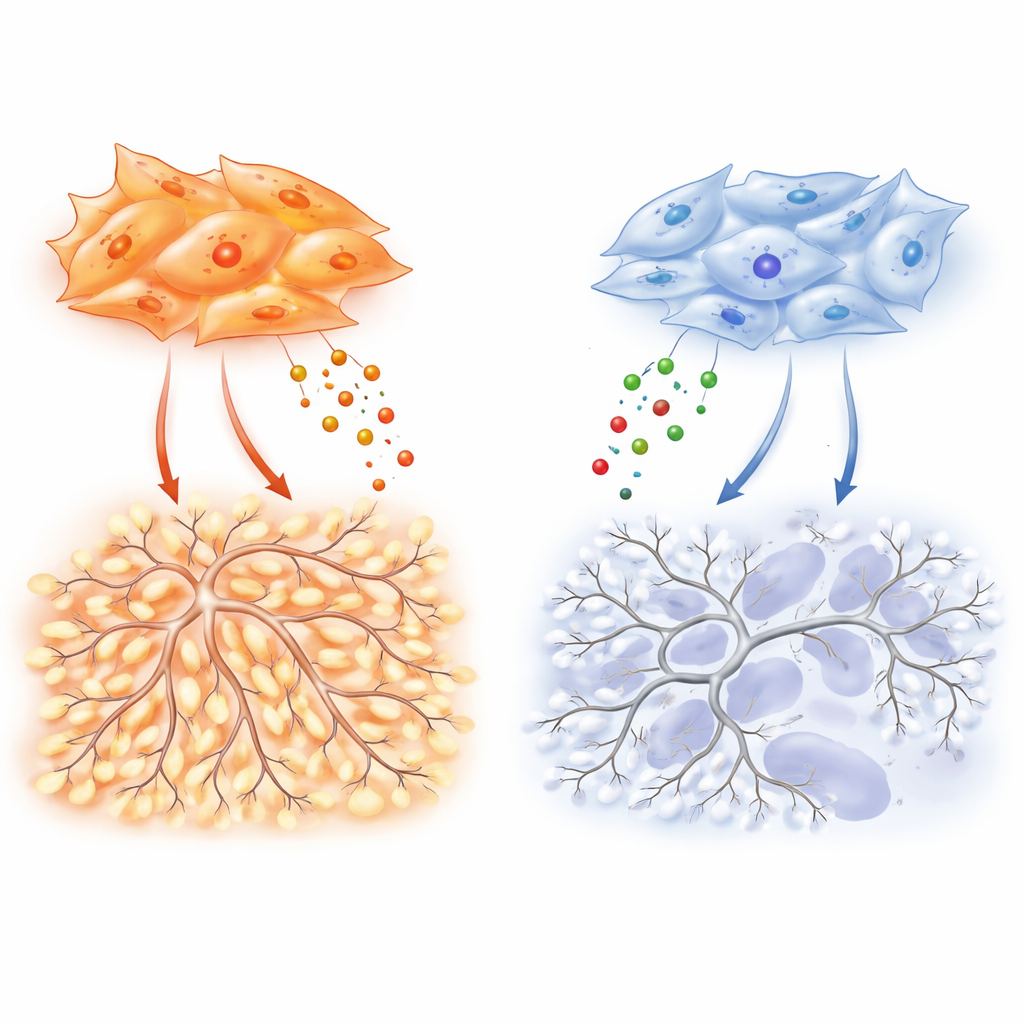
Vad detta betyder för patienter och framtida behandlingar
Genom att koppla blodkärlens beteende till fibroblastprogram i varje tumörtyp hjälper studien till att förklara varför anti-angiogena läkemedel fungerat bättre i adenocarcinom än i skivepitelcancer i lungan. I adenocarcinom kan riktning mot SMAD3–VEGF–TIMP-1-axeln både normalisera den abnorma vaskulaturen och lätta lokal immunsuppression, vilket kan göra checkpoint-hämmande immunoterapier mer effektiva. I skivepitelstumörer, där fibroblasterna snarare skapar en hård, syrefattig och sur miljö än stark kärltillväxt, kan terapier som lindrar hypoxi, neutraliserar surhet eller blockerar specifika inflammatoriska signaler vara mer lovande än klassiska anti-angiogena angreppssätt. För patienter understryker detta arbete att framgången för vaskulära och immuntinriktade behandlingar inte bara beror på cancercellerna, utan på den fibrösa stroma som tyst orkestrerar tumörens blodförsörjning.
Citering: Díaz-Valdivia, N., Duch, P., Ikemori, R. et al. Antagonistic SMAD2/3 control of TIMP-1, VEGF-A, and hypoxia signaling in myofibroblasts shapes histotype-specific angiogenesis in lung cancer. Cell Death Dis 17, 431 (2026). https://doi.org/10.1038/s41419-026-08677-2
Nyckelord: lungcancer angiogenes, tumörassocierade fibroblaster, VEGF och TIMP-1, tumörmikromiljö, SMAD-signalering