Clear Sky Science · it
Controllo antagonista di SMAD2/3 su TIMP-1, VEGF-A e segnalazione da ipossia nei miofibroblasti modella l’angiogenesi istotipo-specifica nel cancro del polmone
Perché i vasi sanguigni nei tumori polmonari sono importanti
Il cancro del polmone non è una singola malattia e pazienti con tipi tumorali diversi rispondono spesso in modo molto differente agli stessi farmaci. Questo studio pone una domanda semplice ma cruciale: perché alcuni tumori polmonari comuni sviluppano reti vascolari ricche mentre altri soffocano in nicchie a basso ossigeno — e come il tessuto circostante simile a una cicatrice contribuisce a decidere l’esito? Comprendere questa conversazione nascosta tra cellule tumorali, cellule di supporto e vasi sanguigni potrebbe guidare trattamenti più mirati e migliorare il successo sia della chemioterapia sia dell’immunoterapia.
Due tumori polmonari comuni, due paesaggi vascolari
Gli autori si concentrano sulle due forme principali di carcinoma polmonare non a piccole cellule: l’adenocarcinoma, che spesso origina nelle porzioni periferiche del polmone, e il carcinoma squamoso, che tende a formarsi più vicino alle vie aeree centrali. Analizzando migliaia di campioni di pazienti e immagini provenienti da grandi database pubblici, mostrano che gli adenocarcinomi sono generalmente meglio irrorati di sangue, con canali vascolari più ampi e maggiore attività di geni associati alla crescita vascolare. Al contrario, i tumori squamosi mostrano più spesso segni di scarsa perfusione, inclusi ampi tessuti necrotici e alti livelli di markers di ipossia, indicatori della mancanza di ossigeno. Questa divisione nel comportamento vascolare persiste anche dopo aver tenuto conto di variabili cliniche come età, stadio tumorale e storia di fumo. 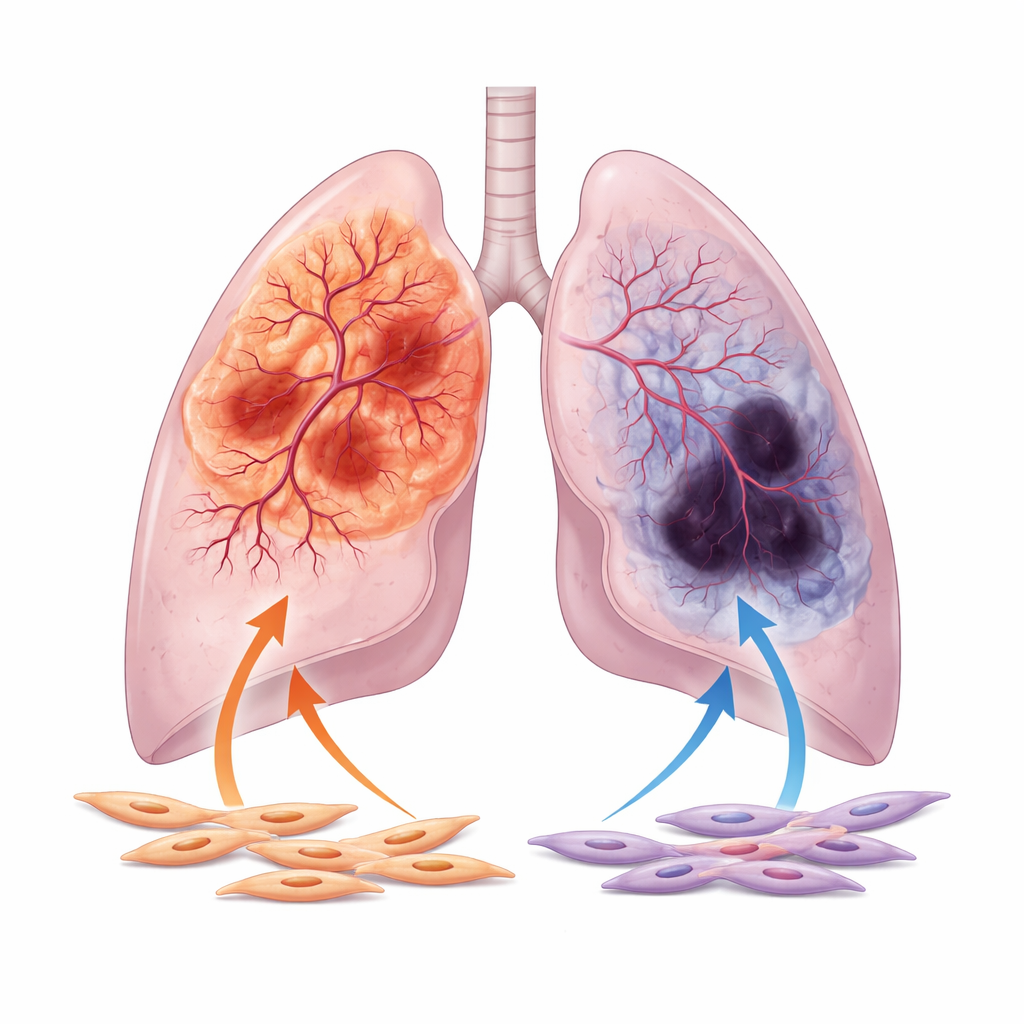
Il potere silenzioso dei fibroblasti tumorali
L’attenzione si sposta quindi sui fibroblasti associati al tumore, cellule contrattili di tipo miofibroblastico che circondano e infiltrano i tumori polmonari. Queste cellule, meglio note per la produzione di tessuto cicatriziale, secernono anche molte sostanze che possono incoraggiare o inibire la crescita dei vasi. Utilizzando il sequenziamento dell’RNA a singola cellula, i ricercatori rilevano che i fibroblasti nell’adenocarcinoma interagiscono in modo più intenso con le cellule endoteliali vicine, i mattoni dei vasi sanguigni, rispetto ai fibroblasti nei tumori squamosi. In colture, il fluido raccolto da fibroblasti di adenocarcinoma induce le cellule endoteliali a migrare e formare reti capillari dense e intrecciate, mentre il fluido dei fibroblasti squamosi genera strutture molto più deboli e rade.
Messaggeri chiave: VEGF, TIMP-1 e un interruttore molecolare
Per scoprire quali segnali sono responsabili, il team profila dozzine di fattori secreti. I fibroblasti dell’adenocarcinoma producono livelli particolarmente elevati di VEGF-A, un classico promotore della neoangiogenesi, e di TIMP-1, una proteina nota soprattutto come freno per gli enzimi degradanti la matrice. Qui TIMP-1 mostra un volto diverso: in esperimenti controllati, l’aggiunta di TIMP-1 aumenta la complessità di diramazione delle reti endoteliali, creando le architetture contorte tipiche dei vasi tumorali. L’eliminazione di TIMP-1 dai fibroblasti di adenocarcinoma riduce nettamente la ramificazione dei vasi in coltura e diminuisce la densità vascolare e la crescita tumorale nei modelli murini. Crucialmente, questo effetto di ramificazione dipende da un livello basale di segnalazione VEGF, suggerendo che VEGF funge da pedale dell’acceleratore mentre TIMP-1 regola la misura in cui la vascolarizzazione risultante diventa caotica.
Controlli opposti tra crescita e ipossia
Sottostante a queste differenze c’è un “interruttore” molecolare nei fibroblasti che bilancia due proteine correlate, SMAD2 e SMAD3, che trasmettono segnali dal fattore di crescita TGF-β. I fibroblasti dell’adenocarcinoma favoriscono SMAD3, e questo elevato rapporto SMAD3/SMAD2 spinge alla sovrapproduzione di VEGF-A, TIMP-1 e altri fattori promotori di vasi. Quando i ricercatori riducono SMAD3 in queste cellule, la loro capacità di stimolare la migrazione endoteliale, la ramificazione e la vascolarizzazione tumorale crolla. I fibroblasti squamosi, spesso plasmati da cambiamenti epigenetici indotti dal fumo, mostrano il modello opposto: SMAD3 è silenziato e SMAD2 è aumentato. Questo stato potenzia i geni correlati all’ipossia e HIF-1α, un regolatore principale delle risposte a basso ossigeno, ma paradossalmente non si traduce in una forte produzione di VEGF-A. Di conseguenza, questi tumori restano più ipossici e necrotici, con un supporto più debole per nuovi vasi nonostante un forte allarme interno di “basso ossigeno”. 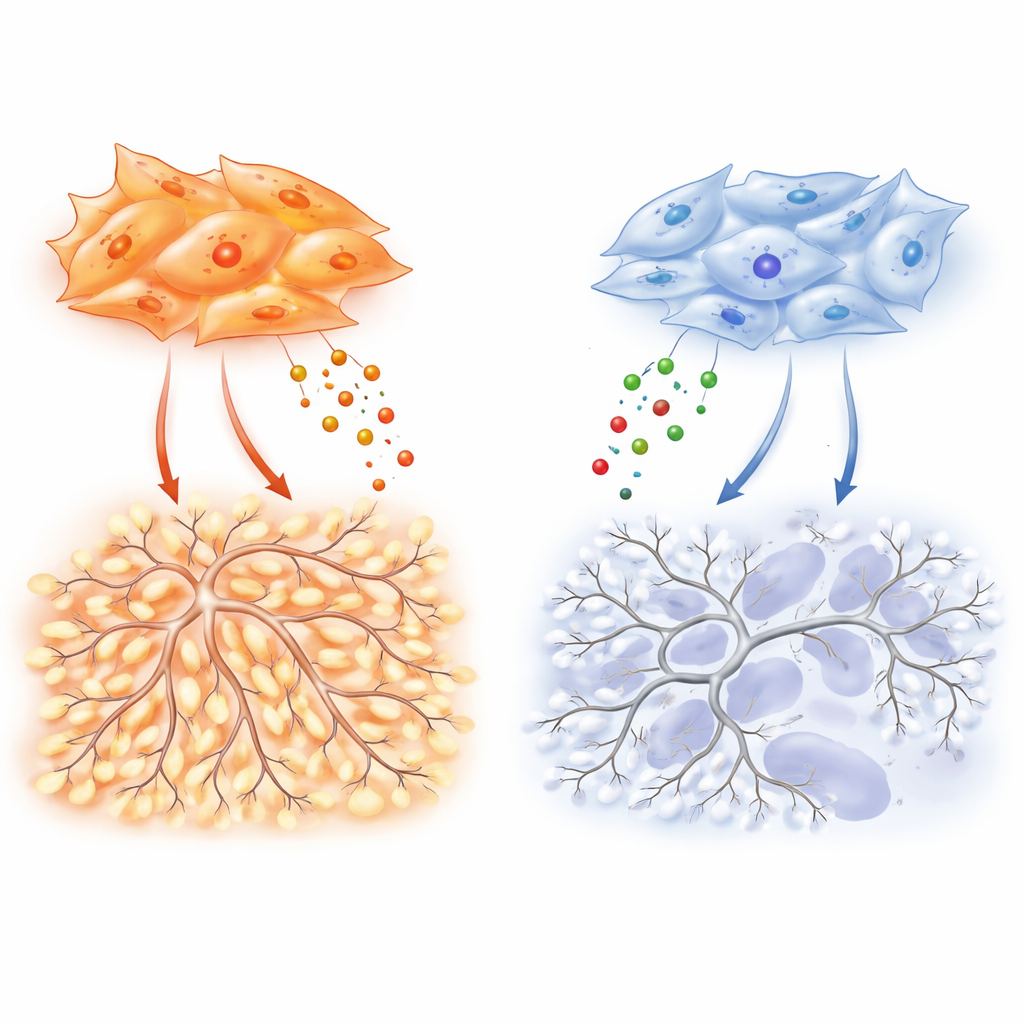
Cosa significa per i pazienti e le terapie future
Collegando il comportamento dei vasi ai programmi fibroblastici in ciascun tipo tumorale, lo studio aiuta a spiegare perché i farmaci anti-angiogenici hanno funzionato meglio negli adenocarcinomi rispetto ai carcinomi squamosi del polmone. Nell’adenocarcinoma, colpire l’asse SMAD3–VEGF–TIMP-1 potrebbe sia normalizzare la vascolarizzazione anomala sia alleviare la soppressione immunitaria locale, rendendo più efficaci le immunoterapie a blocco dei checkpoint. Nei tumori squamosi, dove i fibroblasti favoriscono un ambiente duro, povero di ossigeno e acido piuttosto che una forte crescita vascolare, terapie che riducano l’ipossia, neutralizzino l’acidità o blocchino specifici segnali infiammatori potrebbero essere più promettenti rispetto agli approcci anti-angiogenici classici. Per i pazienti, questo lavoro sottolinea che il successo dei trattamenti mirati alla vascolarizzazione e al sistema immunitario dipende non solo dalle cellule tumorali, ma anche dallo stroma fibroso che silenziosamente orchestra l’apporto di sangue al tumore.
Citazione: Díaz-Valdivia, N., Duch, P., Ikemori, R. et al. Antagonistic SMAD2/3 control of TIMP-1, VEGF-A, and hypoxia signaling in myofibroblasts shapes histotype-specific angiogenesis in lung cancer. Cell Death Dis 17, 431 (2026). https://doi.org/10.1038/s41419-026-08677-2
Parole chiave: angiogenesi nel cancro del polmone, fibroblasti associati al tumore, VEGF e TIMP-1, microambiente tumorale, segnalazione SMAD