Clear Sky Science · ja
拮抗的なSMAD2/3によるTIMP-1、VEGF-A、低酸素シグナルの制御が肺がんの筋線維芽細胞における組織型特異的血管新生を形づくる
腫瘍内の血管がなぜ重要か
肺がんは単一疾患ではなく、異なる腫瘍型の患者は同じ薬に対して大きく異なる反応を示すことがあります。本研究は単純だが重要な問いを投げかけます:なぜ一般的な肺腫瘍の中には豊かな血管ネットワークを張るものがある一方で、他は低酸素のポケットに窒息してしまうのか—そして周囲の瘢痕様組織がどのようにその結果を決めるのか? がん細胞、支持細胞、血管の間にあるこの目に見えない対話を理解すれば、より精密な治療を導き、化学療法や免疫療法の成功率を高める手がかりになります。
二つの一般的な肺がん、二つの血管の風景
著者らは非小細胞肺がんの二大型、すなわちしばしば肺の外縁で発生する腺がんと、気道中央付近にできやすい扁平上皮がんに注目します。多数の患者サンプルと大規模公開データベースの画像を解析した結果、腺がんは一般に血管がより豊富で、管腔が広く、血管成長に関連する遺伝子の活性が強いことが示されました。対照的に扁平上皮がんは、壊死組織の多発や酸素欠乏を示す低酸素マーカーの高発現など、血流不良の兆候をより頻繁に示します。この血管の違いは年齢、腫瘍病期、喫煙歴といった臨床変数を考慮しても持続します。 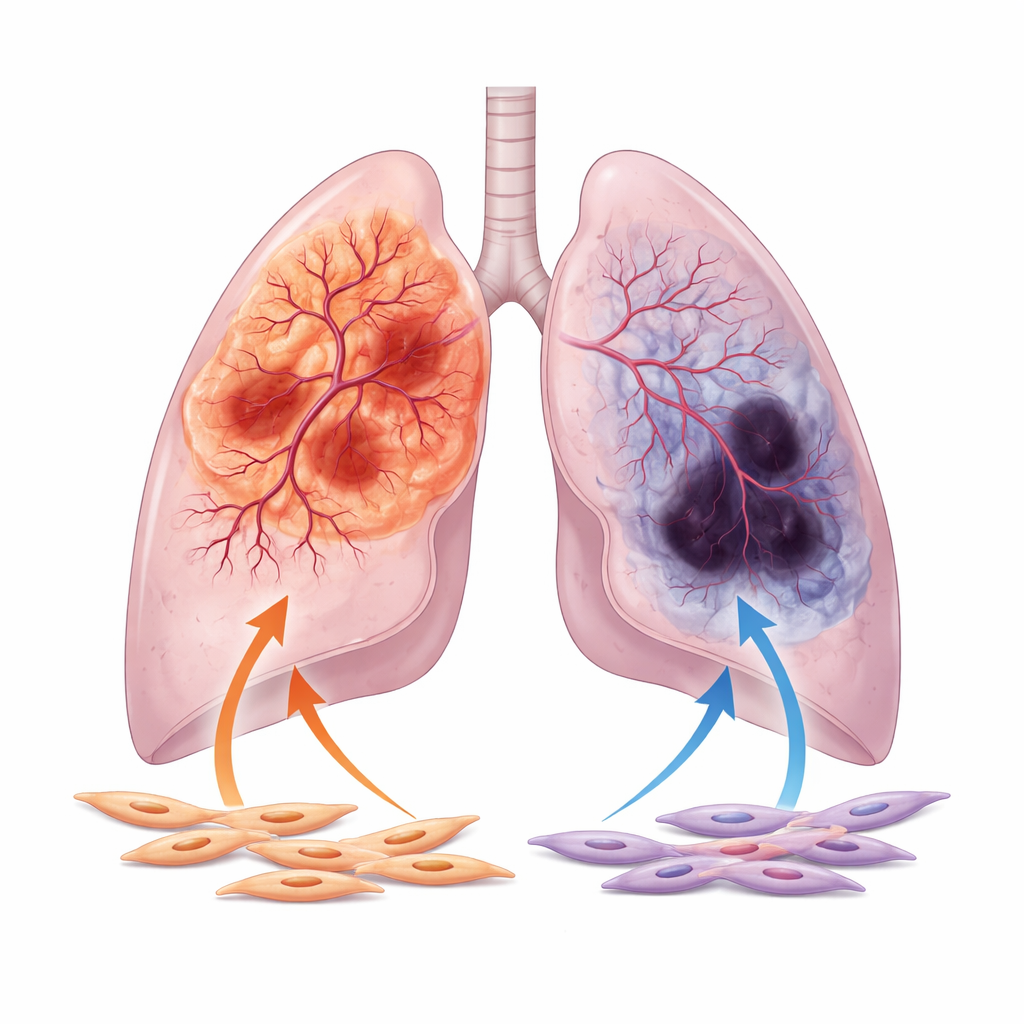
腫瘍線維芽細胞の静かな力
注目は腫瘍関連線維芽細胞、すなわち腫瘍を取り囲み浸潤する収縮性の筋線維芽細胞様の細胞に移ります。これらの細胞は瘢痕組織を産生することでよく知られていますが、血管成長を促進したり抑制したりする多くの分泌物も放出します。単一細胞RNAシーケンシングを用いると、腺がんの線維芽細胞は扁平上皮がんのそれよりも近傍の内皮細胞とより強く相互作用していることが分かりました。培養皿の実験では、腺がん由来の線維芽細胞から得た培養上清が内皮細胞を誘引し、密に絡み合う毛細血管様ネットワークを形成させる一方、扁平上皮がん由来の上清ははるかに弱くまばらな構造を誘導しました。
主要なメッセンジャー:VEGF、TIMP-1、そして分子スイッチ
どのシグナルが責任を負っているかを明らかにするため、研究者らは数十種の分泌因子をプロファイリングしました。腺がん線維芽細胞は新生血管の古典的駆動因子であるVEGF-Aと、組織分解酵素に対するブレーキとして知られるTIMP-1を特に高レベルで産生していました。ここでのTIMP-1は異なる顔を見せます:制御された実験では、TIMP-1を加えると内皮ネットワークの分岐複雑性が増し、腫瘍血管に典型的なもつれた構造を作り出しました。腺がん線維芽細胞からTIMP-1を除去すると、培養内での血管分岐が大幅に減少し、マウスにおける血管密度と腫瘍増殖が低下しました。重要なのは、この分岐効果は基礎的なVEGFシグナルの存在に依存しており、VEGFがアクセル役、TIMP-1が生成される血管構造の混沌度を微調整する役割を担っていることを示唆します。
成長と低酸素の相反する制御
これらの違いの根底には、線維芽細胞内部にある分子「スイッチ」があり、成長因子TGF-βからの信号を伝える関連タンパク質SMAD2とSMAD3のバランスを取っています。腺がん線維芽細胞はSMAD3を優位にし、この高いSMAD3/SMAD2比がVEGF-A、TIMP-1、その他の血管促進因子の過剰産生を駆動します。研究者らがこれらの細胞でSMAD3を下げると、内皮の遊走、分岐、腫瘍血管化を刺激する能力は崩壊しました。喫煙によるエピジェネティック変化に影響されたことが多い扁平上皮がんの線維芽細胞は逆のパターンを示します:SMAD3はサイレンシングされSMAD2が増加します。この状態は低酸素関連遺伝子と低酸素応答の主要調節因子であるHIF-1αを増強しますが、逆説的に強いVEGF-A産生にはつながりません。その結果、これらの腫瘍は内部で「低酸素」アラームが強いにもかかわらず新生血管の支援が弱く、より低酸素で壊死しやすいままになります。 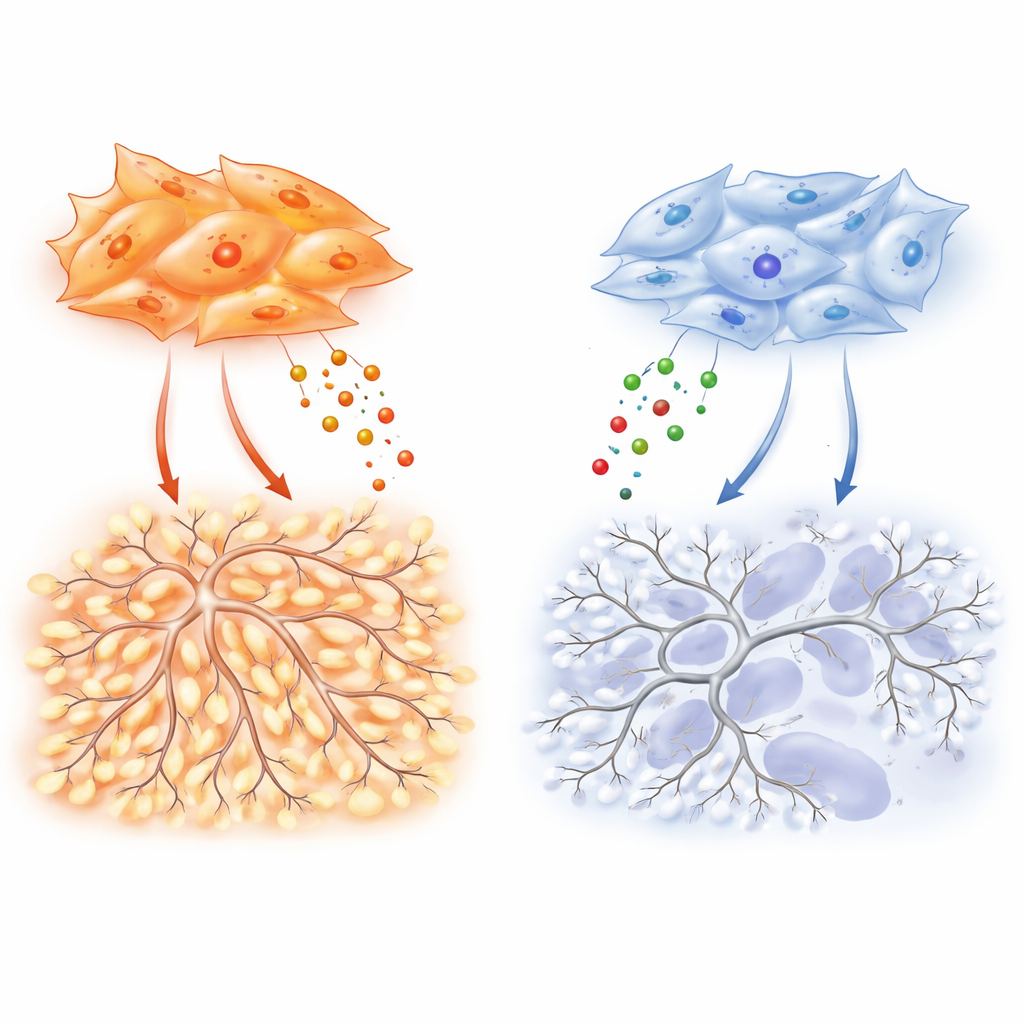
患者と将来の治療への意味
血管の振る舞いを各腫瘍型の線維芽細胞プログラムと結び付けることで、本研究は抗血管新生薬が腺がんで扁平上皮がんより効果的であった理由を説明する助けになります。腺がんではSMAD3–VEGF–TIMP-1軸を標的にすることで、異常な血管を正常化し局所的な免疫抑制を緩和し、チェックポイント阻害療法の効果を高める可能性があります。対照的に、扁平上皮がんでは線維芽細胞が強い血管成長ではなく厳しい低酸素・酸性環境を助長するため、低酸素の緩和、酸性の中和、あるいは特定の炎症性シグナルの遮断といった治療が従来の抗血管新生アプローチより有望かもしれません。患者にとっては、血管や免疫を標的とした治療の成功はがん細胞だけでなく、腫瘍の血管供給を静かに指揮する線維性間質にも依存することを本研究は強調しています。
引用: Díaz-Valdivia, N., Duch, P., Ikemori, R. et al. Antagonistic SMAD2/3 control of TIMP-1, VEGF-A, and hypoxia signaling in myofibroblasts shapes histotype-specific angiogenesis in lung cancer. Cell Death Dis 17, 431 (2026). https://doi.org/10.1038/s41419-026-08677-2
キーワード: 肺がんの血管新生, 腫瘍関連線維芽細胞, VEGFとTIMP-1, 腫瘍微小環境, SMADシグナル伝達