Clear Sky Science · ar
السيطرة المتضادة لـ SMAD2/3 على TIMP-1 وVEGF-A وإشارات نقص الأكسجة في الميوفايبروبلاست تشكل التكوّن الوعائي النوعي بنسيج سرطان الرئة
لماذا تهم الأوعية الدموية في أورام الرئة
سرطان الرئة ليس مرضًا واحدًا، والمرضى ذوو أنواع الأورام المختلفة غالبًا ما يستجيبون بشكل مختلف جدًا لنفس الأدوية. تطرح هذه الدراسة سؤالًا بسيطًا لكنه حاسم: لماذا تنشأ لدى بعض الأورام الرئوية الشائعة شبكات غنية من الأوعية الدموية بينما تختنق أخرى في جيوب منخفضة الأكسجين—وكيف يساهم النسيج الندبي المحيط في تحديد النتيجة؟ فهم هذا الحوار الخفي بين خلايا السرطان والخلايا الداعمة والأوعية الدموية قد يوجّه علاجات أكثر دقة ويعزز نجاح كل من العلاج الكيميائي والمناعي.
نوعان شائعان من سرطان الرئة، مشهدان وعائيان مختلفان
يركز المؤلفون على الشكلين الرئيسيين من سرطان الرئة غير صغير الخلايا: الغدي الذي ينشأ غالبًا في الجزء الخارجي من الرئة، وسرطان الخلايا الحرشفية الذي يميل إلى التكوّن أقرب للمجاري الهوائية المركزية. من خلال تحليل آلاف عينات المرضى والصور من قواعد بيانات عامة كبيرة، يبيّنون أن الأورام الغدية عادةً ما تكون أكثر تزويدًا بالدم، بقنوات أوعية أعرض ونشاط أقوى للجينات المرتبطة بنمو الأوعية. بالمقابل، تظهر الأورام الحرشفية في كثير من الأحيان علامات نقص التروية الدموية، بما في ذلك نسيج ميت واسع ومعدلات مرتفعة من علامات نقص الأكسجين، التي تشير إلى قلة الأكسجين. يستمر هذا الانقسام في السلوك الوعائي حتى بعد احتساب المتغيرات السريرية مثل العمر ومرحلة الورم وتاريخ التدخين. 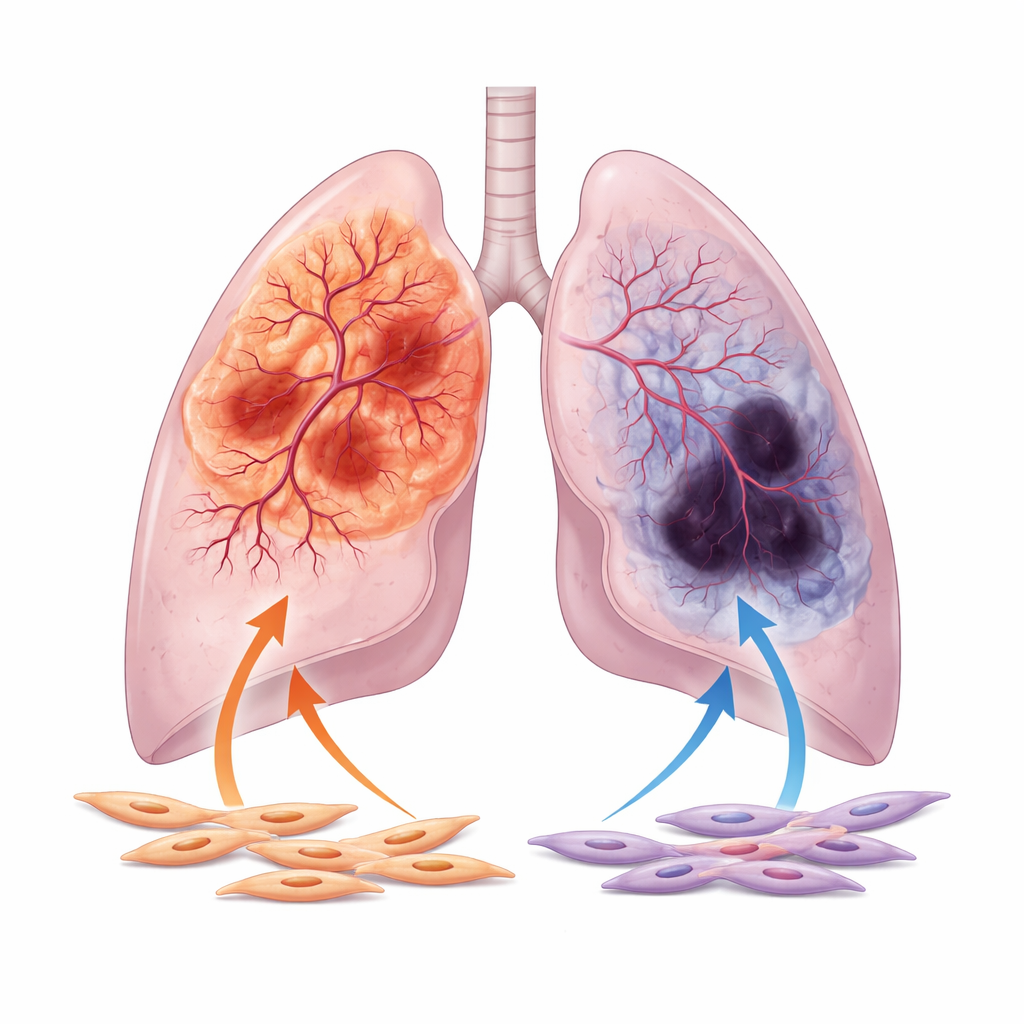
القوة الهادئة للخلايا الليفية الورمية
يتحوّل التركيز بعد ذلك إلى الخلايا الليفية المرتبطة بالورم، الخلايا الانقباضية الشبيهة بالميوفايبروبلاست التي تحيط بالأورام الرئوية وتخترقها. هذه الخلايا، المعروفة أكثر بإنتاج النسيج الندبي، تفرز أيضًا العديد من المواد التي يمكن أن تشجع أو تكبح نمو الأوعية. باستخدام تسلسل RNA أحادي الخلية، يجد الباحثون أن الخلايا الليفية في الأورام الغدية تتفاعل بشكل أكثر كثافة مع الخلايا البطانية المجاورة، وهي لبنات بناء الأوعية الدموية، مقارنة بالخلايا الليفية في الأورام الحرشفية. في أطباق المختبر، تجعل السوائل المجمعة من خلايا ليفية غدية الخلايا البطانية تهاجر وتشكل شبكات دقيقة متشابكة تشبه الشعيرات، بينما تحفز سوائل خلايا الليفية الحرشفية بنى أضعف وأكثر تباعدًا.
الرسل الرئيسيون: VEGF وTIMP-1 ومفتاح جزيئي
لكشف الإشارات المسؤولة، يقوم الفريق بتوصيف عشرات العوامل المفرزة. تنتج خلايا الليفية الغدية مستويات مرتفعة بشكل خاص من VEGF-A، المحرّك الكلاسيكي لنمو الأوعية الجديدة، وTIMP-1، البروتين المعروف أكثر بكبح إنزيمات تحلل الأنسجة. هنا يظهر TIMP-1 وجهًا مختلفًا: في تجارب محكمة، يؤدي إضافة TIMP-1 إلى زيادة تعقيد التفرع في شبكات الخلايا البطانية، مكوّنًا الهندسات الملتوية النموذجية لأوعية الأورام. إزالة TIMP-1 من خلايا الليفية الغدية تقلّل بشكل حاد من تفرع الأوعية في الثقافة وتخفض كثافة الأوعية الدموية ونمو الورم في الفئران. والأهم أن هذا التأثير التفرّعي يعتمد على مستوى أساسي من إشارة VEGF، مما يوحي بأن VEGF يعمل كدواسة الغاز بينما يقوم TIMP-1 بضبط مدى فوضوية الأوعية الناتجة.
ضوابط متقابلة للنمو مقابل نقص الأكسجة
تكمن تحت هذه الاختلافات «مفتاح» جزيئي داخل الخلايا الليفية يوازن بين بروتينين مرتبطين، SMAD2 وSMAD3، اللذين ينقلان إشارات من عامل النمو TGF-β. تفضّل خلايا الليفية الغدية SMAD3، ويقود هذا النسب العالي من SMAD3 إلى SMAD2 الإفراط في إنتاج VEGF-A وTIMP-1 وعوامل أخرى محفزة للأوعية. عندما يقلل الباحثون من SMAD3 في هذه الخلايا، تنهار قدرتها على تحفيز هجرة الخلايا البطانية والتفرع وتوعية الورم. تُظهر الخلايا الليفية الحرشفية، المتشكّلة غالبًا بتغيّرات فوق جينية ناجمة عن التدخين، النمط المعاكس: يُكبت SMAD3 ويزداد SMAD2. تعزز هذه الحالة جينات مرتبطة بنقص الأكسجة وHIF-1α، المنظم الرئيسي لاستجابات قلة الأكسجين، لكنها، بالمفارقة، لا تترجم إلى إنتاج قوي لـ VEGF-A. ونتيجة لذلك، تظل هذه الأورام أكثر تعرضًا لنقص الأكسجة والنخر، مع دعم أضعف للأوعية الجديدة على الرغم من إنذار داخلي قوي لـ «قلة الأكسجين». 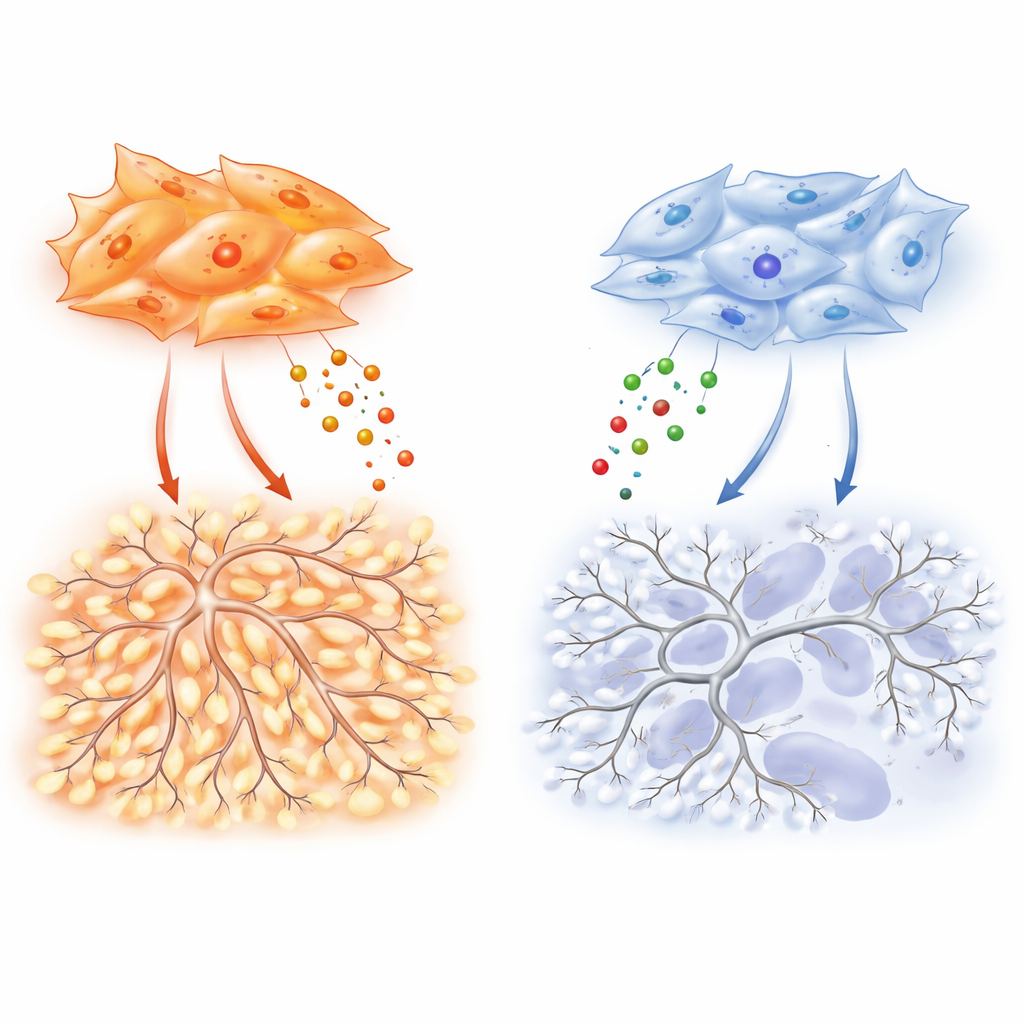
ما يعنيه ذلك للمرضى والعلاجات المستقبلية
من خلال ربط سلوك الأوعية ببرامج الخلايا الليفية في كل نوع ورمي، تساعد الدراسة على تفسير سبب فاعلية الأدوية المضادة للتكوّن الوعائي بشكل أفضل في الأورام الغدية مقارنة بسرطان الرئة الحرشفي. في الأورام الغدية، قد يستهدف محور SMAD3–VEGF–TIMP-1 كلٌّ من تطبيع الأوعية غير الطبيعية وتخفيف القمع المناعي المحلي، مما يجعل علاجات تفكيك نقاط التفتيش المناعية أكثر فعالية. في الأورام الحرشفية، حيث تلاشى دعم الخلايا الليفية إلى بيئة قاسية فقيرة بالأكسجين وحمضية بدلًا من نمو وعائي قوي، قد تكون العلاجات التي تخفف نقص الأكسجة أو تعادل الحموضة أو تحجب إشارات التهابية محددة أكثر وعدًا من المقاربات الكلاسيكية المضادة للتكوّن الوعائي. بالنسبة للمرضى، تؤكد هذه النتائج أن نجاح العلاجات المستهدفة للأوعية والمناعة لا يعتمد فقط على خلايا السرطان، بل على النسج الليفية التي تدير بهدوء تزويد الورم بالدم.
الاستشهاد: Díaz-Valdivia, N., Duch, P., Ikemori, R. et al. Antagonistic SMAD2/3 control of TIMP-1, VEGF-A, and hypoxia signaling in myofibroblasts shapes histotype-specific angiogenesis in lung cancer. Cell Death Dis 17, 431 (2026). https://doi.org/10.1038/s41419-026-08677-2
الكلمات المفتاحية: التكوّن الوعائي في سرطان الرئة, الخلايا الليفية المرتبطة بالورم, VEGF وTIMP-1, البيئة المجهرية للورم, إشارة SMAD