Clear Sky Science · zh
PCDHGC3 沉默通过激活 mTOR/HIF2α、重塑脂质代谢并规避铁死亡,促进清细胞肾细胞癌转移
这项肾癌研究为何重要
清细胞肾细胞癌是最常见的肾癌类型,以易转移和难以治疗著称。本研究揭示了单一细胞表面蛋白 PCDHGC3 的丧失如何帮助肿瘤生长、转移并规避一种与脂质损伤相关的细胞死亡方式。通过从细胞膜层面追溯到癌细胞如何处理脂质的变化,这项工作指向了新的联合疗法方向,可能使晚期肾癌对治疗更为敏感。
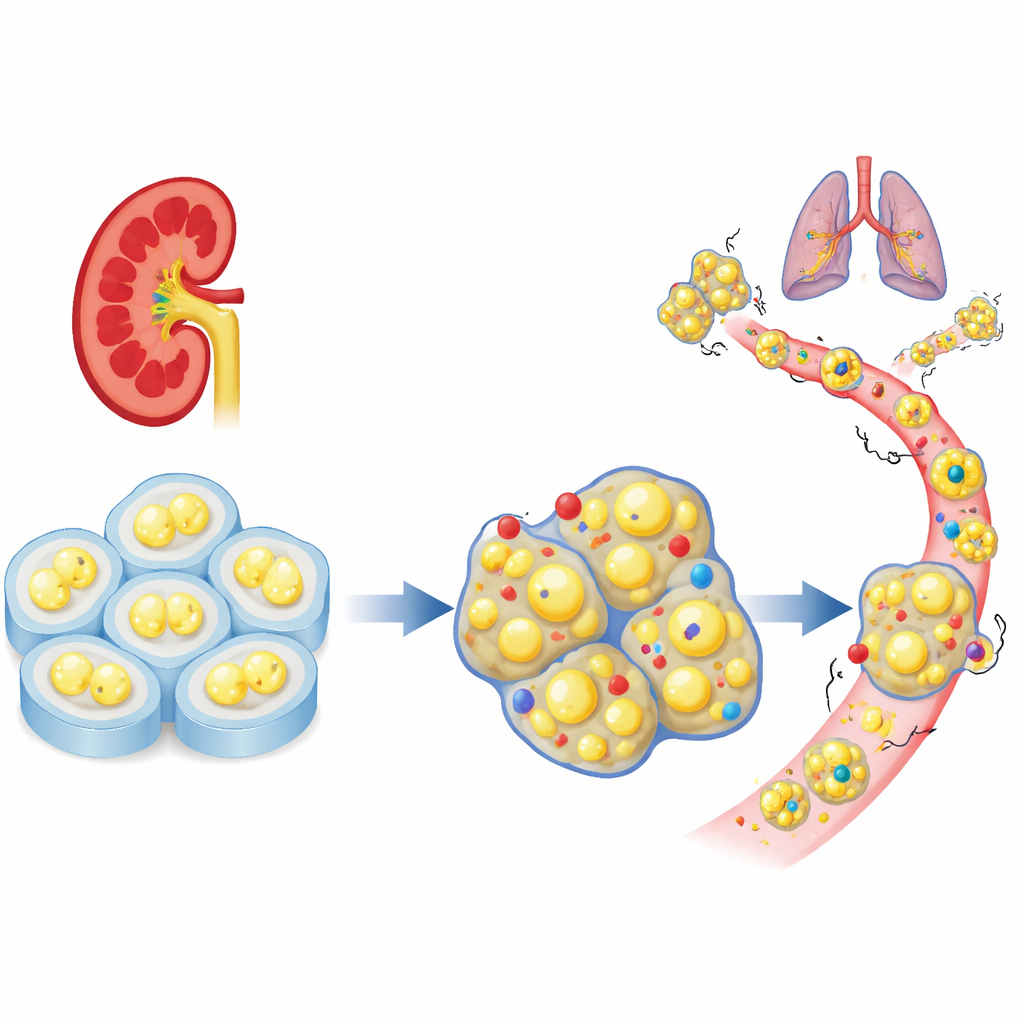
肾瘤中缺失的细胞“刹车”
研究者首先分析了大型病人数据集,以观察一类细胞黏附基因在清细胞肾癌中的表现。在数十个相关基因中,PCDHGC3 在正常组织中异常活跃,但在侵袭性肿瘤中表达降低而显得突出。肿瘤中该基因水平低的患者更可能出现晚期疾病且生存期更短。与许多同家族基因不同,PCDHGC3 并非简单地由 DNA 的大量化学标记关闭,这提示其受不同机制调控,并可能在肾细胞中发挥独特的保护作用。
从生长缓慢到具侵袭性的癌细胞
为验证 PCDHGC3 的功能,研究团队在两个人类肾癌细胞系中降低其表达,并与对照细胞比较。该基因被沉默后,细胞分裂更快、细胞周期推进加速,并在同一培养皿中胜过正常对照细胞。在更能模拟真实组织的三维生物打印肿瘤模型中,缺失 PCDHGC3 的细胞形成了更大、更致密的结构。在小鼠体内,缺乏该基因的肿瘤体积增加超过四倍,并显示出更多处于活跃分裂的细胞。这些改变的细胞也从紧密的上皮样形态转向更具可塑性和迁移性的形态,常与侵袭相关,而且在静脉注射后更容易形成远处肿瘤。
生长通路被推入超速档
深入信号传导机制后,研究者发现 PCDHGC3 的丧失会激活细胞内一个著名的生长调控器 mTOR,以及驱动蛋白合成与细胞存活的相关蛋白。细胞表面的一个关键黏附激酶——黏着斑激酶(focal adhesion kinase)也变得更为活跃,将膜层的改变与这一内部生长开关连接起来。其中一个特别重要的后果是名为 HIF2α 的因子异常积累,HIF2α 帮助肿瘤细胞适应低氧、支持血管生成并改变代谢。阻断 mTOR 或 HIF2α 的药物均可减缓缺失 PCDHGC3 细胞的过度增生,无论在平面培养还是三维模型中均有效,并在肾脏种植的小鼠模型中减少转移性肿瘤,提示该通路在侵袭性行为中居核心地位。
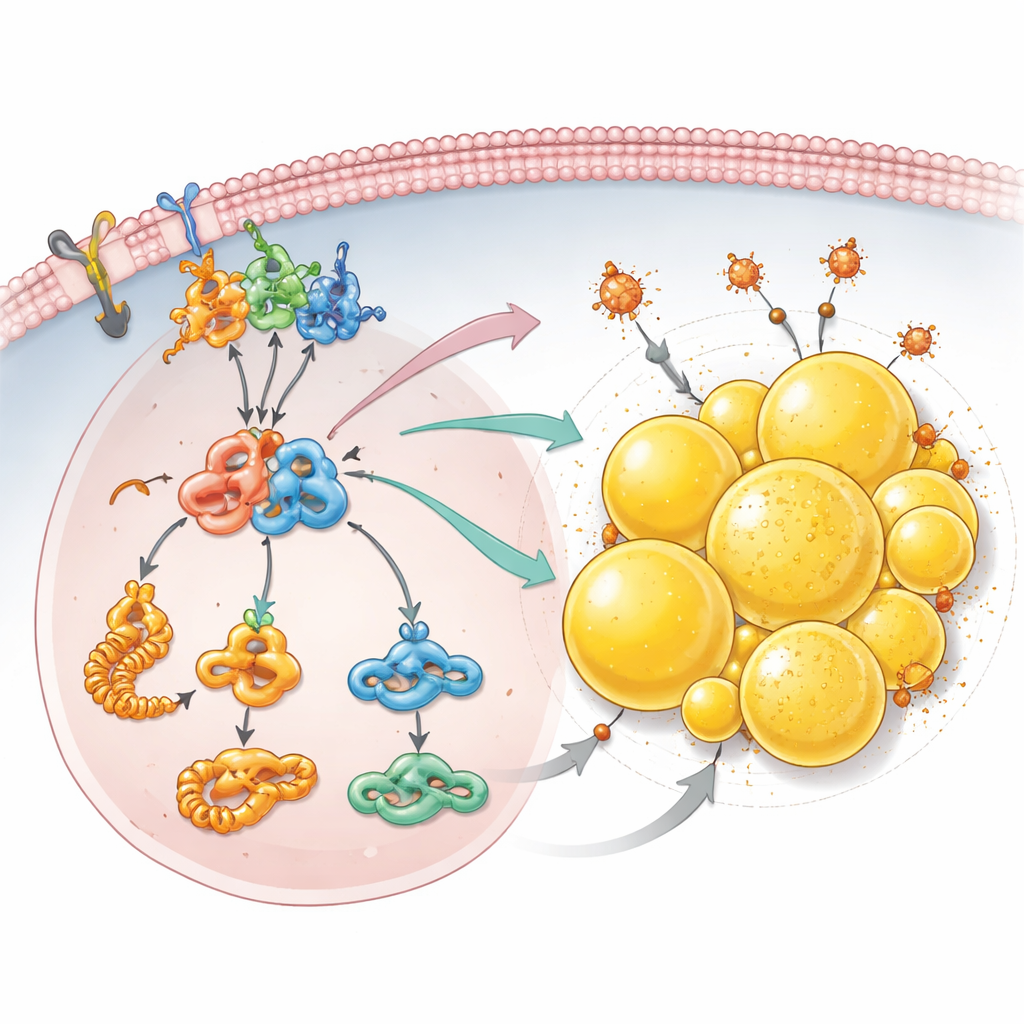
以脂储存作为规避细胞死亡的屏障
除了生长信号外,团队发现 PCDHGC3 丧失还重塑了癌细胞处理脂质的方式。详尽的蛋白质检测显示合成脂肪酸的构件增加,乙酰辅酶 A(用于合成脂质的关键燃料)水平升高。缺失 PCDHGC3 的细胞积累了更多脂滴——细胞内充满脂肪的小球,在该类型肾癌中尤为丰富。这种积累依赖于 mTOR–HIF2α 轴以及当 PCDHGC3 被沉默时上调的脂滴包膜蛋白 PLIN2。脂滴不仅仅是多余脂质的储存库:它们帮助细胞逃避免疫铁依赖且由受损脂质驱动的铁死亡。当特别是在已缺失 PCDHGC3 的细胞中减少 PLIN2 时,脂滴缩小,细胞对诱导铁死亡的药物敏感性显著增加。
将肿瘤的生存伎俩转为其弱点
综述而言,该研究揭示了一条链式事件:细胞表面的 PCDHGC3 丧失激活黏着斑激酶,开启 mTOR 与 HIF2α,增强脂质合成并构建由 PLIN2 包覆的保护性脂滴。这一网络不仅推动肿瘤生长和转移,还使癌细胞将易受损的脂质隔离开,以免遭受本可致死的反应。作者提出,针对新定义的 PCDHGC3–mTOR–HIF2α–PLIN2 轴可作为晚期清细胞肾癌的多重策略:将 mTOR 或 HIF2α 抑制剂与诱导铁死亡的药物联合使用,并可能抑制 PLIN2,有望把肿瘤的代谢适应转变为其阿喀琉斯之踵。
引用: Celada, L., Cubiella, T., San-Juan-Guardado, J. et al. PCDHGC3 silencing promotes clear cell renal cell carcinoma metastasis via mTOR/HIF2α activation, lipid metabolism rewiring, and ferroptosis evasion. Cell Death Dis 17, 409 (2026). https://doi.org/10.1038/s41419-026-08643-y
关键词: 清细胞肾细胞癌, PCDHGC3, mTOR HIF2alpha 通路, 脂滴, 铁死亡