Clear Sky Science · fr
La suppression de PCDHGC3 favorise les métastases du carcinome rénal à cellules claires via l’activation mTOR/HIF2α, le réarrangement du métabolisme des lipides et l’évasion de la ferroptose
Pourquoi cette recherche sur le cancer du rein est importante
Le carcinome rénal à cellules claires est la forme la plus courante de cancer du rein et se caractérise par une forte propension à métastaser et à résister aux traitements. Cette étude révèle comment la perte d’une seule protéine de surface cellulaire, nommée PCDHGC3, aide les tumeurs rénales à croître, à se propager et à échapper à une forme de mort cellulaire liée à l’altération des lipides. En retraçant cette chaîne d’événements depuis la membrane cellulaire jusqu’à la gestion des graisses par les cellules cancéreuses, le travail met en lumière de nouvelles combinaisons thérapeutiques susceptibles de rendre les cancers rénaux avancés plus vulnérables au traitement.
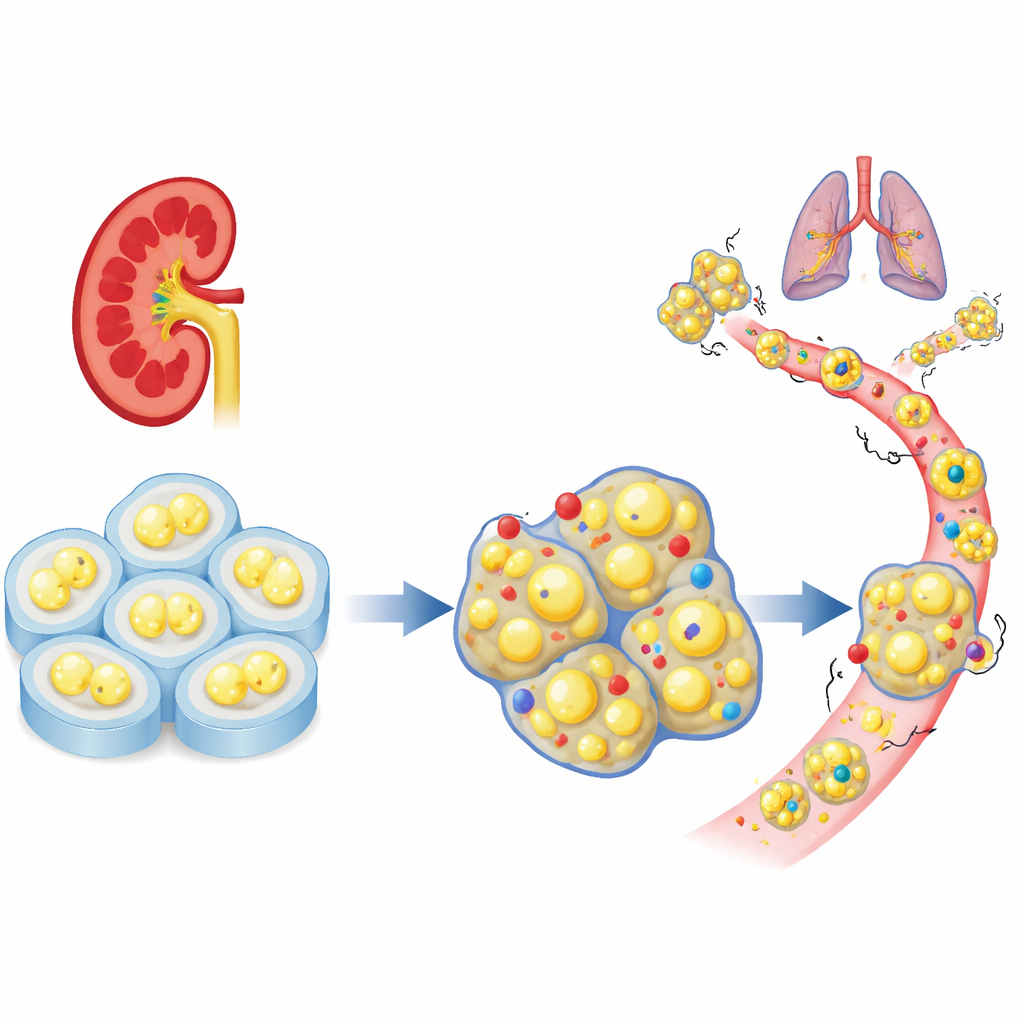
Un « frein » cellulaire absent dans les tumeurs rénales
Les chercheurs ont commencé par analyser de larges jeux de données de patients pour observer le comportement d’une famille de gènes d’adhésion cellulaire dans le carcinome rénal à cellules claires. Parmi des dizaines de gènes apparentés, PCDHGC3 s’est distingué : fortement exprimé dans les tissus normaux mais diminué dans les tumeurs agressives. Les patients dont les tumeurs présentaient de faibles niveaux de ce gène avaient davantage de maladies avancées et une survie plus courte. Contrairement à nombre de ses homologues, PCDHGC3 n’était pas simplement désactivé par une forte méthylation de l’ADN, ce qui suggère qu’il est régulé différemment et peut jouer un rôle protecteur spécifique dans les cellules rénales.
De cellules à croissance lente à des cellules invasives
Pour tester la fonction réelle de PCDHGC3, l’équipe a réduit son expression dans deux lignées cellulaires humaines de cancer du rein et les a comparées à des cellules témoins. Lorsque ce gène était réprimé, les cellules se divisaient plus rapidement, progressaient plus vite dans le cycle cellulaire et surpassaient leurs homologues normales cultivées dans le même milieu. Dans des modèles tumoraux 3D bio-imprimés, qui reproduisent mieux le tissu réel, les cellules déficientes en PCDHGC3 formaient des structures plus grandes et plus denses. Chez la souris, les tumeurs privées de ce gène étaient plus de quatre fois plus volumineuses et présentaient davantage de cellules en division active. Ces cellules modifiées ont aussi changé de morphologie, passant d’une forme épithéliale compacte à une forme plus souple et migratrice associée à l’invasion, et elles formaient plus facilement des tumeurs distantes après injection dans la circulation sanguine.
Une voie de croissance mise en surrégime
En sondant la machinerie de signalisation, les chercheurs ont découvert que la perte de PCDHGC3 active un contrôleur de croissance bien connu à l’intérieur des cellules, appelé mTOR, ainsi que des protéines connexes qui stimulent la synthèse protéique et la survie. Une enzyme d’adhésion clé à la surface cellulaire, la focal adhesion kinase, devenait elle aussi plus active, reliant les changements membranaires à cet interrupteur de croissance interne. Une conséquence particulièrement importante était l’accumulation anormale d’un facteur nommé HIF2α, qui aide les cellules tumorales à s’adapter à la faible oxygénation, à promouvoir l’angiogenèse et à modifier leur métabolisme. Des médicaments bloquant mTOR ou HIF2α ralentissaient chacun la prolifération des cellules déficientes en PCDHGC3, tant en cultures bidimensionnelles qu’en modèles 3D, et réduisaient aussi les tumeurs métastatiques dans un modèle murin avec rein implanté, ce qui suggère que cette voie est centrale pour le comportement agressif.
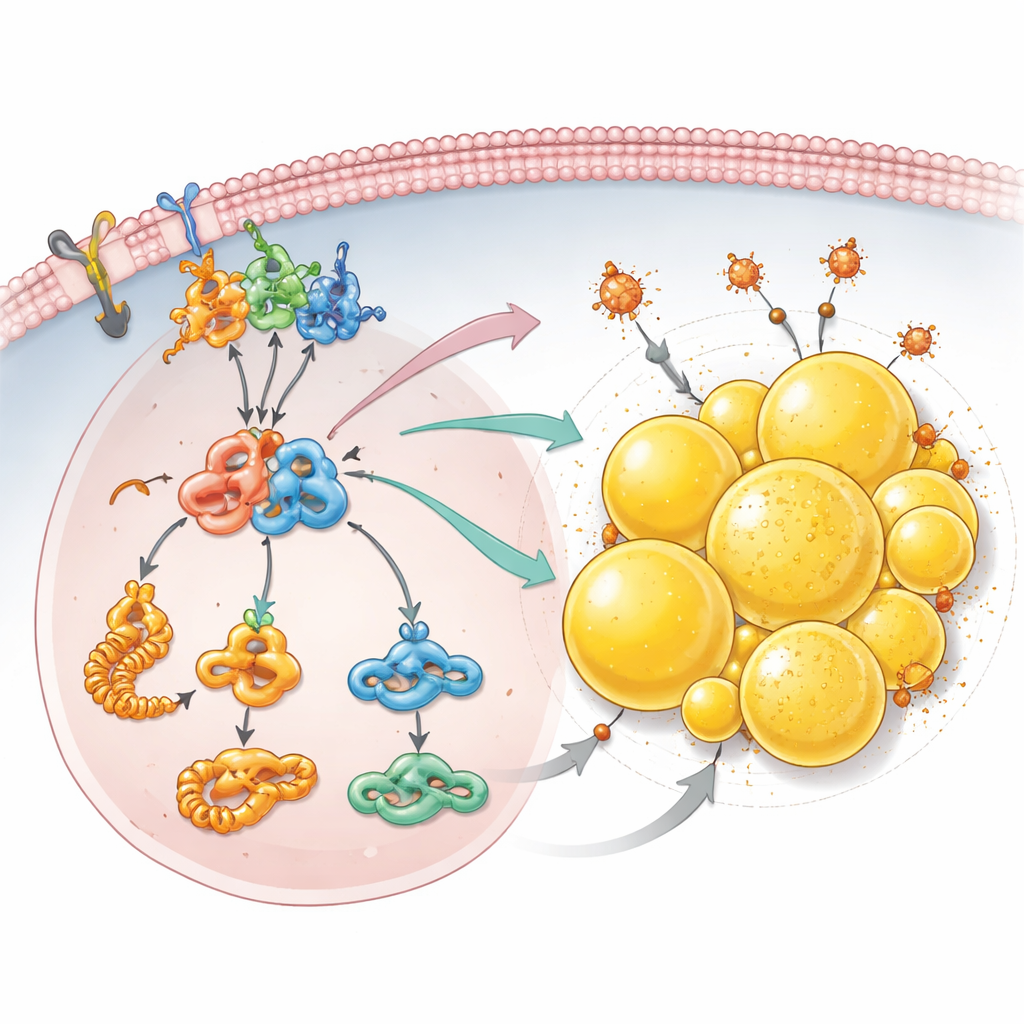
Le stockage des graisses comme bouclier contre la mort cellulaire
Au-delà des signaux de croissance, l’équipe a découvert que la perte de PCDHGC3 réoriente la façon dont les cellules cancéreuses gèrent les lipides. Des analyses protéiques détaillées ont montré une augmentation de la production de précurseurs des acides gras et des niveaux accrus d’acétyl-CoA, un carburant central utilisé pour synthétiser des lipides. Les cellules privées de PCDHGC3 accumulaient beaucoup plus de gouttelettes lipidiques — de petites sphères remplies de graisse à l’intérieur de la cellule, particulièrement abondantes dans ce type de cancer du rein. Cette accumulation dépendait de l’axe mTOR–HIF2α et de PLIN2, une protéine recouvrant les gouttelettes dont l’expression augmentait lorsque PCDHGC3 était réprimé. Ces gouttelettes faisaient plus que stocker l’excès de graisse : elles aidaient les cellules à échapper à la ferroptose, une forme de mort cellulaire induite par le fer et l’endommagement des lipides. Lorsque PLIN2 était diminué, en particulier dans les cellules déjà dépourvues de PCDHGC3, les gouttelettes lipidiques diminuaient et les cellules devenaient beaucoup plus sensibles à un médicament qui induit la ferroptose.
Transformer l’astuce de survie d’une tumeur en sa faiblesse
Au total, l’étude révèle une chaîne d’événements où la perte de PCDHGC3 à la surface cellulaire active la focal adhesion kinase, met en marche mTOR et HIF2α, augmente la synthèse lipidique et favorise la formation de gouttelettes protectrices revêtues de PLIN2. Ce réseau alimente non seulement la croissance tumorale et la dissémination, mais permet aussi aux cellules cancéreuses de mettre à l’abri des lipides vulnérables contre des réactions destructrices qui les tueraient autrement. Les auteurs proposent que cibler cet axe nouvellement défini PCDHGC3–mTOR–HIF2α–PLIN2 pourrait offrir une stratégie multiprise pour le carcinome rénal à cellules claires avancé : combiner des inhibiteurs de mTOR ou de HIF2α avec des agents qui induisent la ferroptose, et potentiellement bloquer PLIN2, pourrait transformer l’adaptation métabolique de la tumeur en talon d’Achille.
Citation: Celada, L., Cubiella, T., San-Juan-Guardado, J. et al. PCDHGC3 silencing promotes clear cell renal cell carcinoma metastasis via mTOR/HIF2α activation, lipid metabolism rewiring, and ferroptosis evasion. Cell Death Dis 17, 409 (2026). https://doi.org/10.1038/s41419-026-08643-y
Mots-clés: carcinome rénal à cellules claires, PCDHGC3, voie mTOR HIF2alpha, gouttelettes lipidiques, ferroptose