Clear Sky Science · he
שתיקת PCDHGC3 מקדמת גרורת סרטן כליה של תאי צלולית דרך הפעלת mTOR/HIF2α, שינוי מטבוליזם השומנים והימנעות מפרורפטוזיס
מדוע המחקר הזה על סרטן הכליה חשוב
סרטן כליה של תאי צלולית הוא הצורה השכיחה ביותר של סרטן הכליה ומפורסם בנטייתו להתפשט לאיברים אחרים ולהתנגד לטיפולים. מחקר זה חושף כיצד אובדן חלבון יחיד על פני התא, המכונה PCDHGC3, מסייע לגידולי כליה לגדול, להתפשט ולהתחמק מצורת מוות תאי הקשורה לנזק לשומנים. במעקב אחר שרשרת אירועים זו מהממברנה ועד לאופן שבו תאי הסרטן מטפלים בשומנים, העבודה מצביעה על טיפולים משולבים חדשים שעשויים להפוך סרטן כליה מתקדם לפגיע יותר לטיפול.
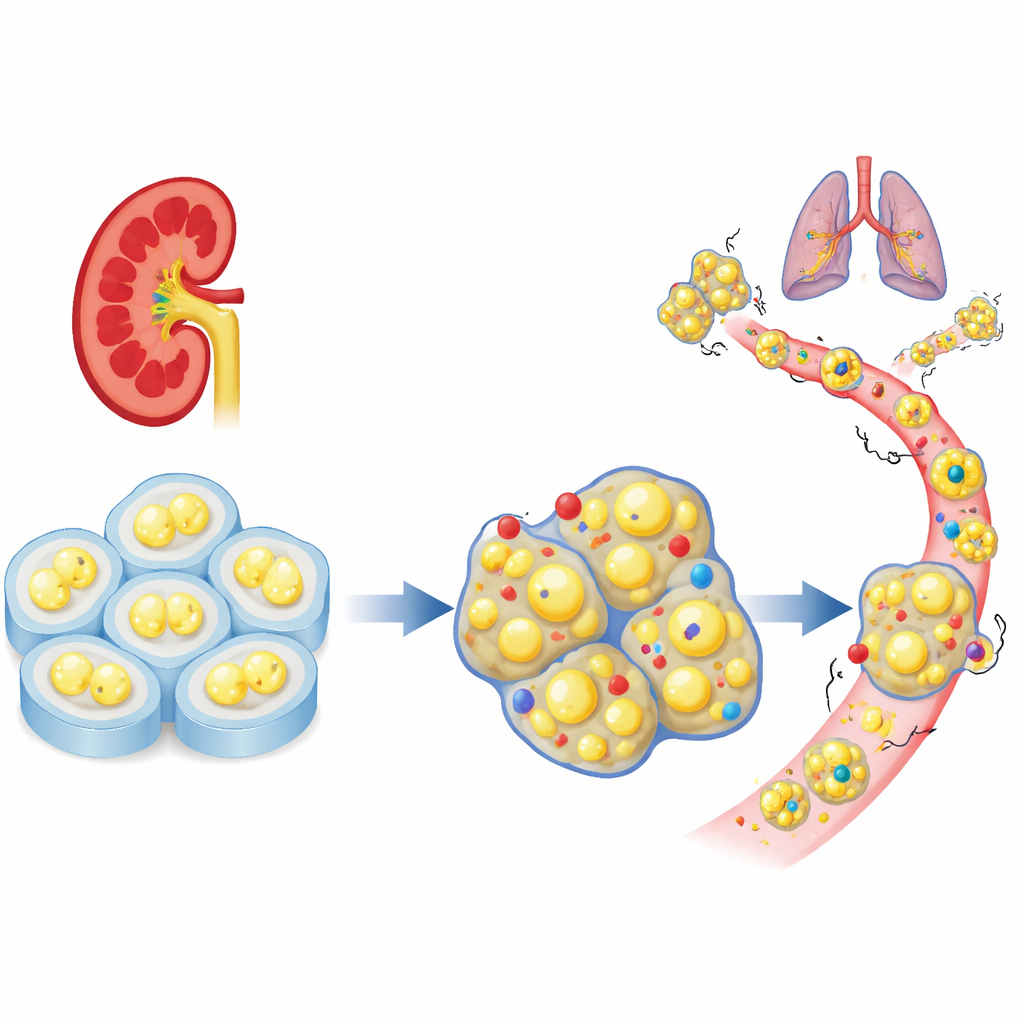
"בלם" תאילתי חסר בגידולי הכליה
החוקרים החלו בבדיקת מאגרי נתונים גדולים של חולים כדי לראות כיצד משפחת גני ההיצמדות התאית מתנהגת בסרטן כליה של תאי צלולית. מבין עשרות גנים קרובים, PCDHGC3 בלט כפעיל בצורה חריגה ברקמה נורמלית אך מופחת בגידולים אגרסיביים. חולים שלגידוליהם היו רמות נמוכות של גן זה נטו להציג מחלה מתקדמת ותוחלת חיים נמוכה יותר. בשונה מרבים מקרובי משפחתו, PCDHGC3 לא כובתה פשוט על ידי תגובות כימיות כבדות על ה‑DNA, מה שמרמז שהיא מווסתת באופן שונה ועלולה למלא תפקיד מגן ייחודי בתאי הכליה.
מתאים שגדל לאט לתאים פולשים
כדי לבדוק מה PCDHGC3 עושה בפועל, הצוות הפחית את רמותיו בשני קווי תאי סרטן כליה אנושיים והשווה אותם לתאים ביקורת. כאשר הגן דוכא, התאים התחלקו מהר יותר, עברו את מחזור החיים התאי במהירות רבה יותר וניצחו תאים נורמליים שגודלו באותו צלחת. במודלים תלת־ממדיים המדפיסים ביולוגית שמחקים רקמה אמיתית טוב יותר, תאים חסרי PCDHGC3 יצרו מבנים גדולים וצפופים יותר. בעכברים, גידולים חסרי הגן גדלו יותר מארבע פעמים והראו יותר תאים מתחלקים באופן פעיל. תאים משונים אלו גם הראו מעבר מצורה אפיתליאלית קומפקטית לצורה גמישה ונודדת הקשורה לפלישה, והם יצרו גרורות מרוחקות ביתר קלות לאחר הזרקה למחזור הדם.
מסלול גדילה שהופעל יתר על המידה
בחיפוש אחרי מכניקת האיתות התאית, החוקרים מצאו שאובדן PCDHGC3 מפעיל בקרה גדילה מוכרת בתוך התאים בשם mTOR, יחד עם חלבונים קשורים שמניעים סינתזת חלבונים והישרדות. אנזים הצמדה מוקדית במשטח התא, focal adhesion kinase, הפך גם הוא ליעיל יותר, וקישר בין שינויים בממברנה למתג הגדילה הפנימי הזה. אחת התוצאות החשובות הייתה הצטברות חריגה של גורם שנקרא HIF2α, שמסייע לתאי הגידול להסתגל לחוסר חמצן, לתמוך ביצירת כלי דם ולשנות את המטבוליזם שלהם. תרופות החוסמות mTOR או HIF2α האטו כל אחת את הצמיחה המוגזמת של תאים חסרי PCDHGC3, הן בתרביות שטוחות והן במודלים תלת־ממדיים, והפחיתו גם גידולים גרורתיים במודל עכבר עם שתילת כליה, מה שמרמז שהמסלול הזה מרכזי להתנהגות האגרסיבית.
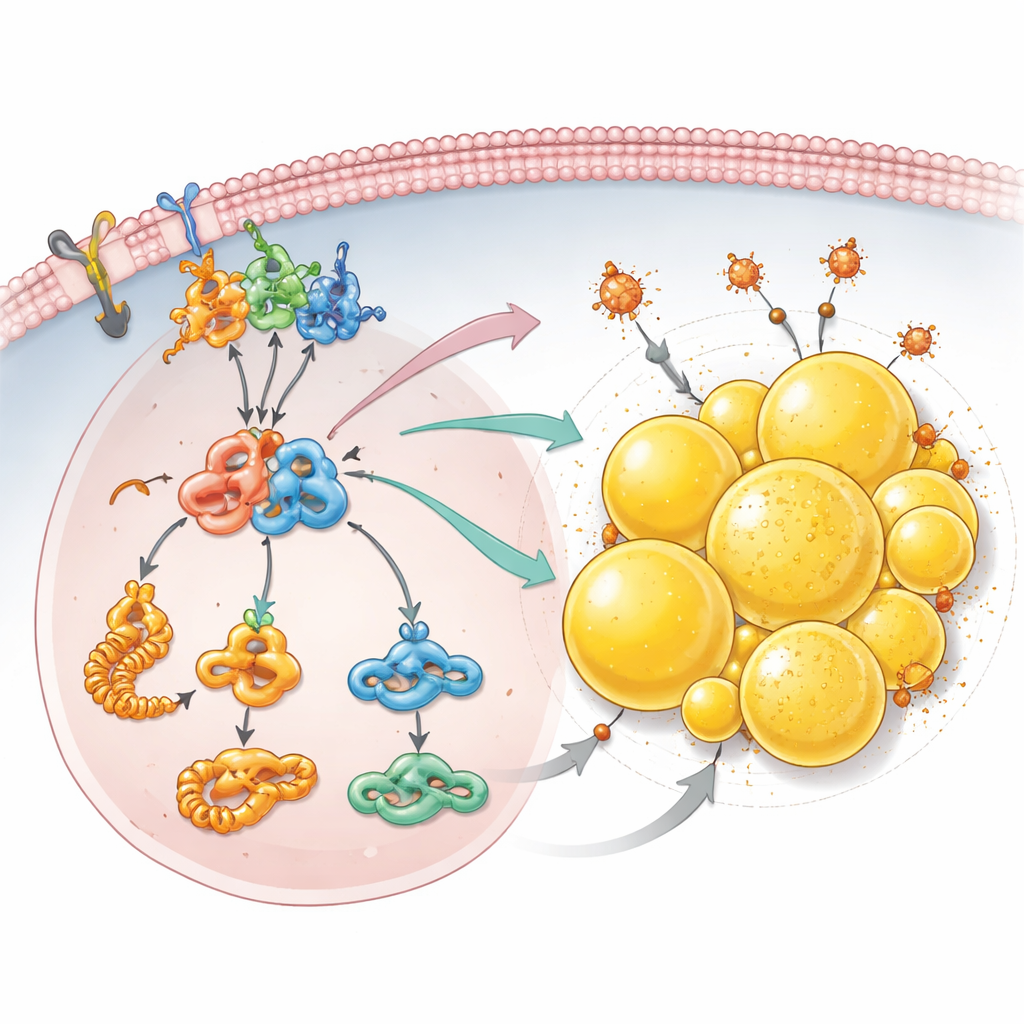
אחסון שומן כמגן מפני מוות תאי
מעבר לאותות גדילה, הצוות גילה שאובדן PCDHGC3 משנה את האופן שבו תאי הסרטן מטפלים בשומנים. סקרי חלבונים מפורטים הראו עלייה בייצור אבני בניין לחומצות שומן ועליה ברמות של אצטיל‑CoA, דלק מרכזי לשילוב ליפידים. תאים חסרי PCDHGC3 צברו הרבה יותר טיפות שומן—כדורים קטנים מלאי שומן בתוך התא ששכיחים במיוחד בסוג זה של סרטן כליה. הצבירה הזו הייתה תלויה בציר mTOR–HIF2α וב‑PLIN2, חלבון מצפה הטיפות שהרמות שלו עלו כאשר PCDHGC3 דוכא. הטיפות האלו עשו יותר מאשר לאחסן שומן עודף: הן עזרו לתאים להימלט מפרורפטוזיס, צורת מוות תאי המונעת על ידי ברזל וליפידים פגועים. כאשר PLIN2 הוקטן, במיוחד בתאים שכבר חסרו PCDHGC3, הטיפות הצטמצמו והתאים הפכו לרגישים הרבה יותר לתרופה שמגרה פרורפטוזיס.
הפיכת פטנט הישרדות של הגידול לחולשה שלו
ביחד, המחקר חושף שרשרת אירועים שבה אובדן PCDHGC3 במשטח התא מפעיל את focal adhesion kinase, מפעיל את mTOR ו‑HIF2α, ממריץ סינתזת שומנים ובונה טיפות שומן מגוננות המצופות ב‑PLIN2. רשת זו לא רק מזינה את צמיחת הגידול והתפשטותו, אלא גם מאפשרת לתאי הסרטן להסתיר שומנים פגיעים מפני תגובות הרסניות שהיו הורגות אותם אחרת. המחברים מציעים שמיקוד בציר החדש שהוגדר PCDHGC3–mTOR–HIF2α–PLIN2 עשוי להציע אסטרטגיה רב‑נוייתית לסרטן כליה של תאי צלולית מתקדם: שילוב מעכבי mTOR או HIF2α עם תרופות שמעוררות פרורפטוזיס, ועל ידי כך אולי חסימת PLIN2, עשוי להפוך את ההתאמה המטבולית של הגידול לעקב־אכילס שלו.
ציטוט: Celada, L., Cubiella, T., San-Juan-Guardado, J. et al. PCDHGC3 silencing promotes clear cell renal cell carcinoma metastasis via mTOR/HIF2α activation, lipid metabolism rewiring, and ferroptosis evasion. Cell Death Dis 17, 409 (2026). https://doi.org/10.1038/s41419-026-08643-y
מילות מפתח: סרטן כליה של תאי צלולית, PCDHGC3, מסלול mTOR HIF2alpha, טיפות שומן, פרורפטוזיס