Clear Sky Science · nl
Silencing van PCDHGC3 bevordert metastase van clear cell niercelcarcinoom via activatie van mTOR/HIF2α, herprogrammering van lipidenmetabolisme en ontwijking van ferroptose
Waarom dit nierkankeronderzoek ertoe doet
Clear cell niercelcarcinoom is de meest voorkomende vorm van nierkanker en staat erom bekend dat het uitzaait naar andere organen en moeilijk te behandelen is. Deze studie onthult hoe het verlies van een enkel celmembraaneiwit, PCDHGC3, niertumoren helpt groeien, uitzaaien en ontsnappen aan een vorm van celdood die samenhangt met lipideschade. Door de keten van gebeurtenissen te volgen van het celmembraan tot hoe kankercellen vetten verwerken, wijzen de bevindingen op nieuwe combinatietherapieën die gevorderde nierkankers kwetsbaarder voor behandeling zouden kunnen maken.
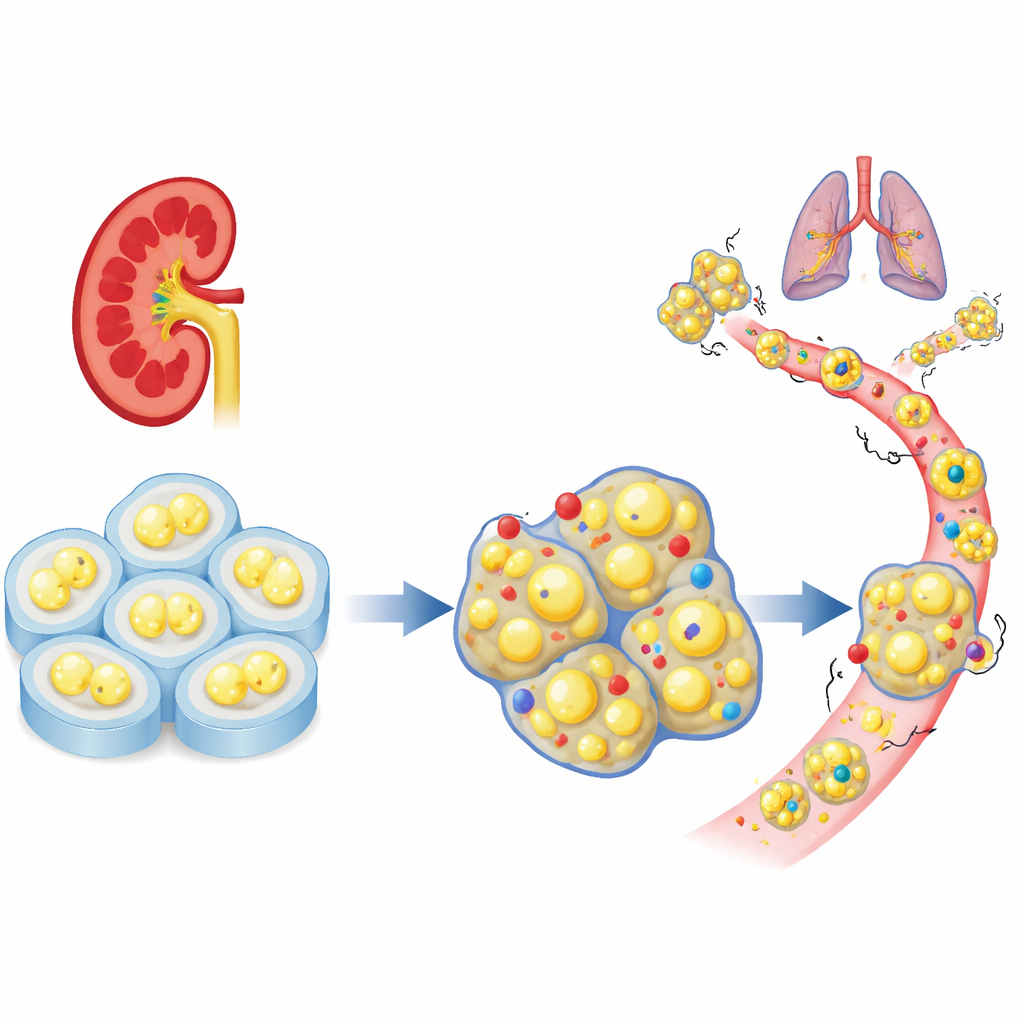
Een ontbrekende cellulaire "rem" in niertumoren
De onderzoekers begonnen met het analyseren van grote patiëntendatasets om te zien hoe een familie van celadhesiegenen zich gedraagt in clear cell nierkanker. Uit tientallen verwante genen bleek PCDHGC3 op te vallen: het was relatief actief in normaal weefsel maar verminderd in agressieve tumoren. Patiënten met tumoren die lage niveaus van dit gen hadden, hadden vaker gevorderde ziekte en een kortere overleving. In tegenstelling tot veel verwanten werd PCDHGC3 niet simpelweg uitgeschakeld door sterke chemische bepaling van het DNA (methylatie), wat suggereert dat het op een andere manier gereguleerd wordt en mogelijk een unieke beschermende rol in niercellen speelt.
Van langzaam groeiende naar invasieve kankercellen
Om te onderzoeken wat PCDHGC3 daadwerkelijk doet, verlaagde het team de expressie ervan in twee humane nierkankercellijnen en vergeleek deze met controlecellen. Toen dit gen werd stilgelegd, deelden de cellen sneller, doorliepen ze de celcyclus vlotter en overtroffen ze normale tegenhangers die in dezelfde kweekschaal werden gekweekt. In 3D-bioprintmodellen die beter echt weefsel nabootsen, vormden PCDHGC3‑deficiënte cellen grotere, dichtere structuren. In muismodellen groeiden tumoren zonder dit gen meer dan vier keer zo groot en vertoonden ze meer actief delende cellen. Deze gewijzigde cellen maakten ook de overgang van een compacte, epitheliale vorm naar een meer flexibele, migrerende morfologie die geassocieerd is met invasie, en ze vormden makkelijker verre metastasen nadat ze in de bloedbaan werden geïnjecteerd.
Een groeipad dat in overdrive schiet
Bij het onderzoeken van de signaalmechanismen vonden de onderzoekers dat het verlies van PCDHGC3 een bekende groeiregelaar in cellen activeert, mTOR, samen met verwante eiwitten die eiwitsynthese en overleving stimuleren. Een belangrijke adhesiekinase aan het celoppervlak, focal adhesion kinase, werd ook actiever, waardoor veranderingen aan het membraan gekoppeld werden aan deze interne groeischakelaar. Een bijzonder belangrijk gevolg was de abnormale ophoping van een factor genaamd HIF2α, die helpt tumorcellen aan lage zuurstofcondities aan te passen, bloedvatvorming te ondersteunen en hun metabolisme te veranderen. Middelen die mTOR of HIF2α blokkeren, remden elk de overgroei van PCDHGC3‑deficiënte cellen, zowel in platte kweek als in 3D‑modellen, en verminderden ook metastatische tumoren in een in-de-nier muismodel, wat suggereert dat deze route centraal staat voor het agressieve gedrag.
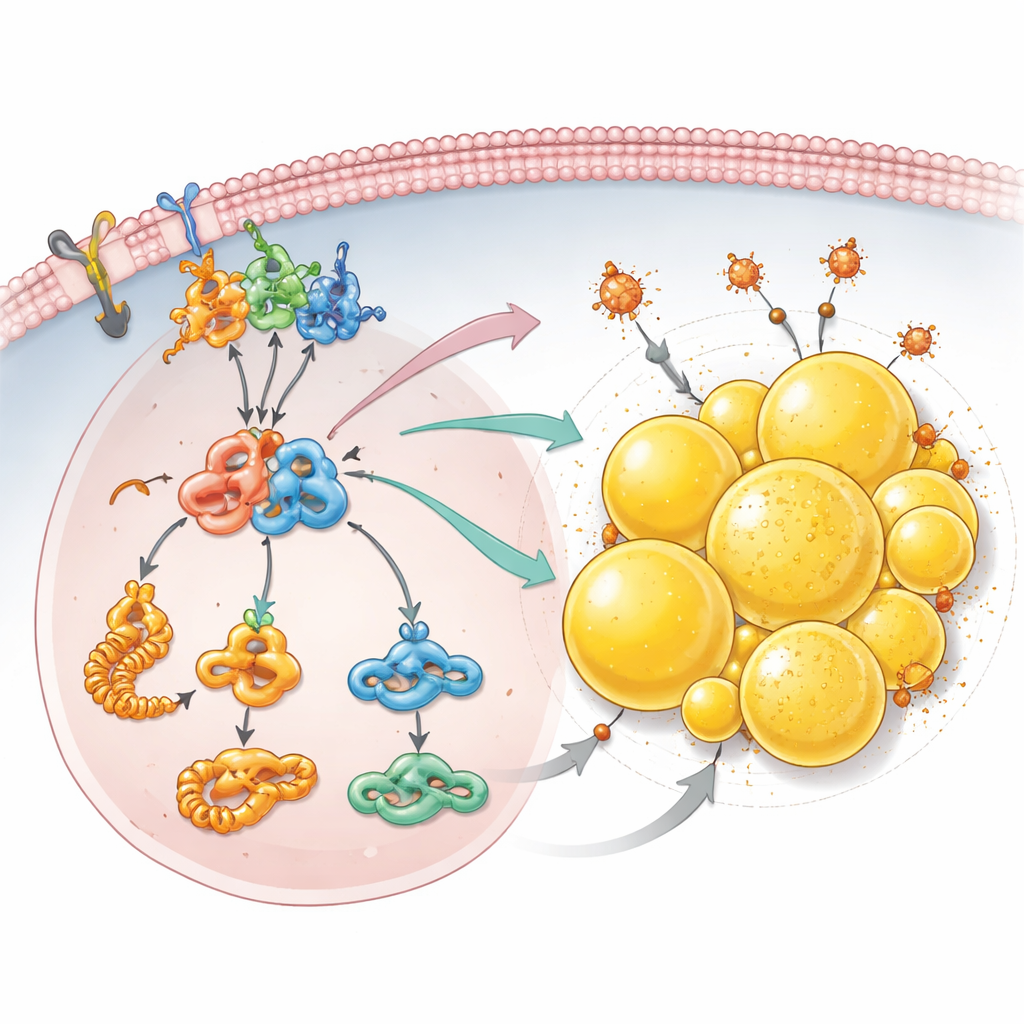
Vetopslag als schild tegen celdood
Buiten groeisignalen ontdekte het team dat het verlies van PCDHGC3 herprogrammering veroorzaakt in hoe kankercellen met vetten omgaan. Gedetailleerde eiwitanalyses toonden een verhoogde productie van bouwstenen voor vetzuren en hogere niveaus van acetyl‑CoA, een centraal brandstofmolecuul voor lipidesynthese. Cellen zonder PCDHGC3 bouwden veel meer lipidedruppels op — kleine vetgevulde bolletjes in de cel die bijzonder overvloedig zijn in dit type nierkanker. Deze ophoping was afhankelijk van de mTOR–HIF2α‑as en van PLIN2, een druppel‑omhullend eiwit waarvan de niveaus stegen wanneer PCDHGC3 werd uitgeschakeld. Deze druppels deden meer dan alleen overtollig vet opslaan: ze hielpen de cellen te ontsnappen aan ferroptose, een vorm van celdood aangedreven door ijzer en beschadigde lipiden. Wanneer PLIN2 werd verminderd, vooral in cellen die al PCDHGC3 misten, slonk het aantal lipidedruppels en werden de cellen veel gevoeliger voor een middel dat ferroptose induceert.
Een overlevingstruc van de tumor in een zwakte veranderen
Alles bij elkaar onthult de studie een keten van gebeurtenissen waarbij verlies van PCDHGC3 aan het celoppervlak focal adhesion kinase activeert, mTOR en HIF2α inschakelt, vetsynthese verhoogt en beschermende lipidedruppels opbouwt die door PLIN2 worden omhuld. Dit netwerk voedt niet alleen tumorgroei en -uitzaaiing, maar stelt kankercellen ook in staat kwetsbare vetten weg te stoppen van destructieve reacties die hen anders zouden doden. De auteurs stellen voor dat het richten op deze nieuw gedefinieerde PCDHGC3–mTOR–HIF2α–PLIN2‑as een meervoudige strategie kan bieden voor gevorderd clear cell niercelcarcinoom: het combineren van mTOR‑ of HIF2α‑remmers met middelen die ferroptose induceren, en mogelijk het blokkeren van PLIN2, kan de metabole aanpassing van de tumor in een achillespees veranderen.
Bronvermelding: Celada, L., Cubiella, T., San-Juan-Guardado, J. et al. PCDHGC3 silencing promotes clear cell renal cell carcinoma metastasis via mTOR/HIF2α activation, lipid metabolism rewiring, and ferroptosis evasion. Cell Death Dis 17, 409 (2026). https://doi.org/10.1038/s41419-026-08643-y
Trefwoorden: clear cell niercelcarcinoom, PCDHGC3, mTOR HIF2alpha-route, lipidedruppels, ferroptose