Clear Sky Science · ru
Ингибиция PCDHGC3 способствует метастазированию светлоклеточного почечно-клеточного рака через активацию mTOR/HIF2α, перестройку липидного метаболизма и уклонение от ферроптоза
Почему это исследование рака почки важно
Светлоклеточный почечно-клеточный рак — наиболее распространённая форма рака почки, известная своей склонностью к метастазированию и устойчивостью к лечению. В этом исследовании показано, как утрата одного белка на поверхности клетки, названного PCDHGC3, помогает опухолям почки расти, распространяться и избегать формы гибели клеток, связанной с повреждением липидов. Проследив эту цепочку событий от мембраны клетки до того, как раковые клетки обращаются с жирами, работа указывает на новые комбинированные терапевтические подходы, которые могут сделать запущенные раки почки более уязвимыми для лечения.
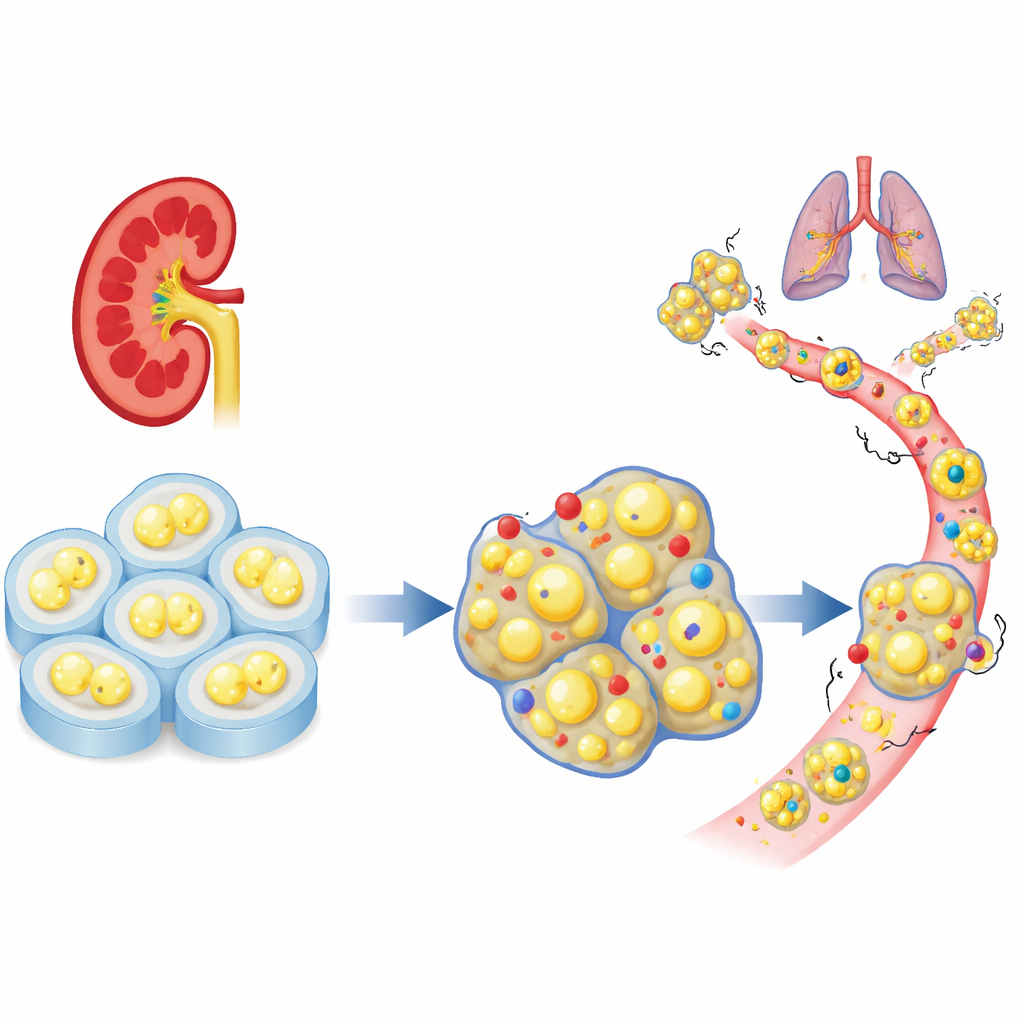
Отсутствие «тормоза» на поверхности клеток в опухолях почки
Исследователи начали с анализа больших наборов данных пациентов, чтобы выяснить, как ведёт себя семья генов адгезии клеток в светлоклеточном раке почки. Среди десятков родственных генов PCDHGC3 выделялся тем, что в нормальной ткани был заметно активен, а в агрессивных опухолях его экспрессия снижена. У пациентов с низким уровнем этого гена опухоли чаще были в продвинутой стадии, и выживаемость была короче. В отличие от многих родственных генов, PCDHGC3 не выключался просто за счёт интенсивной химической метки ДНК, что указывает на его особый механизм регуляции и потенциально уникальную защитную роль в почечных клетках.
От медленно растущих клеток к инвазивным
Чтобы проверить функцию PCDHGC3, команда уменьшила его уровни в двух линиях человеческих клеток рака почки и сравнила их с контрольными клетками. При заглушении этого гена клетки делились быстрее, быстрее проходили клеточный цикл и превосходили нормальные аналоги в конкурентном росте в одной культуре. В 3D-биопечатных моделях опухоли, более приближённых к живой ткани, клетки без PCDHGC3 формировали более крупные и плотные структуры. У мышей опухоли, лишённые этого гена, вырастали более чем в четыре раза больше и содержали больше активно делящихся клеток. Эти изменённые клетки также переходили от компактной эпителиальной формы к более пластичной, миграционно-активной форме, связанной с инвазией, и с большей готовностью образовывали отдалённые метастазы после введения в кровоток.
Сигнальный путь переключился на повышенную активность
Изучая сигнальные механизмы, исследователи обнаружили, что утрата PCDHGC3 активирует известный контролёр роста внутри клетки — mTOR, а также связанные белки, стимулирующие синтез белка и выживание. Ключевой фермент адгезии на поверхности клетки, киназа фокальной адгезии, также стал более активен, связывая изменения на мембране с этим внутренним «включателем роста». Одним из особенно важных последствий оказалось аномальное накопление фактора HIF2α, который помогает опухолевым клеткам адаптироваться к низкому уровню кислорода, поддерживать ангиогенез и изменять метаболизм. Препараты, блокирующие mTOR или HIF2α, замедляли чрезмерный рост клеток, лишённых PCDHGC3, как в плоских культурах, так и в 3D-моделях, а также снижали образование метастатических опухолей в мышиной модели с имплантацией в почку, что указывает на центральную роль этого пути в агрессивном поведении.
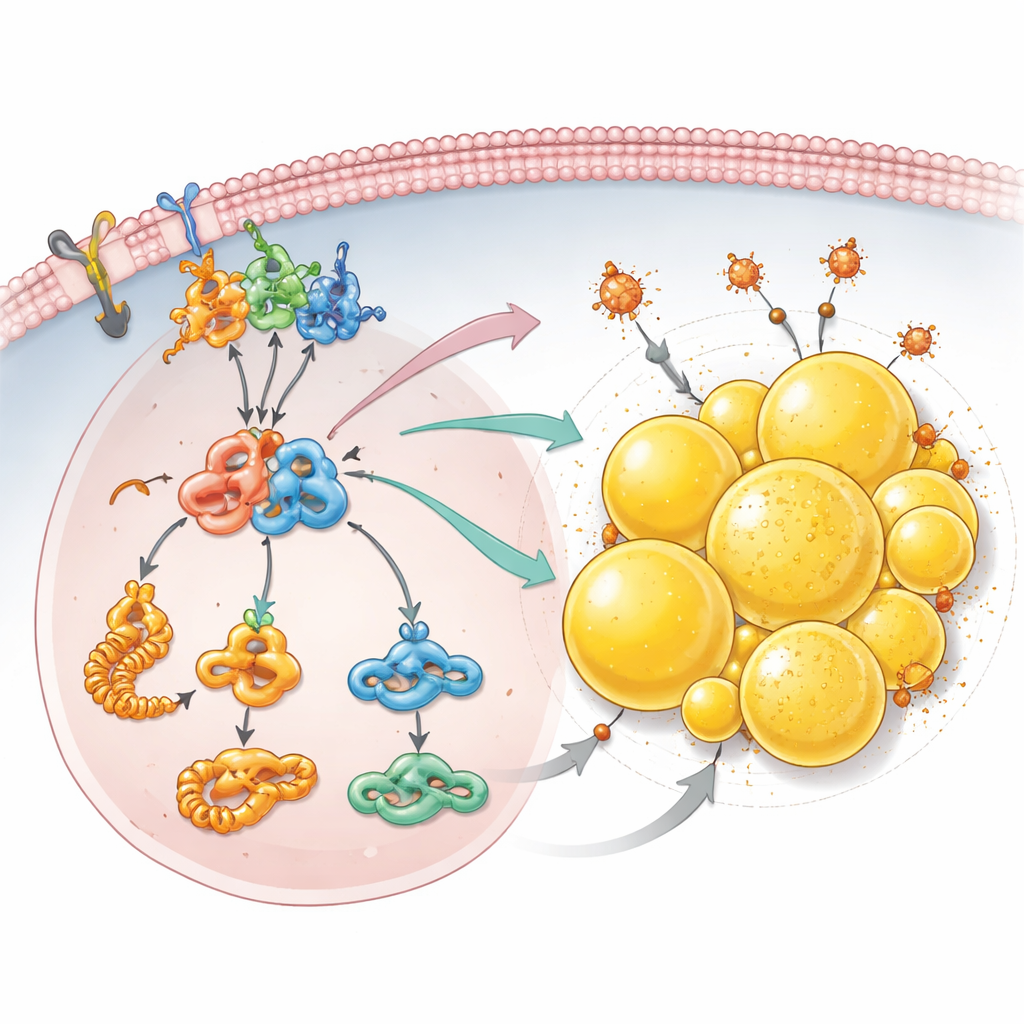
Запасание жира как щит от гибели клеток
Помимо сигналов роста, команда обнаружила, что утрата PCDHGC3 перестраивает обращение раковых клеток с жирами. Подробные протеомные исследования показали повышенное производство строительных блоков для жирных кислот и повышение уровня ацетил‑CoA — ключевого субстрата для синтеза липидов. Клетки без PCDHGC3 накапливали значительно больше липидных капель — маленьких наполненных жиром сфер внутри клетки, особенно характерных для этого типа рака почки. Это накопление зависело от оси mTOR–HIF2α и от PLIN2, белка, покрывающего капли, уровень которого повышался при подавлении PCDHGC3. Эти капли выполняли не только функцию хранения избыточного жира: они помогали клеткам избегать ферроптоза — формы гибели клеток, вызванной железом и повреждёнными липидами. При снижении PLIN2, особенно в клетках, уже лишённых PCDHGC3, липидные капли уменьшались, и клетки становились значительно более чувствительны к лекарству, вызывающему ферроптоз.
Преобразование трюка выживания опухоли в её слабость
В сумме исследование выявляет цепочку событий, в которой потеря PCDHGC3 на поверхности клетки активирует киназу фокальной адгезии, включает mTOR и HIF2α, усиливает синтез жиров и приводит к образованию защитных липидных капель, покрытых PLIN2. Эта сеть не только подпитывает рост и распространение опухоли, но и позволяет раковым клеткам прятать уязвимые липиды от реакций разрушения, которые в противном случае их уничтожили бы. Авторы предлагают, что нацеленность на новоопределённую ось PCDHGC3–mTOR–HIF2α–PLIN2 может обеспечить многогранную стратегию для лечения продвинутого светлоклеточного рака почки: сочетание ингибиторов mTOR или HIF2α с препаратами, индуцирующими ферроптоз, и потенциальная блокада PLIN2 могут превратить метаболическую адаптацию опухоли в её ахиллесову пяту.
Цитирование: Celada, L., Cubiella, T., San-Juan-Guardado, J. et al. PCDHGC3 silencing promotes clear cell renal cell carcinoma metastasis via mTOR/HIF2α activation, lipid metabolism rewiring, and ferroptosis evasion. Cell Death Dis 17, 409 (2026). https://doi.org/10.1038/s41419-026-08643-y
Ключевые слова: светлоклеточный почечно-клеточный рак, PCDHGC3, путь mTOR HIF2alpha, липидные капли, ферроптоз