Clear Sky Science · es
El silenciamiento de PCDHGC3 promueve la metástasis del carcinoma renal de células claras mediante la activación de mTOR/HIF2α, la reprogramación del metabolismo lipídico y la evasión de la ferroptosis
Por qué importa esta investigación sobre el cáncer renal
El carcinoma renal de células claras es la forma más común de cáncer de riñón y es conocido por su capacidad de diseminarse a otros órganos y por su resistencia a los tratamientos. Este estudio desvela cómo la pérdida de una sola proteína de superficie celular, denominada PCDHGC3, facilita que los tumores renales crezcan, se diseminen y eludan una forma de muerte celular relacionada con el daño lipídico. Al rastrear esta cadena de eventos desde la membrana celular hasta la forma en que las células cancerosas gestionan las grasas, el trabajo apunta a nuevas terapias combinadas que podrían hacer que los cánceres renales avanzados sean más vulnerables al tratamiento.
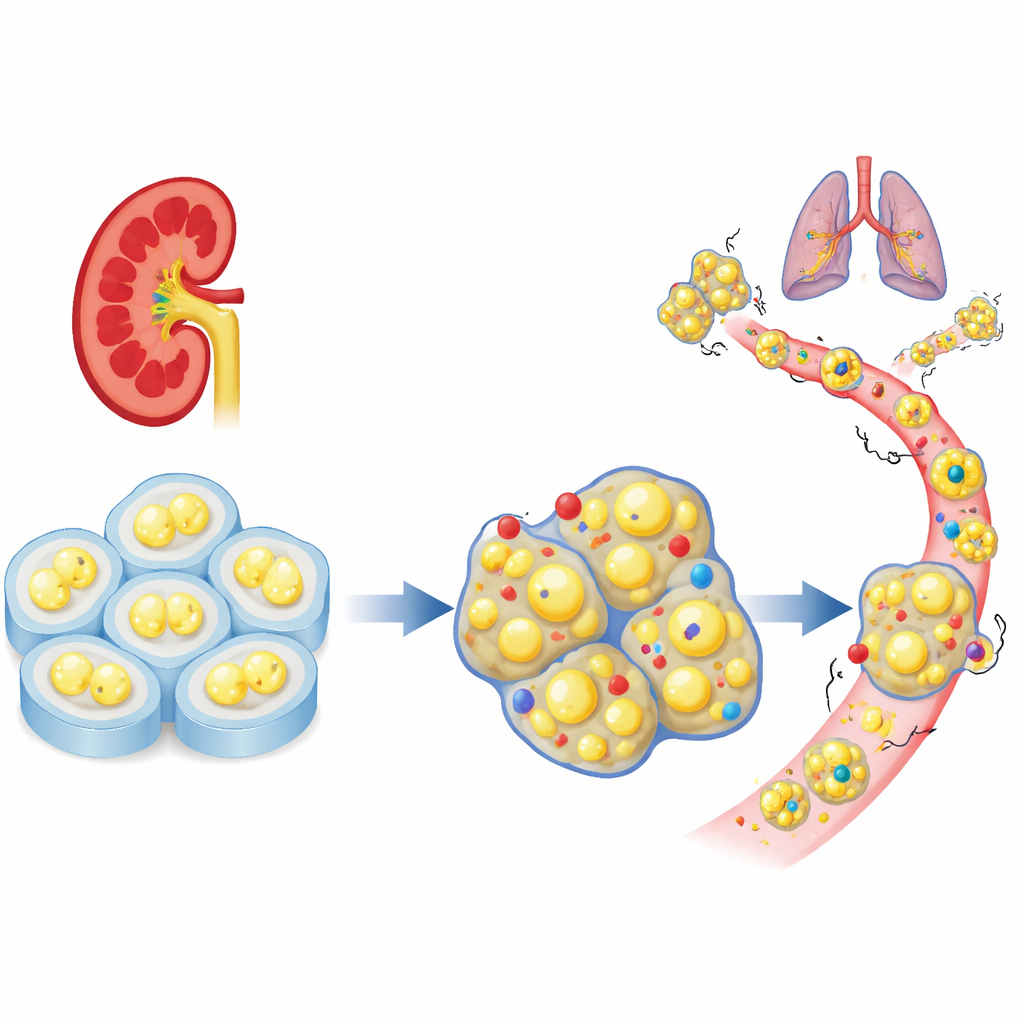
Un “freno” celular ausente en los tumores renales
Los investigadores comenzaron examinando grandes conjuntos de datos de pacientes para ver cómo se comporta una familia de genes de adhesión celular en el carcinoma renal de células claras. Entre docenas de genes relacionados, PCDHGC3 destacó por estar inusualmente activa en el tejido normal pero reducida en tumores agresivos. Los pacientes cuyos tumores tenían niveles bajos de este gen tendieron a presentar enfermedad más avanzada y una supervivencia más corta. A diferencia de muchos de sus parientes, PCDHGC3 no parece apagarse simplemente por una marcada metilación del ADN, lo que sugiere que se regula de forma distinta y que puede desempeñar un papel protector único en las células renales.
De células de crecimiento lento a invasivas
Para comprobar qué hace realmente PCDHGC3, el equipo redujo sus niveles en dos líneas celulares humanas de cáncer renal y las comparó con células control. Cuando se silenció este gen, las células se dividieron más rápido, avanzaron más deprisa a través del ciclo celular y superaron en competencia a las células normales cultivadas en el mismo plato. En modelos tumorales 3D bioprintados que imitan mejor el tejido real, las células deficientes en PCDHGC3 formaron estructuras más grandes y densas. En ratones, los tumores sin este gen crecieron más de cuatro veces y mostraron más células en división activa. Estas células alteradas también cambiaron de una morfología compacta y epitelial hacia una forma más flexible y migratoria asociada a la invasión, y con mayor facilidad formaron tumores distantes tras ser inyectadas en el torrente sanguíneo.
Una vía de crecimiento puesta a todo gas
Al profundizar en la maquinaria de señalización, los investigadores observaron que la pérdida de PCDHGC3 activa un conocido regulador de crecimiento dentro de las células llamado mTOR, junto con proteínas relacionadas que impulsan la síntesis proteica y la supervivencia. Una enzima de adhesión clave en la superficie celular, la quinasa de adhesión focal, también se volvió más activa, conectando los cambios en la membrana con este interruptor interno de crecimiento. Una consecuencia especialmente importante fue la acumulación anómala de un factor llamado HIF2α, que ayuda a las células tumorales a adaptarse a la baja disponibilidad de oxígeno, a promover el crecimiento vascular y a cambiar su metabolismo. Los fármacos que bloquean mTOR o HIF2α ralentizaron por separado la sobreexpansión de las células deficientes en PCDHGC3, tanto en cultivos planos como en modelos 3D, y también redujeron tumores metastásicos en un modelo de ratón con implante renal, lo que sugiere que esta vía es central en el comportamiento agresivo.
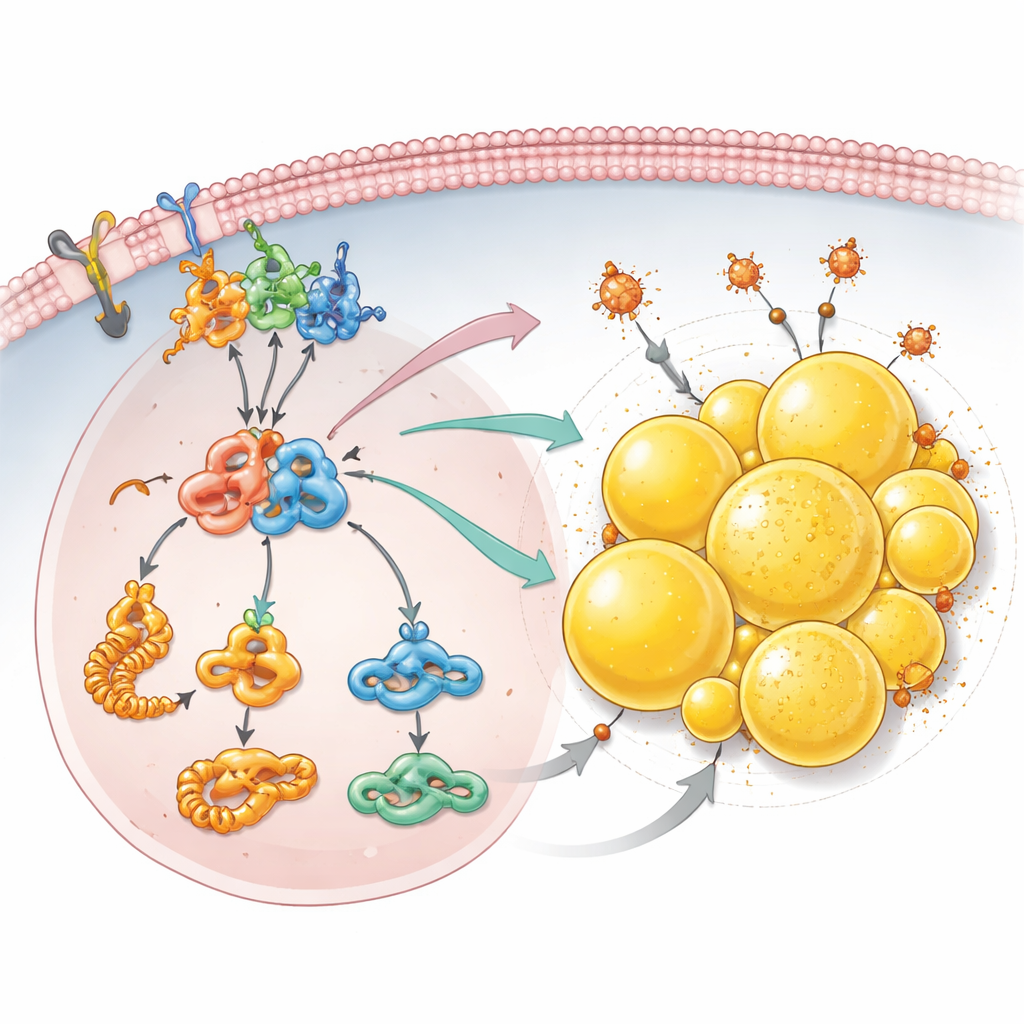
El almacenamiento de grasa como escudo contra la muerte celular
Más allá de las señales de crecimiento, el equipo descubrió que la pérdida de PCDHGC3 reprograma la forma en que las células cancerosas manejan las grasas. Estudios proteómicos detallados mostraron un aumento en la producción de bloques de construcción de ácidos grasos y niveles más altos de acetil-CoA, un combustible central para la síntesis lipídica. Las células carentes de PCDHGC3 acumularon muchas más gotas lipídicas —pequeñas esferas llenas de grasa dentro de la célula que son especialmente abundantes en este tipo de cáncer renal. Esta acumulación dependió del eje mTOR–HIF2α y de PLIN2, una proteína que recubre las gotas y cuyos niveles aumentaron cuando se silenció PCDHGC3. Estas gotas hicieron más que almacenar grasa en exceso: ayudaron a las células a escapar de la ferroptosis, una forma de muerte celular impulsada por el hierro y por lípidos dañados. Cuando se redujo PLIN2, especialmente en células ya carentes de PCDHGC3, las gotas lipídicas disminuyeron y las células se volvieron mucho más sensibles a un fármaco que induce ferroptosis.
Convirtiendo el truco de supervivencia del tumor en su debilidad
En conjunto, el estudio revela una cadena de eventos en la que la pérdida de PCDHGC3 en la superficie celular activa la quinasa de adhesión focal, enciende mTOR y HIF2α, aumenta la síntesis de grasas y genera gotas lipídicas protectoras recubiertas por PLIN2. Esta red no solo alimenta el crecimiento y la diseminación tumoral, sino que también permite a las células cancerosas esconder los lípidos vulnerables de reacciones destructivas que de otro modo las matarían. Los autores proponen que dirigirse a este recién definido eje PCDHGC3–mTOR–HIF2α–PLIN2 podría ofrecer una estrategia multifacética para el carcinoma renal de células claras avanzado: combinar inhibidores de mTOR o HIF2α con fármacos que induzcan ferroptosis, y potencialmente bloquear PLIN2, podría convertir la propia adaptación metabólica del tumor en un talón de Aquiles.
Cita: Celada, L., Cubiella, T., San-Juan-Guardado, J. et al. PCDHGC3 silencing promotes clear cell renal cell carcinoma metastasis via mTOR/HIF2α activation, lipid metabolism rewiring, and ferroptosis evasion. Cell Death Dis 17, 409 (2026). https://doi.org/10.1038/s41419-026-08643-y
Palabras clave: carcinoma renal de células claras, PCDHGC3, vía mTOR HIF2alfa, gotas lipídicas, ferroptosis