Clear Sky Science · pt
Silenciamento de PCDHGC3 promove metástase do carcinoma de células claras do rim via ativação de mTOR/HIF2α, reprogramação do metabolismo lipídico e evasão da ferroptose
Por que esta pesquisa sobre câncer renal importa
O carcinoma de células claras do rim é a forma mais comum de câncer renal e é notório por se espalhar para outros órgãos e resistir a tratamentos. Este estudo revela como a perda de uma única proteína de superfície celular, chamada PCDHGC3, ajuda tumores renais a crescer, metastizar e escapar de uma forma de morte celular ligada a danos lipídicos. Ao rastrear essa cadeia de eventos desde a membrana celular até o manejo dos lipídios pelas células cancerosas, o trabalho aponta para novas terapias combinadas que poderiam tornar cânceres renais avançados mais vulneráveis ao tratamento.
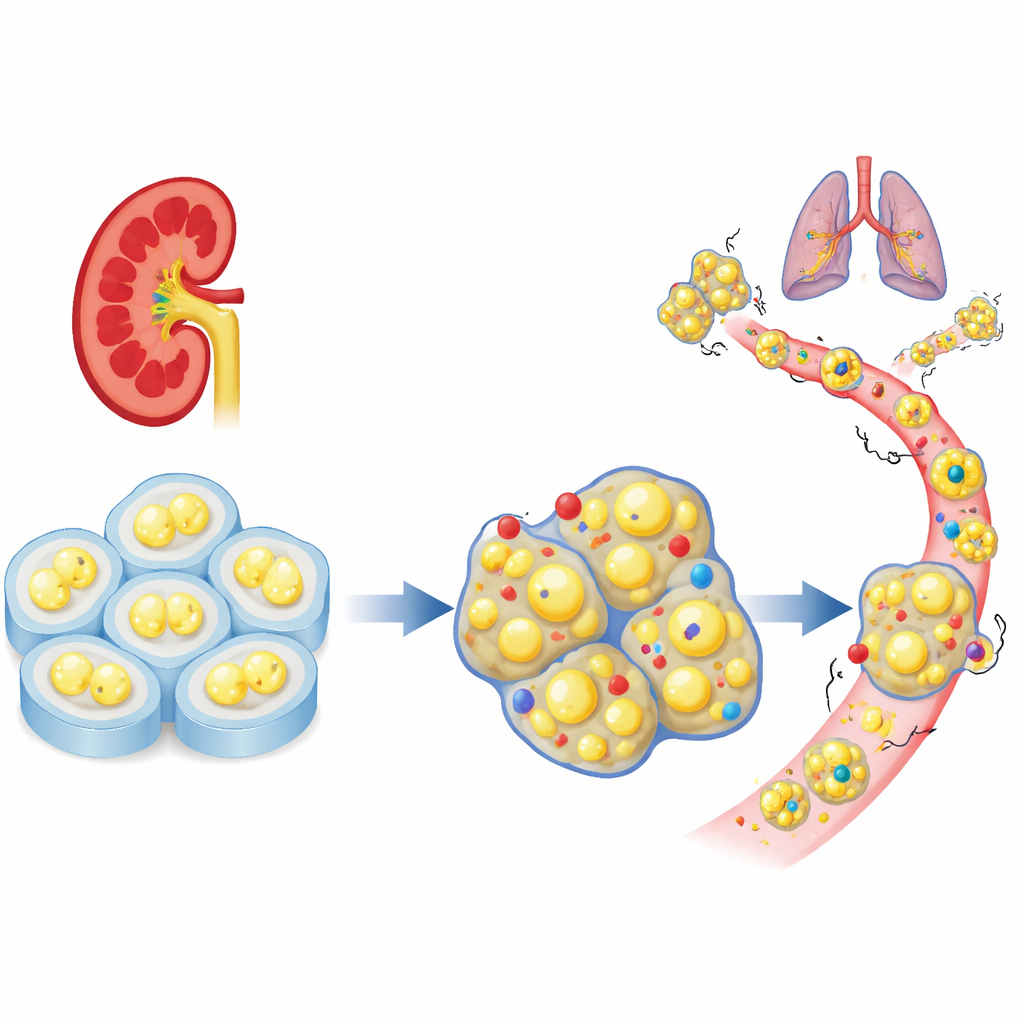
Um “freio” celular ausente em tumores renais
Os pesquisadores começaram analisando grandes conjuntos de dados de pacientes para ver como uma família de genes de adesão celular se comporta no carcinoma renal de células claras. Entre dezenas de genes relacionados, PCDHGC3 destacou-se por ser incomumente ativo em tecido normal, mas reduzido em tumores agressivos. Pacientes cujos tumores tinham baixos níveis desse gene apresentaram maior probabilidade de doença avançada e sobrevida mais curta. Ao contrário de muitos de seus parentes, PCDHGC3 não foi simplesmente desligado por marcação química intensa do DNA, o que sugere que é regulado de maneira distinta e pode desempenhar um papel protetor único nas células renais.
De células de crescimento lento para células invasivas
Para testar o que PCDHGC3 realmente faz, a equipe reduziu seus níveis em duas linhagens humanas de câncer renal e as comparou com células controle. Quando esse gene foi silenciado, as células dividiram-se mais rápido, avançaram pelo ciclo celular mais rapidamente e competiram melhor que as equivalentes normais cultivadas no mesmo prato. Em modelos tumorais 3D bioprintados que imitam melhor o tecido real, células deficientes em PCDHGC3 formaram estruturas maiores e mais densas. Em camundongos, tumores sem esse gene cresceram mais de quatro vezes e mostraram mais células em divisão ativa. Essas células alteradas também mudaram de uma forma epitelial compacta para uma forma mais flexível e migratória associada à invasão, e formaram com maior facilidade tumores distantes após serem injetadas na corrente sanguínea.
Uma via de crescimento acelerada
Ao investigar o maquinário de sinalização, os pesquisadores descobriram que a perda de PCDHGC3 ativa um controlador de crescimento bem conhecido dentro das células, chamado mTOR, juntamente com proteínas relacionadas que impulsionam a síntese proteica e a sobrevivência. Uma enzima de adesão chave na superfície celular, a quinase de adesão focal, também tornou-se mais ativa, ligando mudanças na membrana a esse interruptor interno de crescimento. Uma consequência particularmente importante foi o acúmulo anômalo de um fator chamado HIF2α, que ajuda células tumorais a se adaptarem a baixos níveis de oxigênio, a apoiar a formação de vasos sanguíneos e a alterar seu metabolismo. Drogas que bloqueiam mTOR ou HIF2α retardaram o crescimento excessivo de células deficientes em PCDHGC3, tanto em culturas planas quanto em modelos 3D, e também reduziram tumores metastáticos em um modelo de camundongo com implante renal, sugerindo que essa via é central para o comportamento agressivo.
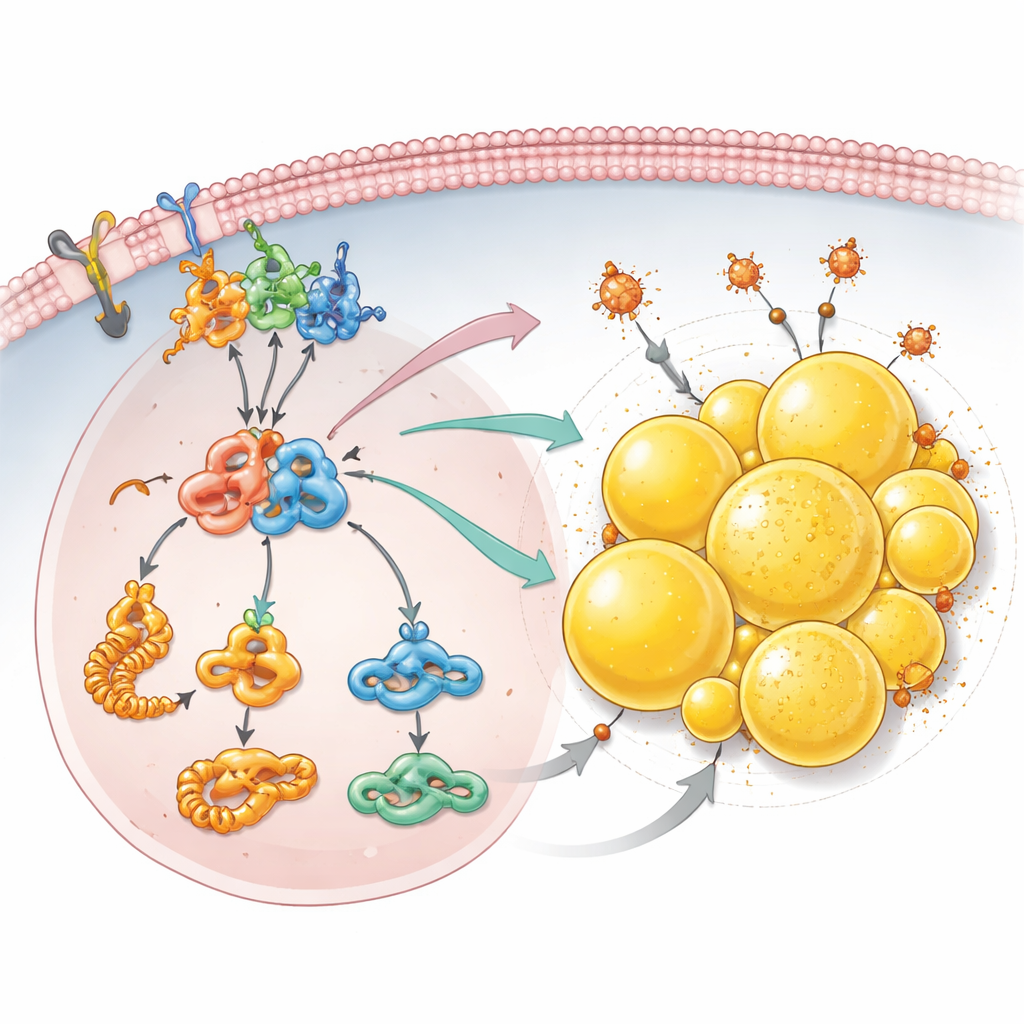
Armazenamento de gordura como escudo contra morte celular
Além dos sinais de crescimento, a equipe descobriu que a perda de PCDHGC3 reprograma a forma como as células cancerosas lidam com lipídios. Levantamentos detalhados de proteínas mostraram aumento na produção de blocos de construção para ácidos graxos e níveis mais altos de acetil-CoA, um combustível central usado para sintetizar lipídios. Células sem PCDHGC3 acumularam muitas mais gotículas lipídicas — pequenas esferas preenchidas por gordura dentro da célula que são especialmente abundantes neste tipo de câncer renal. Esse acúmulo dependia do eixo mTOR–HIF2α e da PLIN2, uma proteína que reveste as gotículas e cujos níveis aumentaram quando PCDHGC3 foi silenciado. Essas gotículas fizeram mais do que apenas armazenar gordura em excesso: ajudaram as células a escapar da ferroptose, uma forma de morte celular impulsionada por ferro e lipídios danificados. Quando a PLIN2 foi reduzida, especialmente em células já deficientes em PCDHGC3, as gotículas lipídicas diminuíram e as células ficaram muito mais sensíveis a um medicamento que induz a ferroptose.
Transformando a manobra de sobrevivência do tumor em sua fraqueza
Em conjunto, o estudo revela uma cadeia de eventos na qual a perda de PCDHGC3 na superfície celular ativa a quinase de adesão focal, liga mTOR e HIF2α, aumenta a síntese de lipídios e constrói gotículas protetoras revestidas por PLIN2. Essa rede não apenas alimenta o crescimento e a disseminação do tumor, mas também permite que as células cancerosas escondam lipídios vulneráveis de reações destrutivas que as matariam. Os autores propõem que mirar nesse eixo recém-definido PCDHGC3–mTOR–HIF2α–PLIN2 poderia oferecer uma estratégia multifacetada para o carcinoma de células claras avançado: combinar inibidores de mTOR ou HIF2α com drogas que induzem ferroptose, e potencialmente bloquear a PLIN2, pode transformar a adaptação metabólica do tumor em um calcanhar de Aquiles.
Citação: Celada, L., Cubiella, T., San-Juan-Guardado, J. et al. PCDHGC3 silencing promotes clear cell renal cell carcinoma metastasis via mTOR/HIF2α activation, lipid metabolism rewiring, and ferroptosis evasion. Cell Death Dis 17, 409 (2026). https://doi.org/10.1038/s41419-026-08643-y
Palavras-chave: carcinoma de células claras do rim, PCDHGC3, via mTOR HIF2alpha, gotículas lipídicas, ferroptose