Clear Sky Science · sv
Stumning av PCDHGC3 främjar metastasering vid klarcelligt njurcellscarcinom via aktivering av mTOR/HIF2α, omskrivning av lipidmetabolism och undvikande av ferroptos
Varför denna forskning om njurcancer är viktig
Klarcelligt njurcellscarcinom är den vanligaste formen av njurcancer och är ökänd för att sprida sig till andra organ och för att vara svårbehandlad. Denna studie avslöjar hur förlusten av ett enda cellmembranprotein, kallat PCDHGC3, hjälper njurtumörer att växa, sprida sig och undvika en form av celldöd som är kopplad till lipidskador. Genom att spåra denna händelsekedja från cellmembranet ner till hur cancerceller hanterar fetter pekar arbetet ut nya kombinationsbehandlingar som skulle kunna göra avancerade njurcancerformer mer sårbara för behandling.
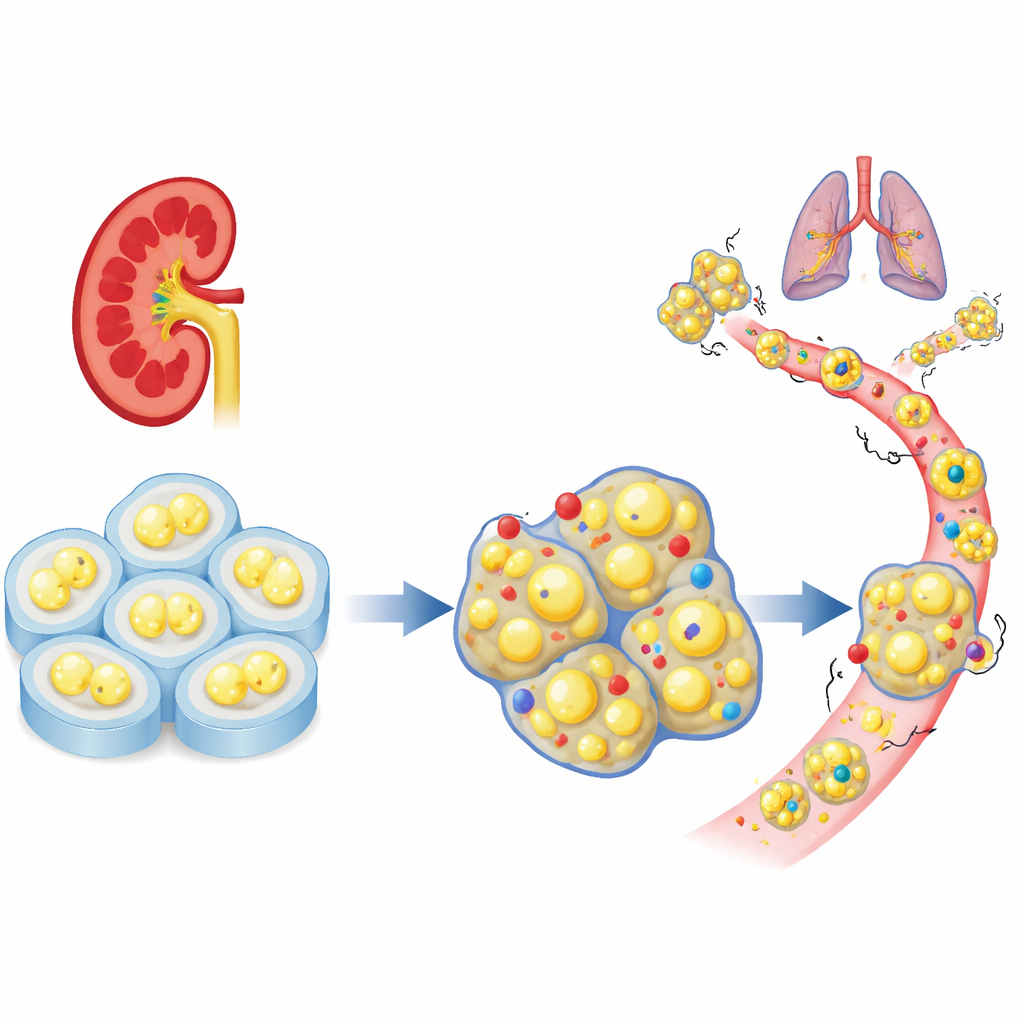
En saknad cellbroms i njurtumörer
Forskarna började med att analysera stora patientdatamängder för att se hur en familj av celladhesionsgener beter sig i klarcellig njurcancer. Bland flera dussin närbesläktade gener framstod PCDHGC3 som ovanligt aktiv i normalt vävnad men reducerad i aggressiva tumörer. Patienter vars tumörer hade låga nivåer av denna gen löpte större risk att ha avancerad sjukdom och kortare överlevnad. Till skillnad från många av sina släktingar slogs inte PCDHGC3 helt enkelt av genom omfattande kemisk märkning av dess DNA, vilket tyder på att den regleras på ett annat sätt och kan ha en unik skyddande roll i njurceller.
Från långsamt växande till invasiva cancerceller
För att testa vad PCDHGC3 faktiskt gör sänkte teamet dess nivåer i två mänskliga njurcancercellinjer och jämförde dem med kontrollceller. När denna gen tystades ned delade cellerna sig snabbare, rörde sig snabbare genom cellcykeln och konkurrerade ut normala motsvarigheter odlade i samma skål. I 3D-bioprintade tumörmodeller som bättre efterliknar verklig vävnad bildade PCDHGC3-bristande celler större, tätare strukturer. I möss växte tumörer utan denna gen till över fyra gånger större storlek och visade fler aktivt delande celler. Dessa förändrade celler skiftade också från en kompakt, epitelial form mot en mer flexibel, migratorisk form som förknippas med invasion, och de bildade lättare avlägsna tumörer efter att ha injicerats i blodomloppet.
En tillväxtväg växlas upp
När forskarna undersökte signalvägarna fann de att förlust av PCDHGC3 aktiverar en välkänd tillväxtregulator inne i cellerna kallad mTOR, tillsammans med relaterade proteiner som driver proteinsyntes och överlevnad. Ett nyckelenzym i adhesionskomplex vid cellytan, focal adhesion kinase, blev också mer aktivt, vilket kopplade förändringar i membranet till denna interna tillväxtbrytare. En särskilt viktig följd var den abnorma ansamlingen av en faktor kallad HIF2α, som hjälper tumörceller att anpassa sig till låg syrehalt, stödja blodkärlsbildning och ändra deras metabolism. Läkemedel som blockerar mTOR eller HIF2α bromsade vardera överväxten av PCDHGC3-defekta celler, både i platta kulturer och i 3D-modeller, och minskade även metastatiska tumörer i en njur-inbäddad musmodell, vilket tyder på att denna väg är central för det aggressiva beteendet.
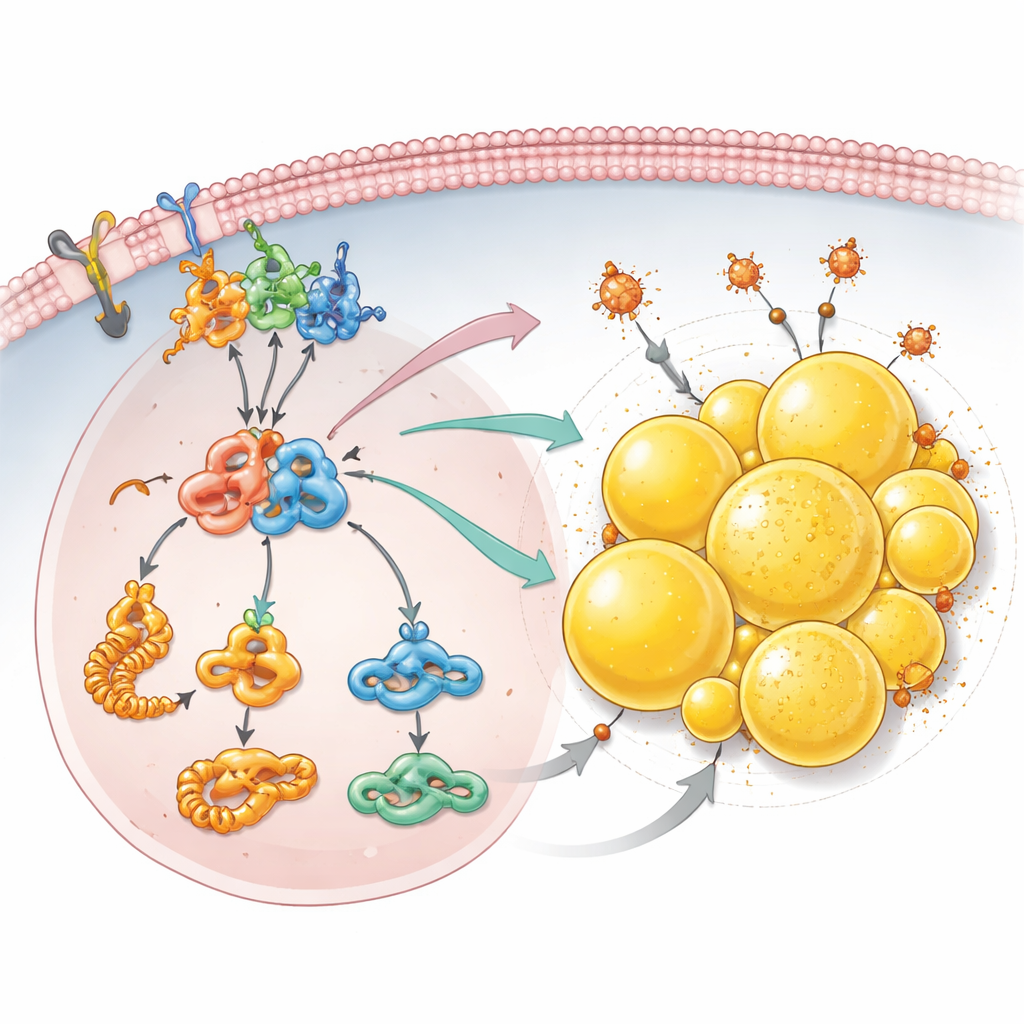
Fettlagring som sköld mot celldöd
Bortom tillväxtsignaler upptäckte teamet att förlust av PCDHGC3 omställer hur cancerceller hanterar fetter. Detaljerade proteinstudier visade ökad produktion av byggstenar för fettsyror och högre nivåer av acetyl-CoA, en central bränslekomponent som används för att skapa lipider. Celler utan PCDHGC3 byggde upp många fler lipiddroppar — små fettfyllda sfärer inuti cellen som är särskilt rikliga i denna typ av njurcancer. Denna ansamling berodde på mTOR–HIF2α-axeln och på PLIN2, ett droppskyddande protein vars nivåer steg när PCDHGC3 tystades. Dessa droppar gjorde mer än att bara lagra överskottsfett: de hjälpte cellerna att undkomma ferroptos, en form av celldöd driven av järn och skadade lipider. När PLIN2 reducerades, särskilt i celler som redan saknade PCDHGC3, krympte lipiddropparna och cellerna blev avsevärt mer känsliga för en substans som utlöser ferroptos.
Att göra tumörens överlevnadstrick till dess svaghet
Tillsammans visar studien en händelsekedja där förlust av PCDHGC3 vid cellytan aktiverar focal adhesion kinase, slår på mTOR och HIF2α, ökar fettsyntesen och bygger skyddande lipiddroppar täckta av PLIN2. Detta nätverk ger inte bara bränsle åt tumörtillväxt och spridning utan tillåter också cancerceller att dölja sårbara lipider från destruktiva reaktioner som annars skulle döda dem. Författarna föreslår att riktade angrepp mot denna nyligen definierade PCDHGC3–mTOR–HIF2α–PLIN2-axel kan erbjuda en flerdelad strategi för avancerad klarcellig njurcancer: att kombinera mTOR- eller HIF2α-hämmare med läkemedel som inducerar ferroptos, och eventuellt blockera PLIN2, kan förvandla tumörens egna metabola anpassning till en akilleshäl.
Citering: Celada, L., Cubiella, T., San-Juan-Guardado, J. et al. PCDHGC3 silencing promotes clear cell renal cell carcinoma metastasis via mTOR/HIF2α activation, lipid metabolism rewiring, and ferroptosis evasion. Cell Death Dis 17, 409 (2026). https://doi.org/10.1038/s41419-026-08643-y
Nyckelord: klarcelligt njurcellscarcinom, PCDHGC3, mTOR HIF2alpha-väg, lipiddroppar, ferroptos