Clear Sky Science · ar
كبت PCDHGC3 يعزز نقائل سرطان الخلايا الكلوية الصافية عبر تفعيل mTOR/HIF2α، إعادة برمجة استقلاب الدهون، وتفادي الفيروبتوز
لماذا يهم هذا البحث عن سرطان الكلى
سرطان الخلايا الكلوية الصافية هو الشكل الأكثر شيوعًا من سرطان الكلى ويشتهر بانتشاره إلى أعضاء أخرى ومقاومته للعلاج. تكشف هذه الدراسة كيف أن فقدان بروتين واحد على سطح الخلية، يُدعى PCDHGC3، يساعد الأورام الكلوية على النمو والانتشار وتجنب شكل من أشكال موت الخلية المرتبط بتلف الدهون. من خلال تتبع سلسلة الأحداث هذه من غشاء الخلية وصولًا إلى كيفية تعامل الخلايا السرطانية مع الدهون، يشير العمل إلى تراكيب علاجية جديدة قد تجعل سرطانات الكلى المتقدمة أكثر عرضة للعلاج.
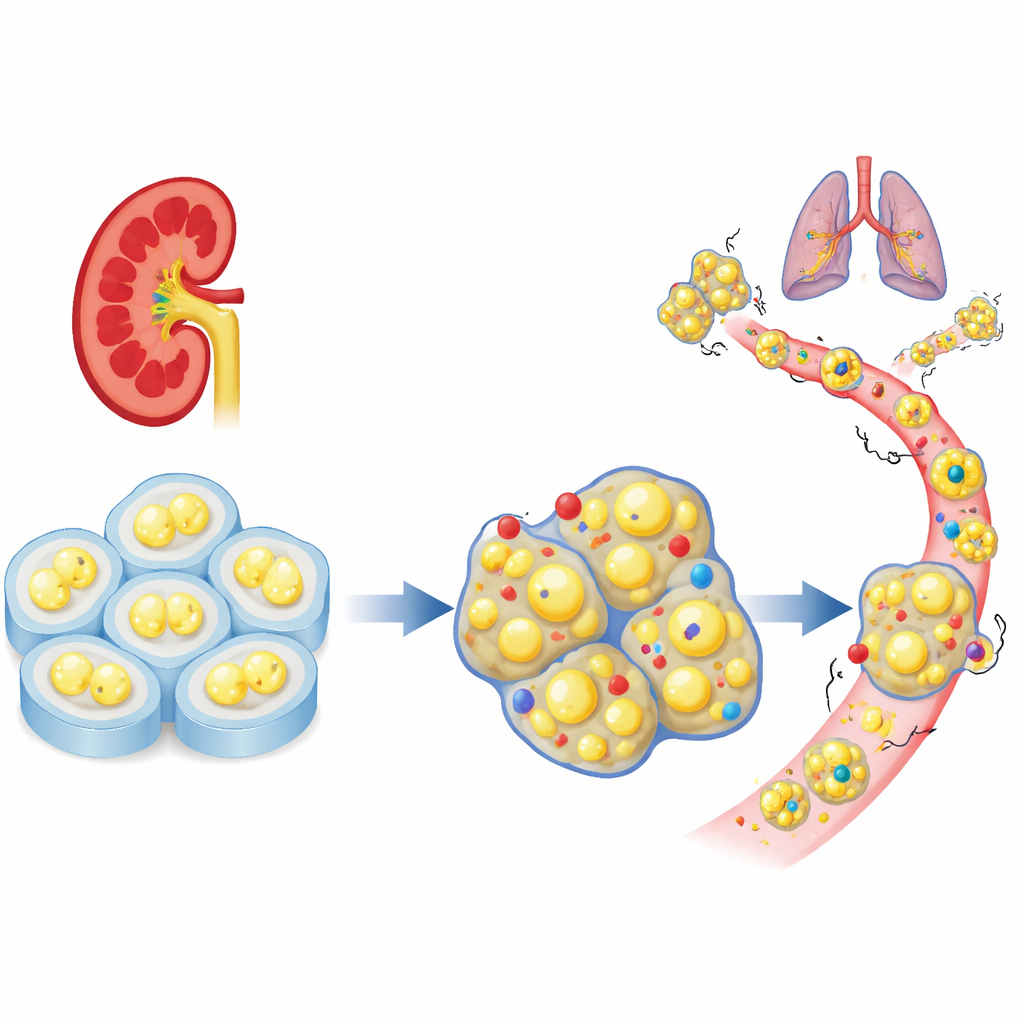
«مكبح» خِلوي مفقود في أورام الكلى
بدأ الباحثون بفحص مجموعات بيانات كبيرة للمرضى لرؤية كيف تتصرف عائلة جينات الالتصاق الخلوية في سرطان الكلى الصافي. من بين عشرات الجينات المرتبطة، برزت PCDHGC3 كنشاط غير عادي: نشطة في النسيج الطبيعي لكنها منخفضة في الأورام العدوانية. كان المرضى الذين تحتوي أورامهم على مستويات منخفضة من هذا الجين أكثر عرضة لمرض متقدم وبقصر في العمر. وعلى عكس العديد من أقاربها، لم تُلغَ PCDHGC3 ببساطة عن طريق علامات كيميائية كثيفة على الحمض النووي، مما يشير إلى أنها تُنظَّم بطريقة مميزة وقد تلعب دورًا وقائيًا فريدًا في خلايا الكلى.
من خلايا بطيئة النمو إلى خلايا غازية
لاختبار وظيفة PCDHGC3 فعليًا، خفّض الفريق مستواها في خطي خلايا سرطان كلوية بشريتين وقارنها بخلايا ضابطة. عندما تم إطفاء هذا الجين، انقسمت الخلايا أسرع، تقدمت عبر دورة الخلية بشكل أسرع، وتفوقت على النظائر الطبيعية المزروعة في نفس الصحفة. في نماذج أورام مطبوعة ثلاثية الأبعاد تحاكي الأنسجة الحقيقية بشكل أفضل، كوّنت الخلايا الناقصة PCDHGC3 هياكل أكبر وأكثر كثافة. في الفئران، نمت الأورام التي تفتقد هذا الجين أكثر من أربعة أضعاف وأظهرت خلايا أكثر نشاطًا في الانقسام. كما تحولت هذه الخلايا المعدلة من شكل ظهاري مدمج إلى شكل أكثر مرونة وهجرة مرتبطًا بالغزو، وشكّلت أورامًا بعيدة بسهولة أكبر بعد حقنها في مجرى الدم.
مسار نمو يتحول إلى تسارع مفرط
بالغوص في آليات الإشارة، وجد الباحثون أن فقدان PCDHGC3 ينشّط متحكم نمو معروف داخل الخلايا يسمى mTOR، إلى جانب بروتينات ذات صلة تدفع تخليق البروتين والبقاء. كما أصبح أحد إنزيمات الالتصاق السطحي، كيناز الالتصاق البؤري، أكثر نشاطًا، ليربط التغيرات عند الغشاء بهذا المُفَسِّر الداخلي للنمو. ومن بين النتائج المهمة تراكم غير طبيعي لعامل يُدعى HIF2α، الذي يساعد خلايا الورم على التكيف مع نقص الأكسجين، ودعم نمو الأوعية الدموية، وتغيير استقلابها. أبطأت الأدوية التي تمنع mTOR أو HIF2α فرط نمو الخلايا الناقصة PCDHGC3، سواء في المزروعات المسطحة أو في النماذج ثلاثية الأبعاد، وقلّلت أيضًا الأورام النقيلية في نموذج فأر بزراعة كلية، مما يشير إلى أن هذا المسار محوري للسلوك العدواني.
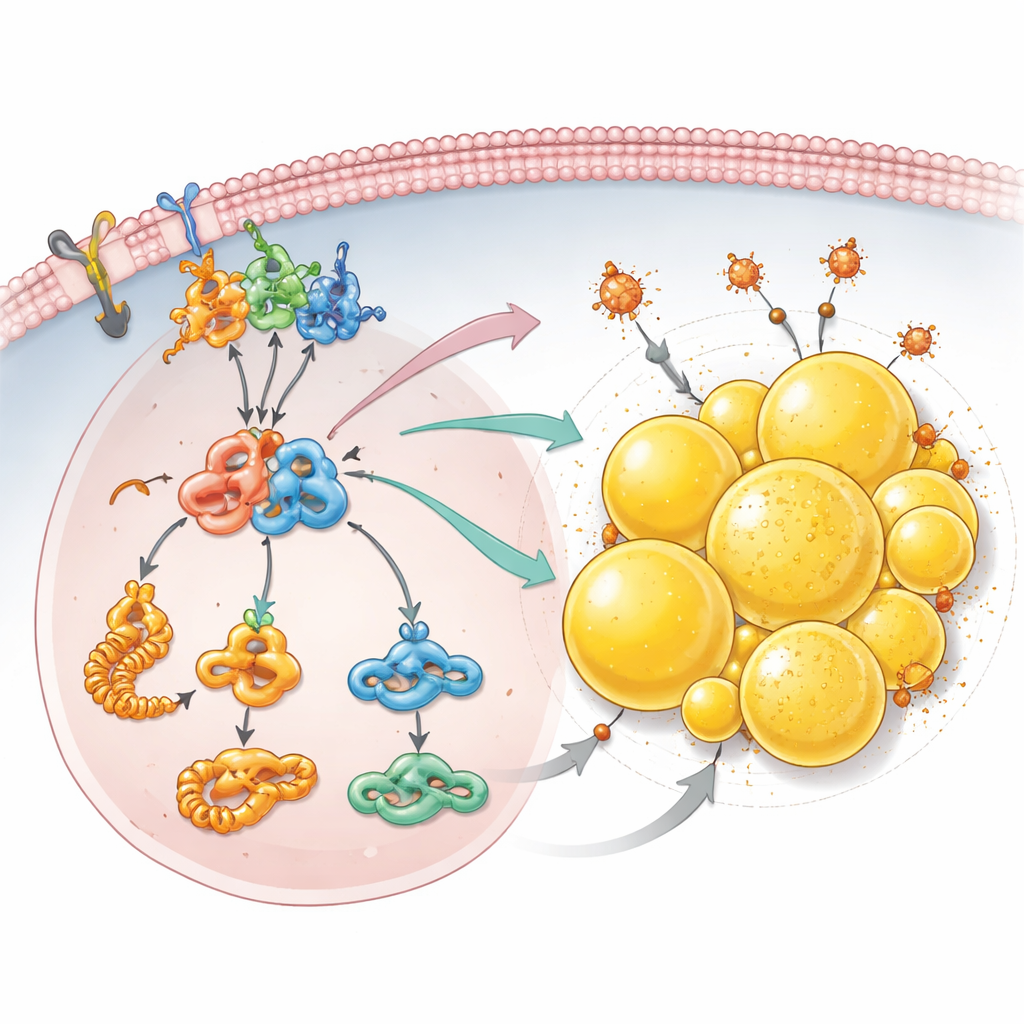
تخزين الدهون كدرع ضد موت الخلية
بعيدًا عن إشارات النمو، اكتشف الفريق أن فقدان PCDHGC3 يعيد برمجة طريقة تعامل الخلايا السرطانية مع الدهون. أظهرت دراسات بروتينية مفصلة زيادة إنتاج اللبنات الأساسية للأحماض الدهنية وارتفاع مستويات أسيتيل-كوإنزيم A، الوقود المركزي المستخدم لصنع الدهون. بنت الخلايا التي تفتقر إلى PCDHGC3 عددًا أكبر بكثير من القطرات الدهنية—كرات صغيرة مملوءة بالدهون داخل الخلية وهي وفيرة بشكل خاص في هذا النوع من سرطان الكلى. اعتمد هذا التجمع على محور mTOR–HIF2α وعلى PLIN2، بروتين يغلف القطرات ارتفع مستواه عند إطفاء PCDHGC3. لم تكن هذه القطرات مجرد مخزن للدهون الزائدة: فقد ساعدت الخلايا على الهروب من اليفروبتوز، وهو شكل من أشكال موت الخلية مدفوع بالحديد والدهون التالفة. عندما تم تقليل PLIN2، خاصة في الخلايا التي تفتقد بالفعل PCDHGC3، تقلصت القطرات الدهنية وأصبحت الخلايا أكثر حساسية بكثير لدواء يحفز اليفروبتوز.
تحويل حيلة بقاء الورم إلى نقطة ضعف
تجتمع النتائج لتكشف سلسلة أحداث حيث يؤدي فقدان PCDHGC3 على سطح الخلية إلى تنشيط كيناز الالتصاق البؤري، وتشغيل mTOR وHIF2α، وزيادة تخليق الدهون، وبناء قطرات دهنية واقية مغطاة بـPLIN2. هذه الشبكة لا تغذي نمو الورم وانتشاره فحسب، بل تُمكّن الخلايا السرطانية أيضًا من إخفاء الدهون الحساسة بعيدًا عن التفاعلات المدمرة التي كانت ستقضي عليها. يقترح المؤلفون أن استهداف هذا المحور المحدد حديثًا PCDHGC3–mTOR–HIF2α–PLIN2 قد يوفر استراتيجية متعددة الجوانب لسرطان الكلى الصافي المتقدم: الجمع بين مثبطات mTOR أو HIF2α مع أدوية تحفز اليفروبتوز، وربما حجب PLIN2، قد يحوّل تكيف الورم الأيضي ذاته إلى كعب أخيل.
الاستشهاد: Celada, L., Cubiella, T., San-Juan-Guardado, J. et al. PCDHGC3 silencing promotes clear cell renal cell carcinoma metastasis via mTOR/HIF2α activation, lipid metabolism rewiring, and ferroptosis evasion. Cell Death Dis 17, 409 (2026). https://doi.org/10.1038/s41419-026-08643-y
الكلمات المفتاحية: سرطان الخلايا الكلوية الصافية, PCDHGC3, مسار mTOR HIF2alpha, قطرات دهنية, اليفروبتوز