Clear Sky Science · tr
PCDHGC3 susturulması, mTOR/HIF2α aktivasyonu, lipid metabolizmasının yeniden programlanması ve ferroptozdan kaçınma yoluyla berrak hücreli böbrek hücreli karsinomun metastazını destekliyor
Bu böbrek kanseri araştırması neden önemli
Berrak hücreli böbrek hücreli karsinom, böbrek kanserinin en yaygın biçimidir ve sıklıkla diğer organlara yayılma ve tedaviye direnç gösterme ile bilinir. Bu çalışma, PCDHGC3 adlı tek bir hücre yüzeyi protein kaybının, böbrek tümörlerinin büyümesine, yayılmasına ve yağ hasarıyla bağlantılı bir hücre ölümü biçiminden kaçınmasına nasıl yardımcı olduğunu ortaya koyuyor. Hücre zarı seviyesinden kanser hücrelerinin yağları nasıl işlediğine kadar bu olay zincirini izleyerek, ileri evre böbrek kanserlerini tedaviye daha duyarlı hâle getirebilecek yeni kombinasyon tedavilerine işaret ediyor.
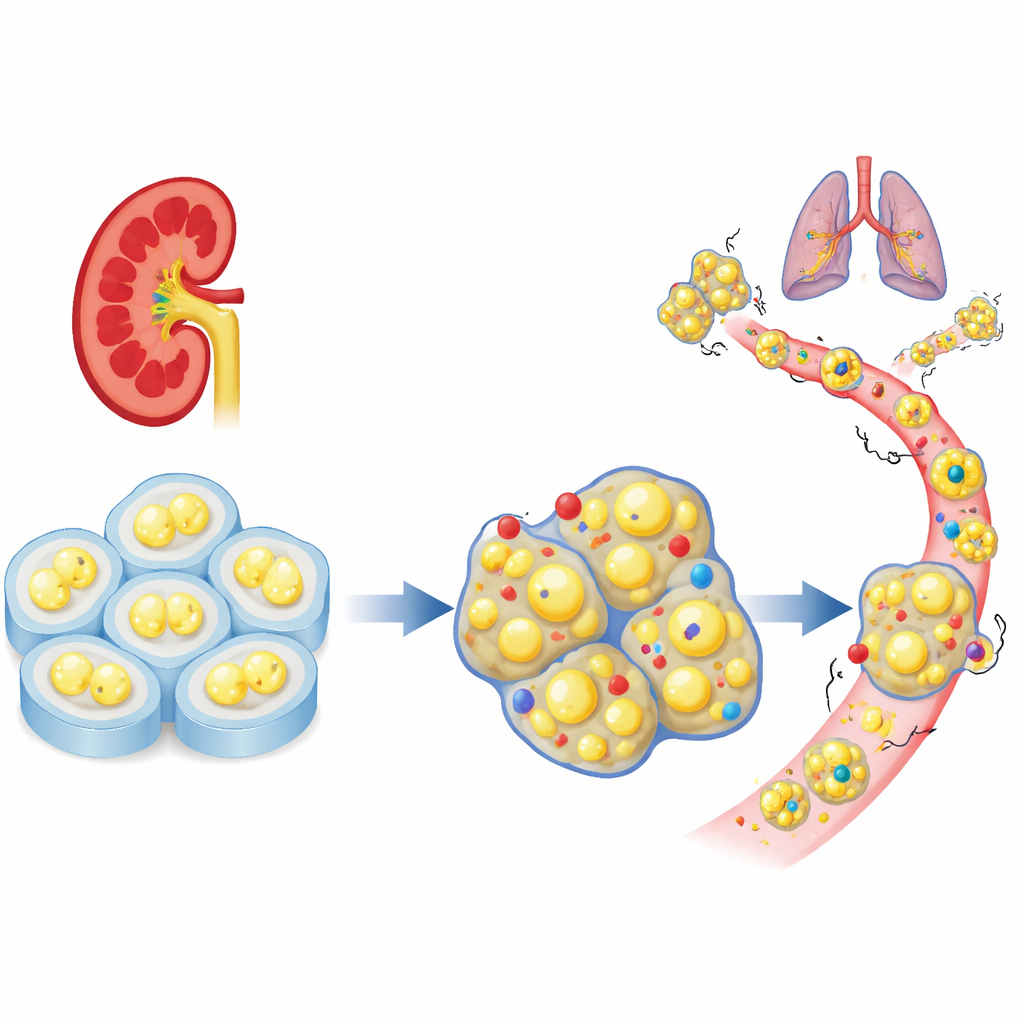
Böbrek tümörlerinde eksik bir hücre “freni”
Araştırmacılar, berrak hücreli böbrek kanserinde bir hücre-adezyon gen ailesinin nasıl davrandığını görmek için büyük hasta veri setlerine baktılar. Onlarca ilişkili gen arasından PCDHGC3, normal dokuda alışılmadık derecede yüksek etkinlik gösterirken agresif tümörlerde azalmış olmasıyla öne çıktı. Tümörlerinde bu genin düşük düzeyleri olan hastalarda hastalık daha ileri olma ve daha kısa sağkalım olasılığı daha yüksekti. Birçok akrabasının aksine, PCDHGC3 yalnızca DNA’nın yoğun kimyasal etiketlenmesiyle susturulmamış gibi görünüyordu; bu da onun farklı bir şekilde düzenlendiğini ve böbrek hücrelerinde benzersiz bir koruyucu rol oynayabileceğini düşündürüyor.
Yavaş büyüyen hücrelerden invazif kanser hücrelerine
PCDHGC3’ün gerçekten ne yaptığını test etmek için ekip, bu genin düzeylerini iki insan böbrek kanseri hücre hattında azalttı ve bunları kontrol hücreleriyle karşılaştırdı. Bu gen susturulduğunda, hücreler daha hızlı bölündü, hücre döngüsünden daha çabuk geçti ve aynı kültürde birlikte büyütülen normal karşıtlarını geride bıraktı. Gerçek dokuya daha iyi benzeyen 3B biyoyazdırılmış tümör modellerinde, PCDHGC3 eksikliği olan hücreler daha büyük ve daha yoğun yapılar oluşturdu. Farelerde bu geni kaybeden tümörler dört katı daha büyük büyüdü ve daha aktif bölünen hücreler gösterdi. Bu değişime uğramış hücreler ayrıca sıkı, epitelial biçimden daha esnek ve göçlü bir forma kaydı; bu form invazyonla ilişkilidir ve kan dolaşımına enjekte edildiklerinde uzak tümörler daha kolay oluşturdu.
Aşırı hızlanan bir büyüme yolu
Sinyal iletim mekanizmasına derinlemesine bakıldığında, araştırmacılar PCDHGC3 kaybının hücre içinde iyi bilinen bir büyüme kontrolörü olan mTOR’u ve protein sentezini ve hücre sağkalımını destekleyen ilgili proteinleri aktive ettiğini buldu. Hücre yüzeyinde bir adezyon enzimi olan fokal adezyon kinazı da daha aktif hale gelerek zar üzerindeki değişiklikleri bu iç büyüme anahtarına bağladı. Özellikle önemli bir sonuç, tümör hücrelerinin düşük oksijene uyum sağlamasına, damar büyümesini desteklemesine ve metabolizmasını değiştirmesine yardımcı olan HIF2α adlı faktörün anormal birikimiydi. mTOR veya HIF2α’yı bloke eden ilaçlar, hem düz kültürlerde hem de 3B modellerde PCDHGC3 eksik hücrelerin aşırı büyümesini yavaşlattı ve böbreğe yerleştirilmiş fare modelinde metastatik tümörleri azalttı; bu da bu yolun agresif davranışta merkezi olduğunu düşündürüyor.
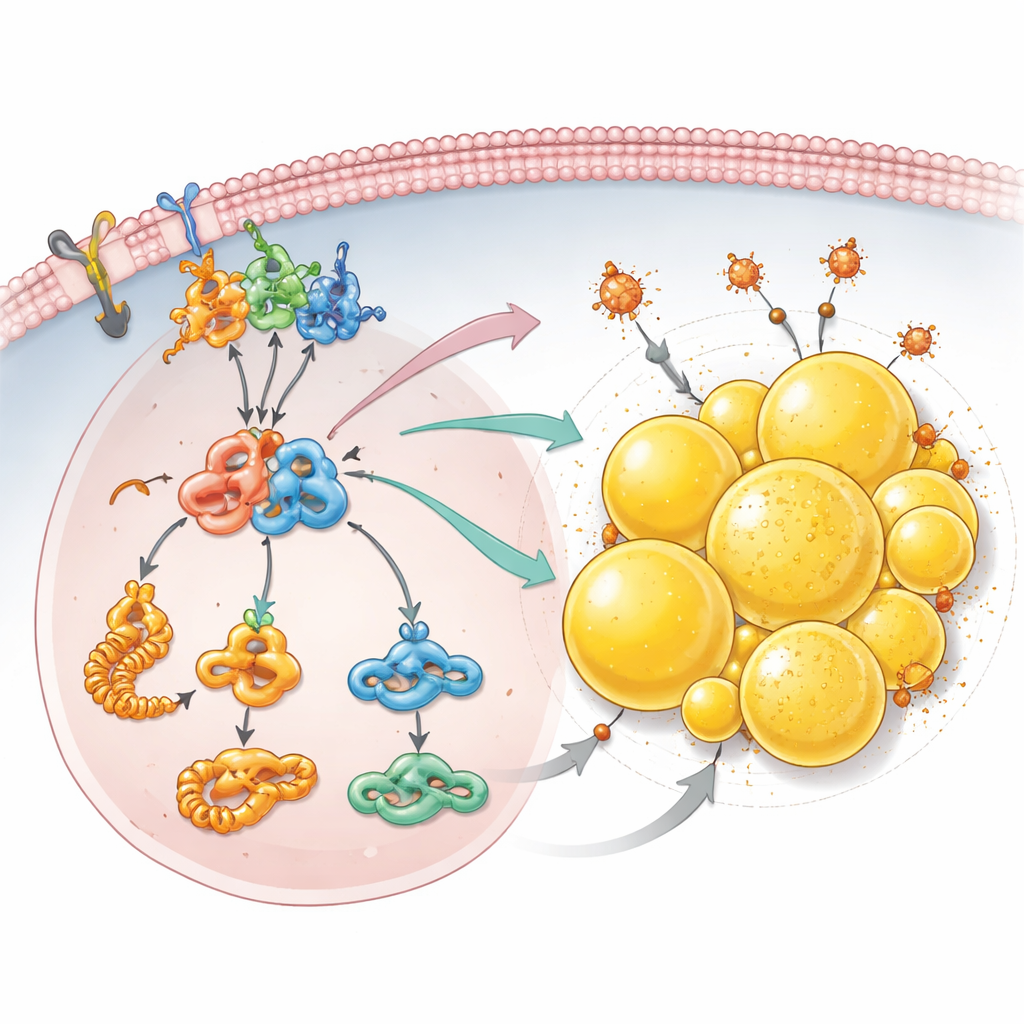
Hücre ölümüne karşı kalkan olarak yağ depolama
Büyüme sinyallerinin ötesinde, ekip PCDHGC3 kaybının kanser hücrelerinin yağlarla nasıl başa çıktığını yeniden programladığını keşfetti. Ayrıntılı protein incelemeleri, yağ asitleri için yapı taşlarının üretiminde artış ve lipit yapmak için kullanılan merkezi bir yakıt olan asetil-CoA düzeylerinde yükselme gösterdi. PCDHGC3 eksik hücreler, özellikle bu böbrek kanseri türünde bol bulunan hücre içi küçük yağ dolu kürecikler olan çok daha fazla lipid damlacığı biriktirdi. Bu birikim mTOR–HIF2α eksenine ve PCDHGC3 susturulduğunda düzeyi artan bir damlacık kaplama proteini olan PLIN2’ye bağlıydı. Bu damlacıklar sadece fazla yağı depolamakla kalmadı: aynı zamanda hücrelerin demir ve hasarlı lipidlerin yol açtığı bir hücre ölümü biçimi olan ferroptozdan kaçmalarına yardımcı oldular. Özellikle PCDHGC3 zaten eksikken PLIN2 azaltıldığında, lipid damlacıkları küçüldü ve hücreler ferroptozu tetikleyen bir ilaca karşı çok daha hassas hale geldi.
Tümörün hayatta kalma numarasını zayıflığa çevirme
Bir araya getirildiğinde, çalışma hücre yüzeyinde PCDHGC3 kaybının fokal adezyon kinazını aktive ettiği, mTOR ve HIF2α’yı açtığı, yağ sentezini artırdığı ve PLIN2 ile kaplanmış koruyucu lipid damlacıkları oluşturduğu bir olay zincirini ortaya koyuyor. Bu ağ yalnızca tümör büyümesini ve yayılmasını desteklemekle kalmıyor, aynı zamanda kanser hücrelerinin yok edici reaksiyonlardan zarar görebilecek yağları gizleyerek hayatta kalmalarına olanak tanıyor. Yazarlar, yeni tanımlanan PCDHGC3–mTOR–HIF2α–PLIN2 eksenini hedeflemenin ileri evre berrak hücreli böbrek kanseri için çok yönlü bir strateji sunabileceğini öne sürüyor: mTOR veya HIF2α inhibitörlerini ferroptozu indükleyen ilaçlarla kombin etmek ve potansiyel olarak PLIN2’yi engellemek, tümörün kendi metabolik adaptasyonunu bir Achilles tendonu hâline getirebilir.
Atıf: Celada, L., Cubiella, T., San-Juan-Guardado, J. et al. PCDHGC3 silencing promotes clear cell renal cell carcinoma metastasis via mTOR/HIF2α activation, lipid metabolism rewiring, and ferroptosis evasion. Cell Death Dis 17, 409 (2026). https://doi.org/10.1038/s41419-026-08643-y
Anahtar kelimeler: berrak hücreli böbrek hücreli karsinom, PCDHGC3, mTOR HIF2alfa yolu, lipid damlacıkları, ferroptoz