Clear Sky Science · it
La silenziamento di PCDHGC3 promuove la metastasi del carcinoma renale a cellule chiare tramite l’attivazione mTOR/HIF2α, il riprogrammamento del metabolismo lipidico e l’evasione della ferroptosi
Perché questa ricerca sul cancro renale è importante
Il carcinoma renale a cellule chiare è la forma più comune di cancro del rene ed è noto per la sua tendenza a diffondersi ad altri organi e a resistere alle terapie. Questo studio svela come la perdita di una singola proteina di superficie cellulare, chiamata PCDHGC3, favorisca la crescita, la diffusione e l’elusione di una forma di morte cellulare legata al danno lipidico. Tracciando questa catena di eventi dalla membrana cellulare fino al modo in cui le cellule tumorali gestiscono i lipidi, il lavoro indica nuove terapie combinate che potrebbero rendere i tumori renali avanzati più vulnerabili al trattamento.
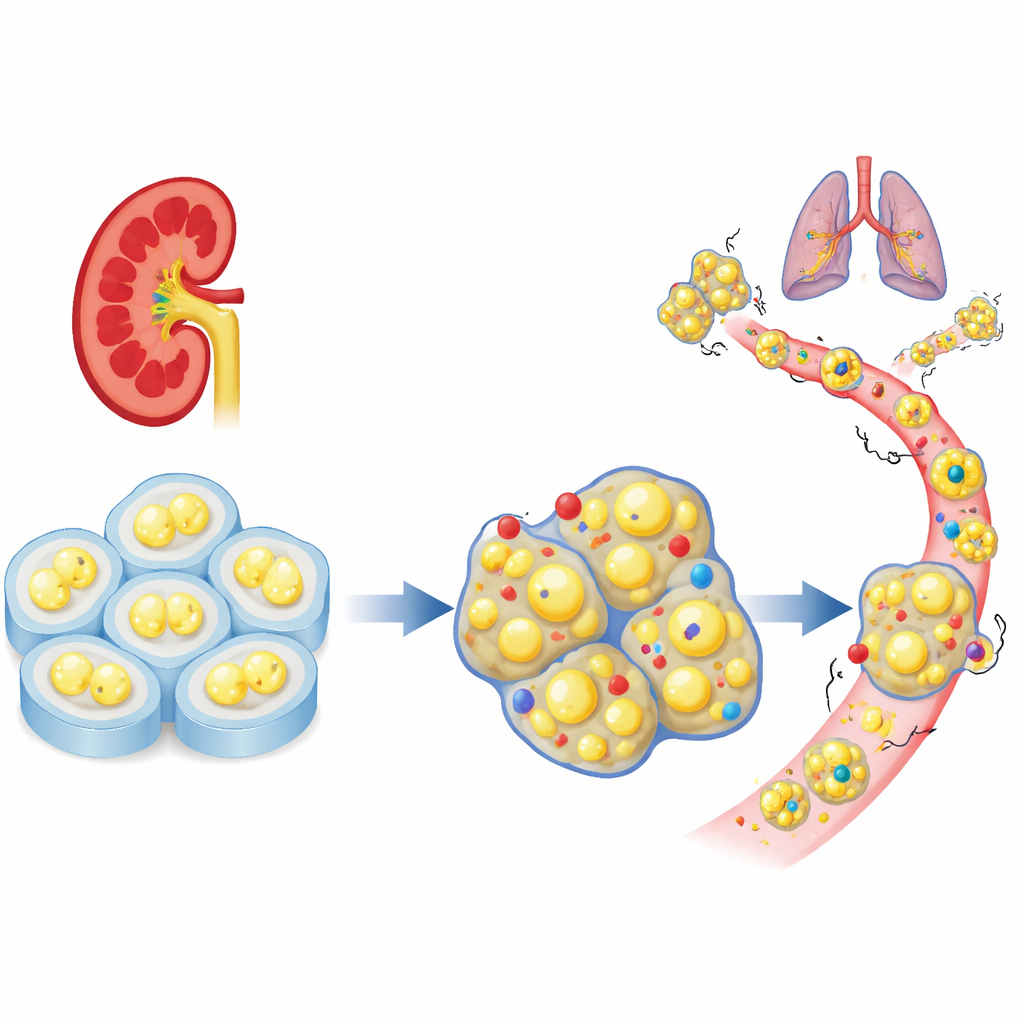
Un “freno” cellulare mancante nei tumori renali
I ricercatori hanno iniziato analizzando grandi set di dati di pazienti per verificare il comportamento di una famiglia di geni di adesione cellulare nel carcinoma renale a cellule chiare. Tra dozzine di geni correlati, PCDHGC3 è emerso come particolarmente attivo nei tessuti normali ma ridotto nei tumori aggressivi. I pazienti i cui tumori presentavano bassi livelli di questo gene avevano più probabilità di avere una malattia avanzata e una sopravvivenza più breve. Diversamente da molti suoi parenti, PCDHGC3 non risultava semplicemente spenta da marcature chimiche pesanti sul DNA, il che suggerisce che sia regolato in modo distinto e potrebbe svolgere un ruolo protettivo unico nelle cellule renali.
Da cellule a crescita lenta a cellule invasive
Per testare la funzione di PCDHGC3, il gruppo ha ridotto i suoi livelli in due linee cellulari umane di carcinoma renale e le ha confrontate con cellule di controllo. Quando questo gene è stato silenziato, le cellule si sono divise più rapidamente, hanno attraversato il ciclo cellulare in modo più veloce e hanno soppiantato le controparti normali coltivate nello stesso piatto. In modelli tumorali 3D biostampati che riproducono meglio il tessuto reale, le cellule carenti di PCDHGC3 hanno formato strutture più grandi e dense. Nei topi, i tumori privi di questo gene sono cresciuti oltre quattro volte di più e hanno mostrato un maggior numero di cellule in attiva divisione. Queste cellule modificate hanno anche mutato la loro morfologia da compatta ed epiteliale a una forma più flessibile e migratoria associata all’invasione, e hanno formato più facilmente tumori a distanza dopo l’iniezione nel circolo sanguigno.
Una via di crescita innestata in sovraattivazione
Esplorando la macchina dei segnali intracellulari, i ricercatori hanno scoperto che la perdita di PCDHGC3 attiva un noto controllore della crescita interno alle cellule chiamato mTOR, insieme a proteine correlate che guidano la sintesi proteica e la sopravvivenza. Anche una chinasi di adesione focale presente sulla superficie cellulare è diventata più attiva, collegando i cambiamenti di membrana a questo interruttore di crescita interno. Una conseguenza particolarmente importante è stato l’accumulo anomalo di un fattore chiamato HIF2α, che aiuta le cellule tumorali ad adattarsi a basse disponibilità di ossigeno, a sostenere la formazione di vasi sanguigni e a modificare il loro metabolismo. Farmaci che bloccano mTOR o HIF2α hanno rallentato la sovracrescita delle cellule carenti di PCDHGC3, sia in colture piane sia in modelli 3D, e hanno anche ridotto i tumori metastatici in un modello murino con innesto renale, suggerendo che questa via è centrale per il comportamento aggressivo.
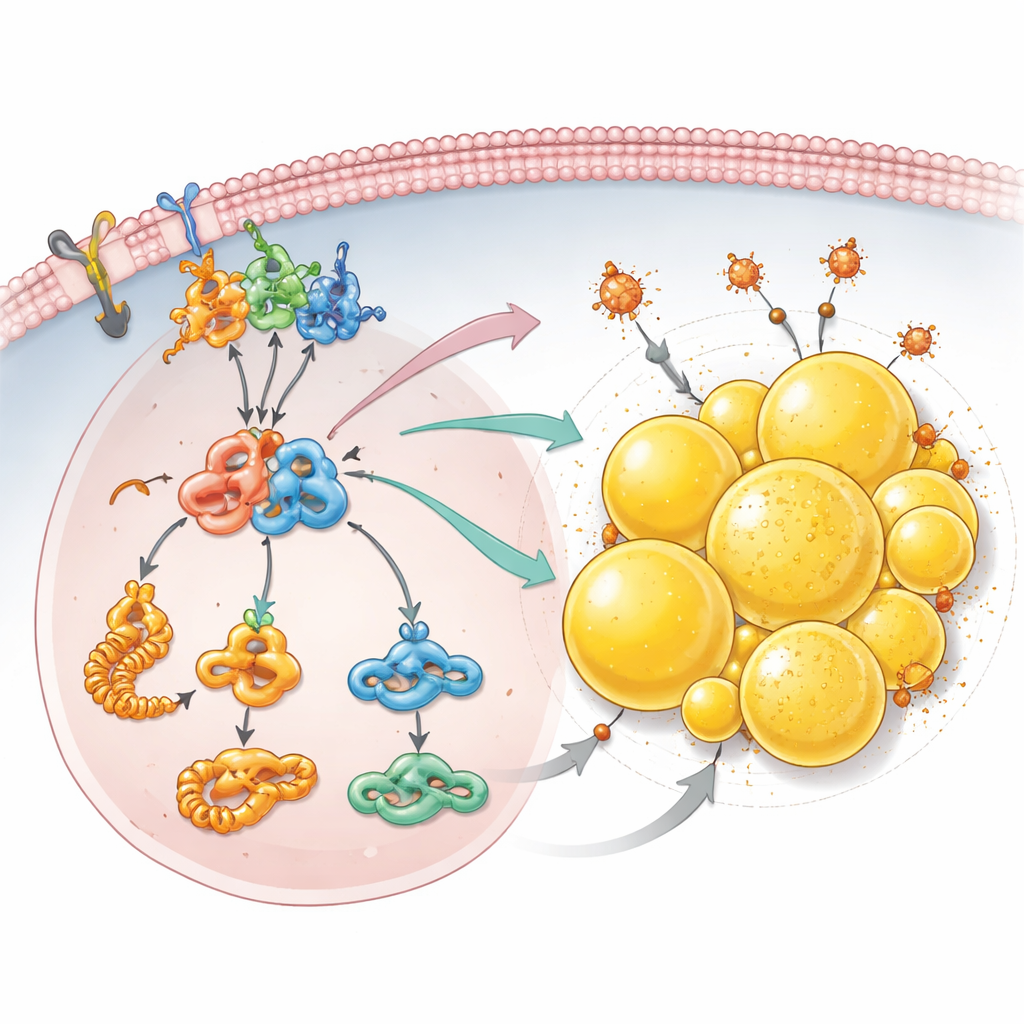
Lo stoccaggio dei grassi come scudo contro la morte cellulare
Oltre ai segnali di crescita, il gruppo ha scoperto che la perdita di PCDHGC3 riprogramma il modo in cui le cellule tumorali gestiscono i lipidi. Indagini proteomiche dettagliate hanno messo in luce una maggiore produzione dei mattoni per gli acidi grassi e livelli più elevati di acetil-CoA, un combustibile centrale usato per sintetizzare i lipidi. Le cellule prive di PCDHGC3 hanno accumulato molte più goccioline lipidiche — piccole sfere piene di grasso all’interno della cellula, particolarmente abbondanti in questo tipo di cancro renale. Questo accumulo dipendeva dall’asse mTOR–HIF2α e da PLIN2, una proteina che riveste le goccioline il cui livello aumentava con il silenziamento di PCDHGC3. Queste goccioline non si limitavano a immagazzinare grasso in eccesso: aiutavano le cellule a sfuggire alla ferroptosi, una forma di morte cellulare guidata dal ferro e dai lipidi danneggiati. Quando PLIN2 è stato ridotto, specialmente nelle cellule già prive di PCDHGC3, le goccioline lipidiche si sono ridotte e le cellule sono diventate molto più sensibili a un farmaco che induce la ferroptosi.
Trasformare il trucco di sopravvivenza del tumore nel suo punto debole
Nel complesso, lo studio rivela una catena di eventi in cui la perdita di PCDHGC3 sulla superficie cellulare attiva la chinasi di adesione focale, accende mTOR e HIF2α, potenzia la sintesi di lipidi e costruisce goccioline protettive rivestite da PLIN2. Questa rete non solo alimenta la crescita e la diffusione del tumore, ma permette anche alle cellule tumorali di nascondere i lipidi vulnerabili da reazioni distruttive che altrimenti le ucciderebbero. Gli autori propongono che mirare a questo neo-definito asse PCDHGC3–mTOR–HIF2α–PLIN2 potrebbe offrire una strategia multipla per il carcinoma renale a cellule chiare avanzato: combinare inibitori di mTOR o di HIF2α con farmaci che inducono la ferroptosi, e potenzialmente bloccare PLIN2, potrebbe trasformare l’adattamento metabolico del tumore nel suo tallone d’Achille.
Citazione: Celada, L., Cubiella, T., San-Juan-Guardado, J. et al. PCDHGC3 silencing promotes clear cell renal cell carcinoma metastasis via mTOR/HIF2α activation, lipid metabolism rewiring, and ferroptosis evasion. Cell Death Dis 17, 409 (2026). https://doi.org/10.1038/s41419-026-08643-y
Parole chiave: carcinoma renale a cellule chiare, PCDHGC3, via mTOR HIF2alpha, goccioline lipidiche, ferroptosi