Clear Sky Science · zh
SARS-CoV-2 非刺突结构蛋白劫持黏膜上皮细胞命运
当身体的内衬失去身份认同
COVID-19 以攻击肺部闻名,但许多患者也会出现口腔、肠道及其他由脆弱黏膜覆盖的器官发生难愈的溃疡。本研究提出了一个看似简单的问题:在出现可见的创伤和炎症之前,形成这些保护性内衬的细胞到底发生了什么——而这种早期损伤是否能提示新的治疗策略?
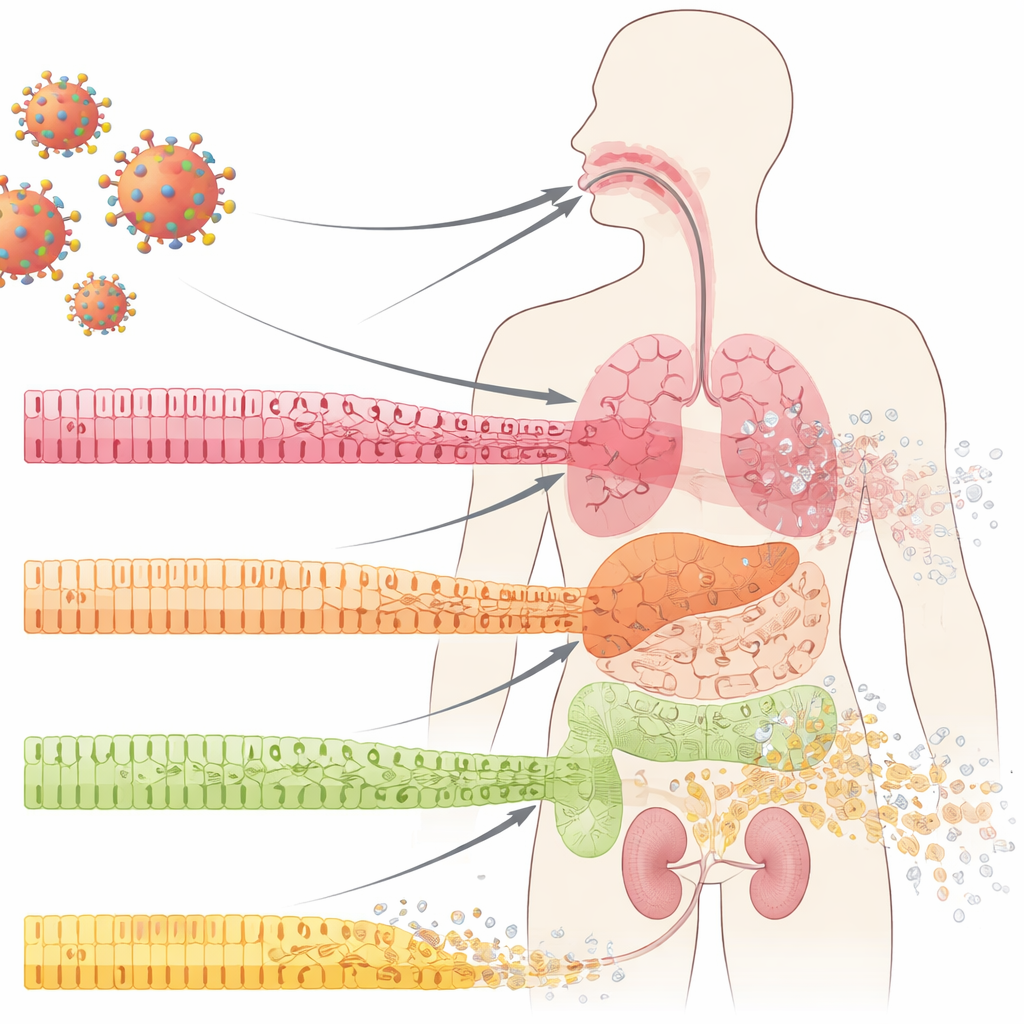
保护我们器官的前线细胞
我们体内的表面——口腔、肺、肠和肾脏内侧——被按序排列的上皮细胞覆盖。这些细胞像防水墙上的瓷砖:紧密相连、具有分化特化,并不断由下层的前体细胞补充更新。在 COVID-19 中,临床上长期注意到这些黏膜屏障出现严重崩解,包括溃疡和组织侵蚀。作者检查了 COVID-19 患者的口腔、肺和肾脏样本,发现在常规检查下仍显正常的区域中也有显著变化:成熟的、特化的细胞正在丧失它们的表型标志,而较不成熟的“干样”细胞标志物呈上升趋势。这一过程称为去分化,通常出现在受控的组织修复过程中——但在这里,它在感染早期就出现了,早于明显的炎症或瘢痕形成。
能够重新编程细胞命运的病毒壳蛋白
冠状病毒最为人所知的是其刺突蛋白,它用于进入细胞。但病毒也携带构成其外壳和内部的其他结构蛋白。在这项工作中,研究者将注意力集中在三种“非刺突”蛋白上:包膜蛋白(E)、膜蛋白(M)和核衣壳蛋白(N)。他们使用精密的人类口腔黏膜三维模型和培养的鼠舌组织,将这些蛋白逐一传递入上皮细胞观察结果。三者都能促使细胞趋向较低分化状态,但包膜蛋白尤为显著。它迅速降低成熟上皮细胞的标志物,增加更原始细胞的标志物,并削弱 E-钙粘蛋白(一种帮助细胞紧密粘连的分子)。与此同时,细胞出现诸如微核的 DNA 损伤信号,在细胞周期早期停滞,并更容易进入程序性细胞死亡。综合这些变化表明,病毒的结构外壳并非只是被动的包衣,而是积极破坏上皮稳定性的破坏者。
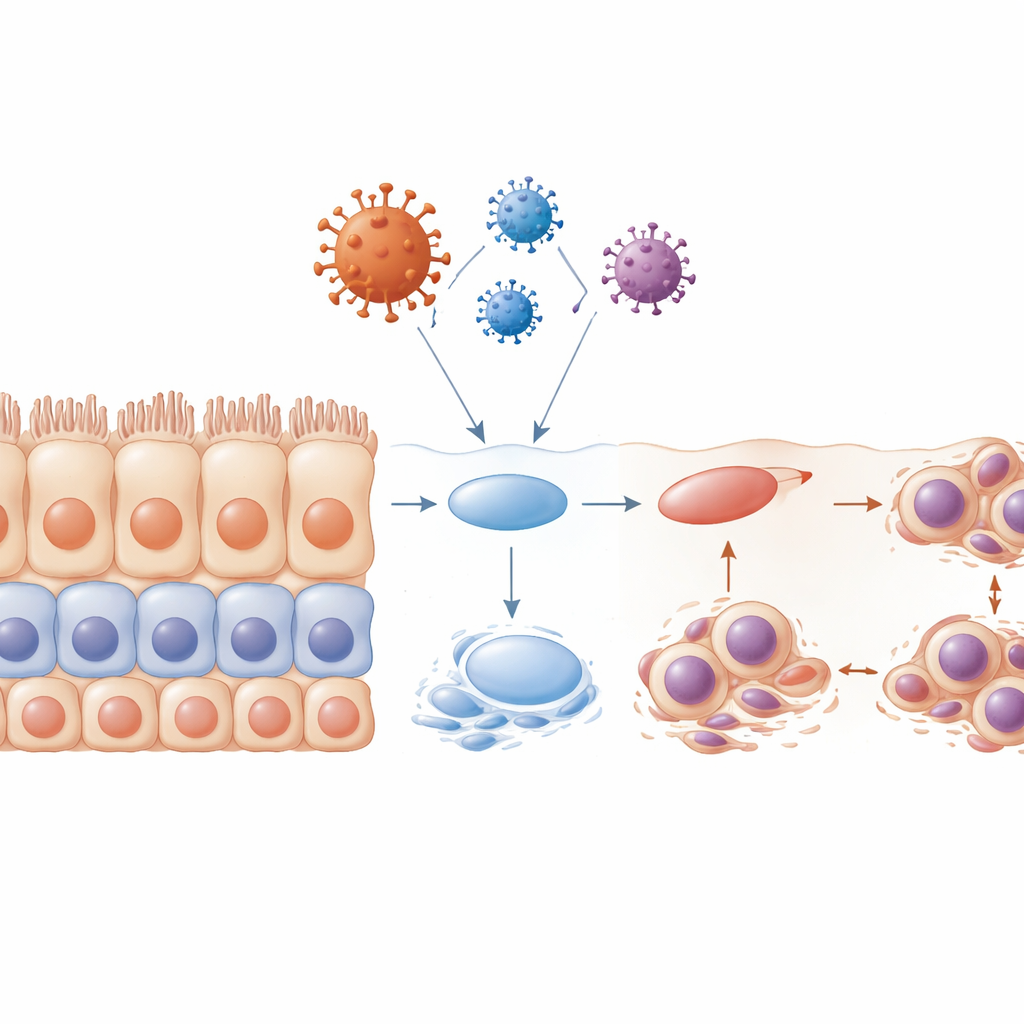
被破坏的层次结构与受损的细胞“刷状”结构
健康的复层上皮通过一个精心编排的程序自我更新:位于基底的前体细胞分裂,其后代向上迁移并成熟为高度特化的表面细胞。当研究组在细胞尚未形成完整层次前暴露于包膜蛋白时,这一程序基本崩溃。结果组织变得混乱,层次欠佳,成熟标志物减少,许多细胞被困在细胞周期的早期阶段。许多细胞呈现畸形或多重细胞核并经历凋亡,留下本应为连续屏障的空隙。研究者还检查了称为纤毛的细小毛状结构,它们有助于移动黏液和清除碎屑。发现纤毛缩短或消失,尤其在包膜蛋白的影响下,这种变化发生在细胞周期的关键阶段。这种纤毛丧失会进一步削弱组织清除病毒和污染物的能力。
一个隐匿的分子开关与潜在的新药靶点
为揭示这些病毒蛋白如何重塑细胞行为,作者比较了感染与未感染上皮细胞的蛋白谱。有一种分子——钙蛋白 2(calponin 2,简称 CNN2)——持续突出:三种非刺突蛋白均显著上调 CNN2,并且在 COVID-19 患者的口腔、肺和肾组织中均检测到升高。CNN2 有助于组织细胞的内在骨架并对机械应力作出响应。当科学家使用靶向遗传学工具降低 CNN2 水平时,包膜蛋白引起的许多有害效应被削弱:上皮标志物得以保存,组织层次改善,死亡细胞减少。他们进一步将 CNN2 的上游调控追溯到一个转录因子 GLIS2,正常情况下 GLIS2 抑制 CNN2。在患者样本和经病毒蛋白处理的细胞中,GLIS2 水平明显下降,解除对 CNN2 的抑制。这个 GLIS2–CNN2 轴似乎是 SARS-CoV-2 壳蛋白扰乱上皮细胞命运的关键通路。
对未来 COVID-19 护理的意义
对于非专业读者,核心信息是:SARS-CoV-2 能在明显组织损伤出现之前,悄然破坏身体的保护性内衬。其非刺突结构蛋白,尤其是包膜蛋白,促使前线上皮细胞失去特化性,扰乱有序层次,损伤 DNA,并导致细胞死亡。在分子层面上,病毒似乎实施了一种“双重劫持”:既使成熟细胞去分化,又阻断前体细胞的正常成熟,主要通过 GLIS2–CNN2 控制开关。因为 CNN2 处在该通路的关键位置,且在实验模型中降低 CNN2 可逆转大部分损害,它有望成为保护 COVID-19 中黏膜屏障并可能减少难愈溃疡与多器官损伤的治疗靶点。
引用: Gao, Y., Souza, L.L., Kang, H.S. et al. SARS-CoV-2 nonspike structural proteins hijack mucosa epithelial cell fate. Cell Death Dis 17, 340 (2026). https://doi.org/10.1038/s41419-026-08611-6
关键词: SARS-CoV-2 包膜蛋白, 黏膜上皮, 细胞去分化, CNN2, GLIS2