Clear Sky Science · ru
Неспайковые структурные белки SARS-CoV-2 перепрограммируют судьбу эпителиальных клеток слизистых
Когда оболочки организма теряют свою идентичность
COVID-19 известен как заболевание, поражающее легкие, но у многих пациентов также появляются упорные язвы во рту, кишечнике и других органах, выстланных тонкими слизистыми оболочками. В этом исследовании задают на первый взгляд простой вопрос: что именно происходит с клетками, формирующими эти защитные покровы, до появления видимых ран и воспаления — и может ли это раннее повреждение указать на новые способы лечения?
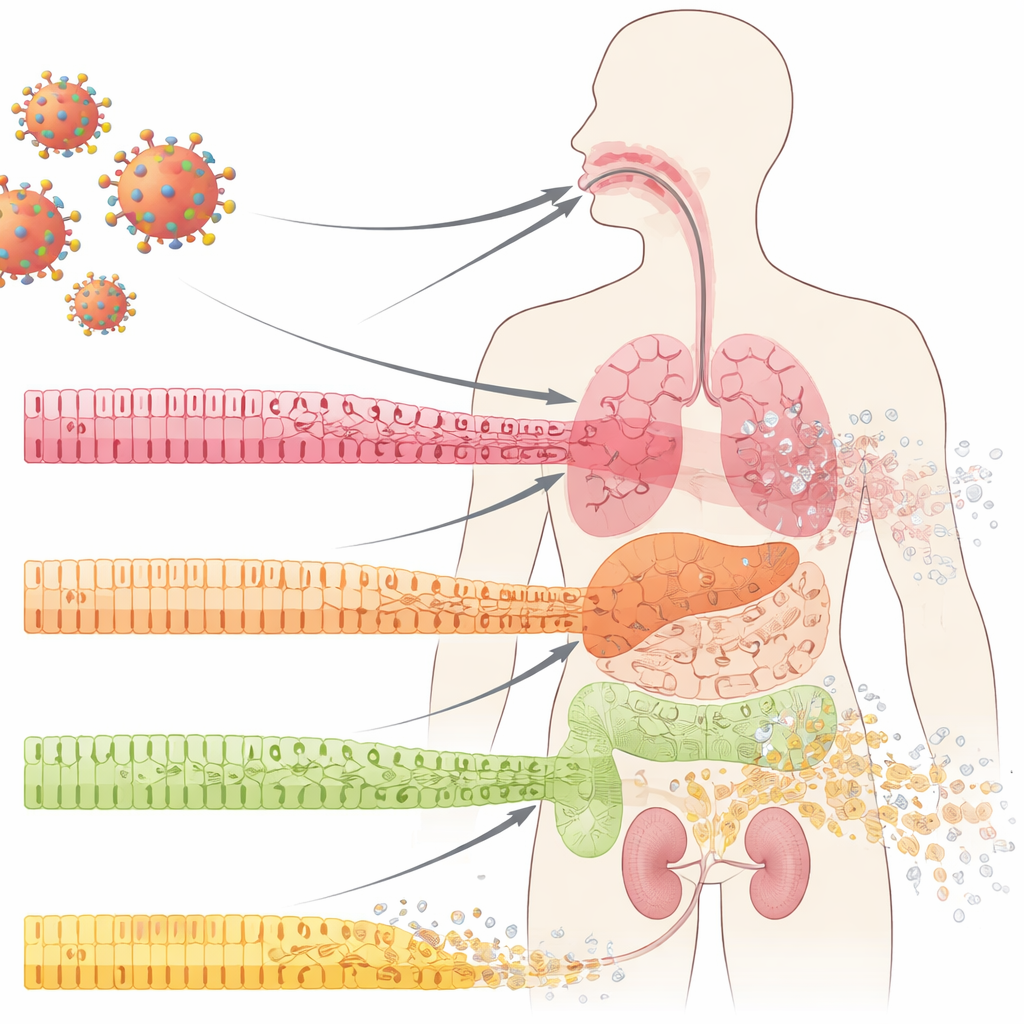
Передовые клетки, защищающие наши органы
Внутренние поверхности — внутри рта, легких, кишечника и почек — покрыты эпителиальными клетками, организованными в упорядоченные слои. Эти клетки действуют как плитки в водонепроницаемой стене: плотно соединённые, специализированные и постоянно обновляющиеся из пула подлежащих пророгениторных клеток. При COVID-19 врачи давно отмечают резкий распад этих слизистых барьеров, включая язвы и эрозии тканей. Авторы изучили образцы из полости рта, легких и почек пациентов с COVID-19 и обнаружили нечто примечательное даже в областях, которые при обычном осмотре выглядели нормально: зрелые, специализированные клетки теряли свою идентичность, а маркеры менее зрелых, «стволовоподобных» клеток увеличивались. Этот процесс, называемый дедифференцировкой, обычно наблюдается при контролируемом восстановлении тканей — но здесь он проявлялся рано в ходе инфекции, ещё до очевидного воспаления или рубцевания.
Вирусные оболочечные белки, перепрограммирующие судьбу клеток
Коронавирус наиболее известен своим спайковым белком, с помощью которого он проникает в клетки. Но у вируса также есть другие структурные белки, формирующие его оболочку и внутреннюю часть. В этой работе исследователи сосредоточились на трёх таких «неспайковых» белках: оболочном (E), мембранном (M) и нуклеокапсидном (N). Используя сложные 3D‑модели человеческой оральной слизистой и культивированные ткани языка мыши, они вводили каждый из этих белков в эпителиальные клетки, чтобы посмотреть, что произойдёт. Все три белка могли сдвинуть клетки в менее дифференцированное состояние, но особенно выделялся оболочечный белок. Он быстро снижал маркеры зрелых эпителиальных клеток, повышал маркеры более примитивных клеток и ослаблял E‑кадгерин — молекулу, помогающую клеткам плотно сцепляться друг с другом. Одновременно клетки демонстрировали сигналы повреждения ДНК, такие как микронуклеи, застревали на раннем контрольном этапе клеточного цикла и чаще подвергались программируемой гибели. В совокупности эти изменения указывают на то, что структурная оболочка вируса — не просто пассивная оболочка, а активный диверсант стабильности эпителия.
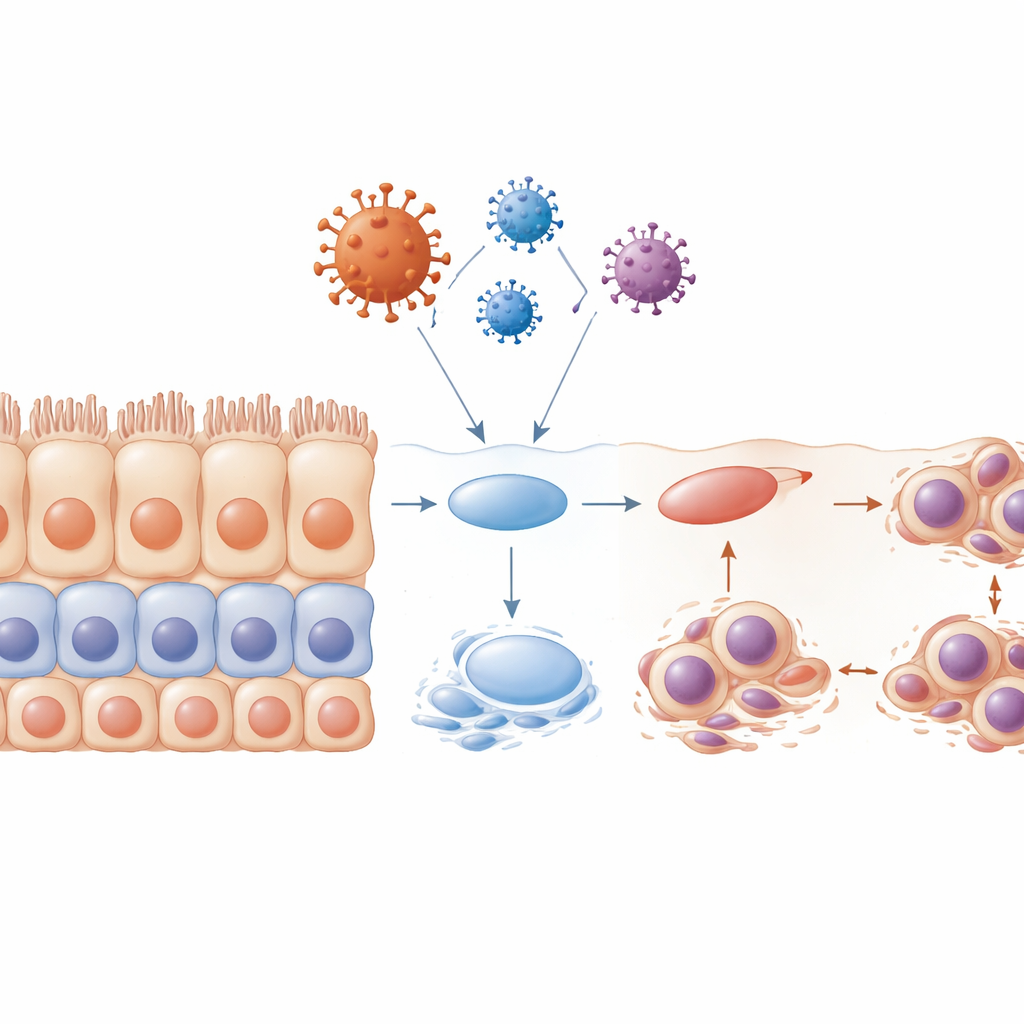
Нарушенная слоистость и повреждённые клеточные «щёточки»
Здоровые многослойные эпителии обновляются посредством тщательно скоординированной программы: проксимальные прогениторные клетки делятся у основания, затем их потомки поднимаются вверх и созревают в высокоспециализированные поверхностные клетки. Когда команда подвергла клетки воздействию оболочечного белка до формирования полных слоёв, эта программа фактически разрушилась. В результате ткань оказалась дезорганизованной, со слабой слоистостью, уменьшением маркеров зрелости и множеством клеток, застрявших в ранней фазе клеточного цикла. У многих клеток наблюдались деформированные или множественные ядра и развивался апоптоз, оставляя пробелы там, где должен быть сплошной барьер. Исследователи также изучали крошечные реснички — цилии, которые помогают перемещать слизь и мусор. Они обнаружили, что цилии уменьшались или исчезали, особенно под влиянием оболочечного белка, и что это происходило на ключевых этапах клеточного цикла. Потеря цилий дополнительно ослабляет способность ткани очищать вирусы и загрязнения.
Скрытый молекулярный переключатель и новая мишень для лекарств
Чтобы выяснить, как вирусные белки перенастраивают поведение клеток, авторы сравнили белковые профили инфицированных и неинфицированных эпителиальных клеток. Одна молекула, кальпоннин‑2 (CNN2), постоянно выделялась: она сильно повышалась под действием всех трёх неспайковых белков и была повышена в тканях рта, легких и почек пациентов с COVID-19. CNN2 помогает организовать внутренний каркас клетки и реагирует на механические напряжения. Когда учёные снизили уровень CNN2 с помощью направленных генетических инструментов, многие вредные эффекты оболочечного белка ослабевали: маркеры эпителия сохранялись, слоистость ткани улучшалась, и меньше клеток погибало. Затем они проследили регуляцию CNN2 вверх по цепочке до фактора транскрипции GLIS2, который обычно сдерживает CNN2. В образцах пациентов и в клетках, обработанных вирусными белками, уровни GLIS2 заметно снижались, что снимало тормоз с CNN2. Ось GLIS2–CNN2, по-видимому, является ключевым путём, через который структурные белки SARS‑CoV‑2 срывают судьбу эпителиальных клеток.
Что это значит для будущего лечения COVID-19
Для неспециалиста основная идея такова: SARS‑CoV‑2 может тихо дестабилизировать защитные оболочки организма задолго до появления очевидного повреждения тканей. Его неспайковые структурные белки, особенно оболочечный белок, заставляют передовые эпителиальные клетки терять специализацию, нарушают их упорядоченную слоистость, повреждают их ДНК и приводят к гибели. На молекулярном уровне вирус осуществляет «двойной захват»: он как дедифференцирует зрелые клетки, так и блокирует нормальное созревание прогениторных клеток, во многом посредством контрольного переключателя GLIS2–CNN2. Поскольку CNN2 занимает ключевое место в этом пути и его подавление может обратить значительную часть повреждений в лабораторных моделях, этот белок предстает как перспективная мишень для терапии, направленной на защиту слизистых барьеров при COVID-19 и потенциальное снижение стойких язв и множественного поражения органов.
Цитирование: Gao, Y., Souza, L.L., Kang, H.S. et al. SARS-CoV-2 nonspike structural proteins hijack mucosa epithelial cell fate. Cell Death Dis 17, 340 (2026). https://doi.org/10.1038/s41419-026-08611-6
Ключевые слова: белок оболочки SARS-CoV-2, слизистая эпителия, дедифференцировка клеток, CNN2, GLIS2