Clear Sky Science · nl
SARS-CoV-2 non-spike structure-eiwitten kapen het lot van mucosa-epitheelcellen
Wanneer de bekledingen van het lichaam hun identiteit verliezen
COVID-19 staat bekend om zijn aanval op de longen, maar veel patiënten ontwikkelen ook hardnekkige zweren in de mond, darm en andere organen die bekleed zijn met kwetsbare slijmvliezen. Deze studie stelt een bedrieglijk eenvoudige vraag: voordat we zichtbare wonden en ontsteking zien, wat gebeurt er precies met de cellen die deze beschermende bekledingen vormen — en kan die vroege schade wijzen op nieuwe behandelstrategieën?
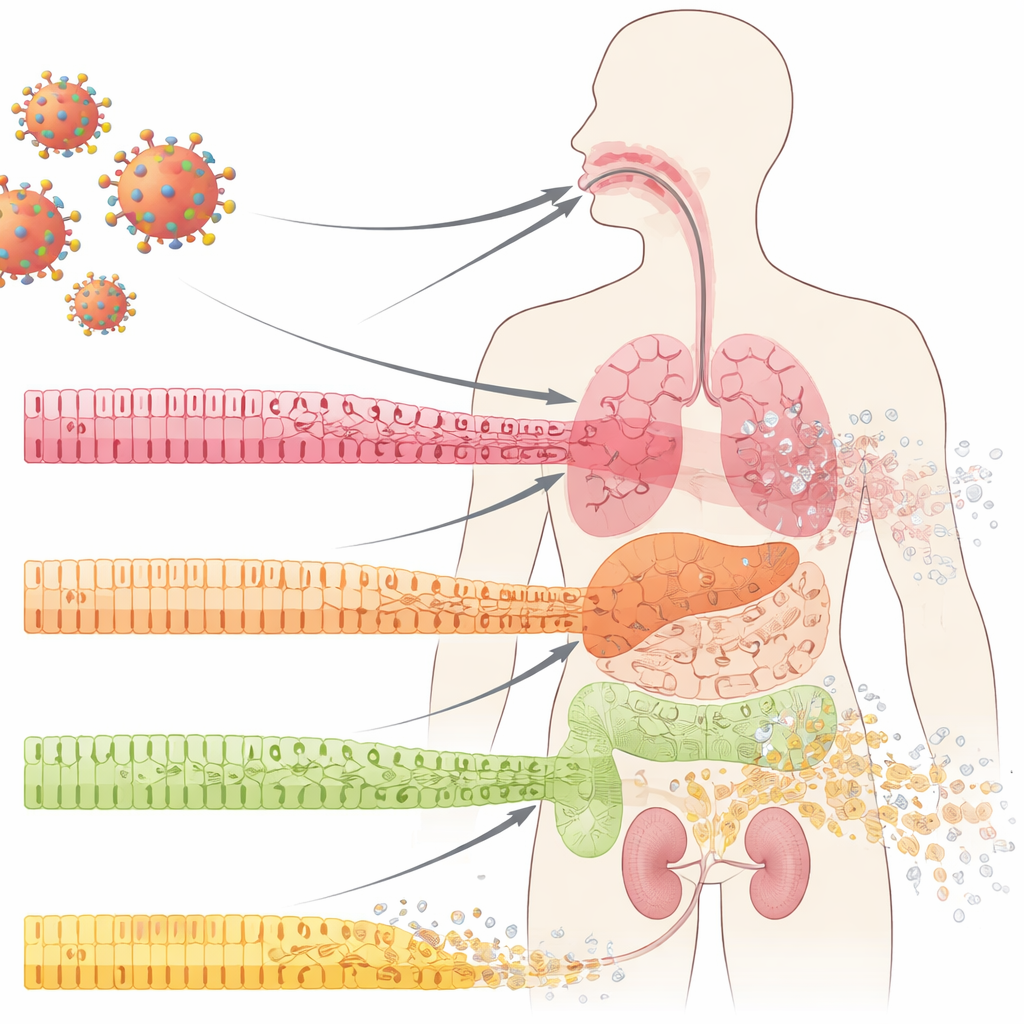
De voorhoedecellen die onze organen beschermen
Onze inwendige oppervlakken — in de mond, longen, darmen en nieren — zijn bedekt met epitheelcellen die in ordelijke lagen zijn gerangschikt. Deze cellen werken als tegels in een waterdichte muur: nauw verbonden, gespecialiseerd en voortdurend vernieuwd vanuit een voorraad onderliggende progenitorcellen. Bij COVID-19 hebben artsen al lang dramatische ineenstortingen van deze slijmvliesbarrières waargenomen, waaronder zweren en weefselerosiën. De auteurs onderzochten monsters uit de mondholte, longen en nieren van COVID-19-patiënten en vonden iets opvallends, zelfs in gebieden die bij routinematig onderzoek nog normaal leken: de rijpe, gespecialiseerde cellen verloren hun identiteit en markers van minder rijpe, ‘stamcelachtige’ cellen namen toe. Dit proces, dedifferentiatie genoemd, verschijnt normaal tijdens gecontroleerd weefselherstel — maar hier trad het vroeg op in de infectie, vóór duidelijke ontsteking of littekenvorming.
Virale schaalproteïnen die het celnlot herschrijven
Het coronavirus is het bekendst om zijn spike-eiwit, dat het gebruikt om cellen binnen te dringen. Maar het virus draagt ook andere structurele eiwitten die zijn schaal en binnenkant vormen. In dit werk richtten de onderzoekers zich op drie van deze “non-spike” eiwitten: envelope (E), membrane (M) en nucleocapsid (N). Met behulp van verfijnde 3D-modellen van menselijk mondslijmvlies en gekweekte muizentongweefsels leverden ze elk van deze eiwitten in epitheelcellen om te zien wat er zou gebeuren. Alle drie konden de cellen naar een minder gedifferentieerde toestand dwingen, maar het enveloppe-eiwit viel op. Het verminderde snel markers van rijpe epitheelcellen, verhoogde markers van meer primitieve cellen en verzwakte E-cadherine, een molecuul dat cellen helpt stevig aan elkaar te hechten. Tegelijkertijd begonnen cellen DNA-schadesignalen te vertonen zoals micronuclei, raakten ze vast in een checkpoint vroeg in de celcyclus en hadden ze een grotere kans op geprogrammeerde celdood. Gezamenlijk suggereren deze veranderingen dat de structurele schaal van het virus niet slechts een passief omhulsel is, maar een actieve saboteur van epitheliale stabiliteit.
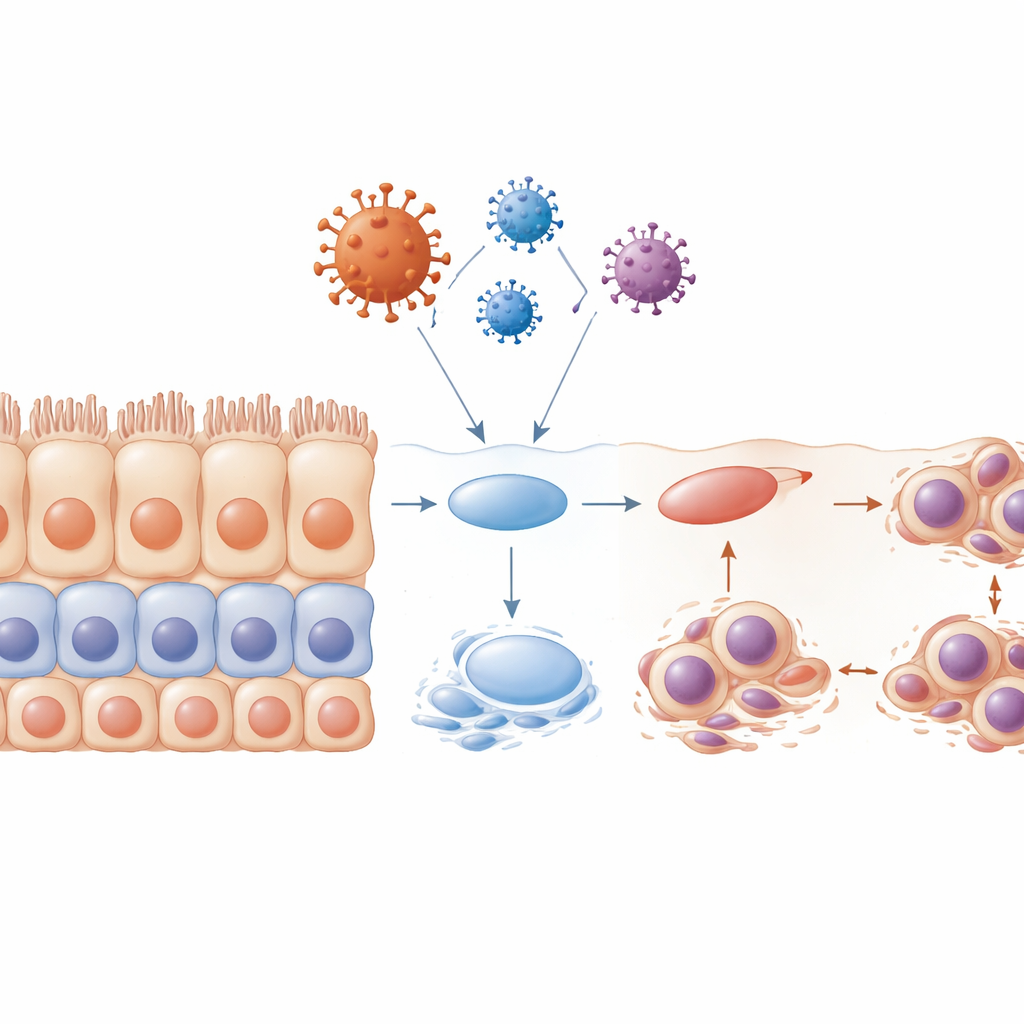
Verstoorde lagen en beschadigde cellulaire “borstels”
Gezond gelaagd epitheel vernieuwt zich via een zorgvuldig georkestreerd programma: progenitorcellen delen zich dicht bij de basis, waarna hun nakomelingen omhoog bewegen en uitrijpen tot sterk gespecialiseerde oppervlakkingscellen. Toen het team cellen blootstelde aan het enveloppe-eiwit voordat ze volledige lagen hadden gevormd, stortte dit programma in feite in. Het resulterende weefsel was ongeorganiseerd, met slechte gelaagdheid, minder rijpe markers en veel cellen die vastzaten in een vroeg stadium van de celcyclus. Veel van deze cellen droegen misvormde of meerdere kernen en ondergingen apoptose, waardoor er gaten ontstonden waar een continue barrière had moeten zijn. De onderzoekers onderzochten ook kleine haarachtige structuren, cilia genaamd, die helpen om slijm en afval te verplaatsen. Ze ontdekten dat cilia krimpten of verdwenen, vooral onder invloed van het enveloppe-eiwit, en dat dit op cruciale momenten van de celcyclus gebeurde. Dit verlies aan cilia zou het vermogen van het weefsel om virussen en verontreinigingen te verwijderen verder ondermijnen.
Een verborgen moleculaire schakel en een nieuw medicijndoel
Om te achterhalen hoe deze virale eiwitten het celgedrag herbedraden, vergeleken de auteurs de eiwitprofielen van geïnfecteerde en niet-geïnfecteerde epitheelcellen. Eén molecuul, calponin 2 (CNN2), viel consequent op: het werd sterk verhoogd door alle drie de non-spike-eiwitten en was verhoogd in het mond-, long- en nierweefsel van COVID-19-patiënten. CNN2 helpt bij het organiseren van het interne geraamte van de cel en reageert op mechanische stress. Toen de wetenschappers CNN2-niveaus verlaagden met gerichte genetische middelen, werden veel van de schadelijke effecten van het enveloppe-eiwit afgezwakt: epitheliale markers bleven behouden, de weefsellaag verbeterde en minder cellen stierven. Ze traceerden vervolgens de regulatie van CNN2 omhoog naar een transcriptiefactor genaamd GLIS2, die normaal gesproken CNN2 in toom houdt. In patiëntmonsters en in door virus-eiwit behandelde cellen waren GLIS2-niveaus merkbaar verlaagd, waardoor de rem op CNN2 werd losgelaten. Deze GLIS2–CNN2-as lijkt een sleutelroute te zijn waardoor de schaalproteïnen van SARS-CoV-2 het celnlot van epitheelcellen ontregelen.
Wat dit betekent voor toekomstige zorg bij COVID-19
Voor niet-specialisten is de kernboodschap dat SARS-CoV-2 stilletjes de beschermende bekledingen van het lichaam kan destabiliseren lang voordat zichtbare weefselschade optreedt. Zijn non-spike structurele eiwitten, vooral het enveloppe-eiwit, drijven voorlinie-epitheelcellen weg van specialisatie, verstoren hun ordelijke gelaagdheid, beschadigen hun DNA en doden ze af. Op moleculair niveau lijkt het virus een “dubbele kaping” uit te voeren: het induceert dedifferentiatie van rijpe cellen en blokkeert de normale rijping van progenitorcellen, grotendeels via een GLIS2–CNN2 regelschakelaar. Omdat CNN2 op een cruciaal punt in deze route zit en vermindering ervan veel van de schade in laboratoriummodellen kan terugdraaien, komt het naar voren als een veelbelovend doel voor therapieën die gericht zijn op het beschermen van mucosale barrières bij COVID-19 en mogelijk het verminderen van hardnekkige zweren en multiorgaanschade.
Bronvermelding: Gao, Y., Souza, L.L., Kang, H.S. et al. SARS-CoV-2 nonspike structural proteins hijack mucosa epithelial cell fate. Cell Death Dis 17, 340 (2026). https://doi.org/10.1038/s41419-026-08611-6
Trefwoorden: SARS-CoV-2 enveloppe-eiwit, mucosa-epitheel, celdedifferentiatie, CNN2, GLIS2