Clear Sky Science · tr
SARS-CoV-2 spike dışı yapısal proteinleri mukoza epitel hücresi kaderini ele geçiriyor
Vücudun Örtüleri Kimliklerini Kaybettiğinde
COVID-19 akciğerleri hedef almasıyla bilinir, ancak birçok hastada ağızda, bağırsakta ve hassas mukoza zarlarıyla kaplı diğer organlarda inatçı ülserler de gelişir. Bu çalışma, aldatıcı derecede basit bir soruyu soruyor: görünür yaralar ve iltihaplanma ortaya çıkmadan önce, bu koruyucu yüzeyleri oluşturan hücrelerle tam olarak ne oluyor—ve bu erken hasar yeni tedavi stratejilerine işaret edebilir mi?
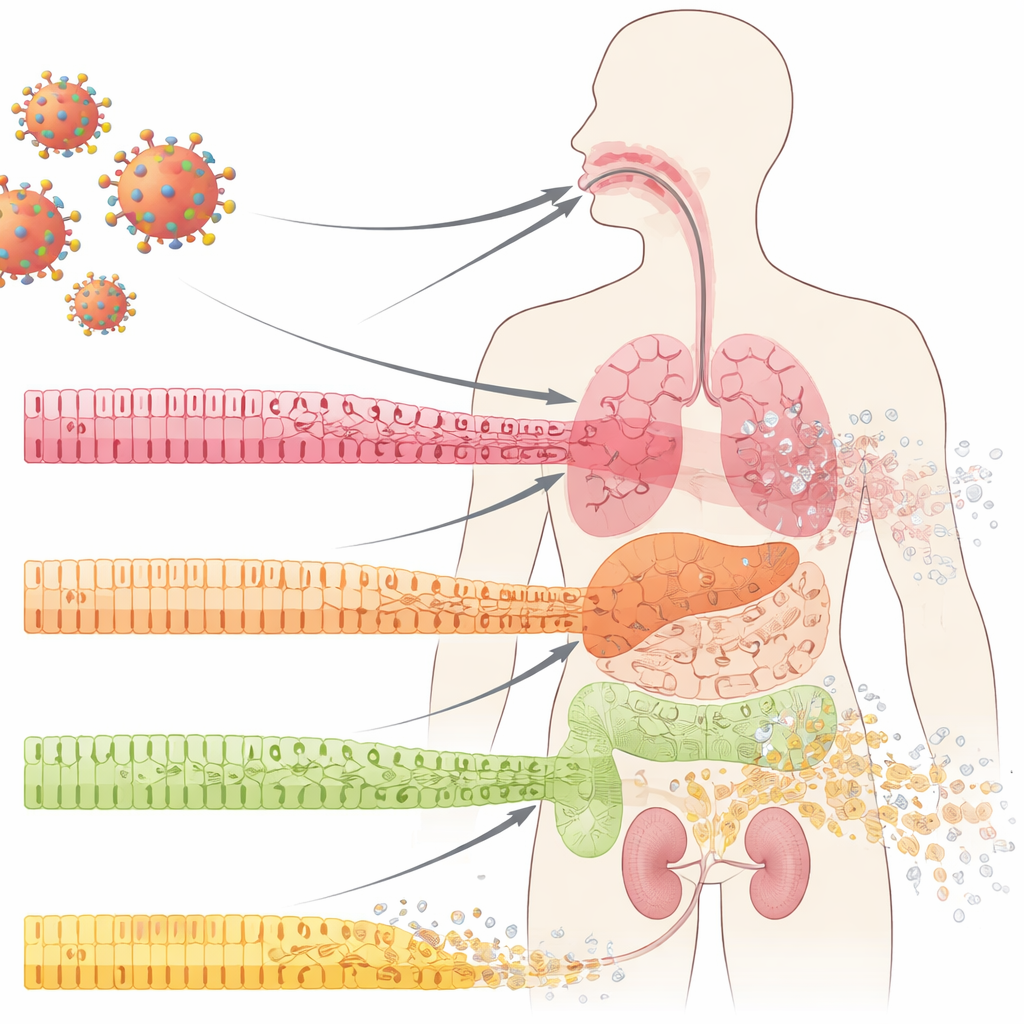
Organlarımızı Koruyan Ön Cephe Hücreleri
Ağız, akciğer, bağırsak ve böbrek gibi iç yüzeylerimiz düzenli katmanlar halinde dizilmiş epitel hücreleriyle kaplıdır. Bu hücreler su geçirmez bir duvardaki karolar gibi davranır: sıkı bağlantılı, özelleşmiş ve altındaki progenitör hücre havuzundan sürekli yenilenir. COVID-19’da hekimler uzun süredir mukoza bariyerlerinde, ülserler ve doku erozyonları dahil, dramatik bozulmalar gözlemlemiştir. Yazarlar COVID-19 hastalarının ağız boşluğu, akciğer ve böbrek örneklerini incelediler ve rutin muayenede hâlâ normal görünen bölgelerde bile çarpıcı bir bulgu buldular: olgun, özelleşmiş hücreler kimliklerini kaybediyor ve daha az olgun, “kök-benzeri” hücre işaretçileri artıyordu. Bu süreç, dediferansiyasyon olarak adlandırılır ve genellikle kontrollü doku onarımında ortaya çıkar—ama burada belirgin iltihap veya skarlaşma olmadan enfeksiyonun erken döneminde görülüyordu.
Hücre Kaderini Yeniden Programlayan Viral Kabuk Proteinleri
Koronavirüs, hücrelere girmek için kullandığı spike (diken) proteiniyle en çok tanınır. Ancak virüs, kabuğunu ve iç yapısını oluşturan başka yapısal proteinler de taşır. Bu çalışmada araştırmacılar bu “spike dışı” üç proteine odaklandılar: zarf (E), membran (M) ve nükleokapsid (N). İnsan ağız mukozasının gelişmiş 3B modelleri ve kültüre edilmiş fare dil dokusu kullanarak, bu proteinlerin her birini epitel hücrelerine verip ne olacağını gözlemlediler. Üçü de hücreleri daha az farklılaşmış bir duruma itebildi, ama zarf proteini öne çıktı. Olgun epitel hücre işaretçilerini hızla azalttı, daha ilkel hücre işaretçilerini artırdı ve hücrelerin sıkı yapışmasına yardımcı olan E-kaderin’i zayıflattı. Aynı zamanda hücreler mikronükleus gibi DNA hasarı sinyalleri göstermeye, hücre döngüsünde erken bir kontrol noktasında takılmaya ve programlı hücre ölümüne daha yatkın hale gelmeye başladı. Bu değişiklikler birlikte virusun yapısal kabuğunun yalnızca pasif bir örtü olmayıp epitel stabilitesinin aktif bir sabotekarı olduğunu düşündürüyor.
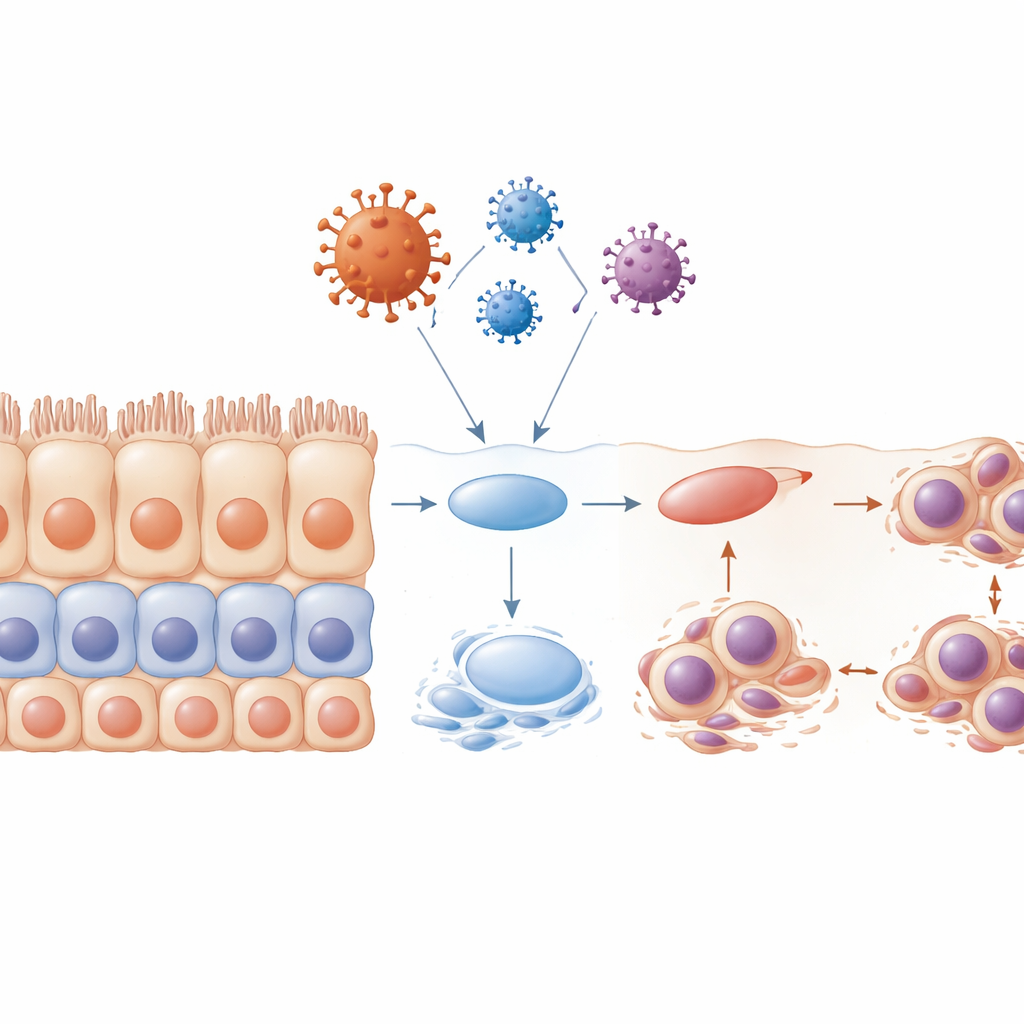
Bozulmuş Katmanlaşma ve Hasar Görmüş Hücresel “Fırçalar”
Sağlıklı çok katlı epiteller, progenitör hücrelerin tabana yakın bölgedeki bölünmesiyle, ardından soylarının yukarı hareket edip yüzeyde yüksek derecede özelleşmiş hücrelere olgunlaşmasıyla kendini özenle yeniler. Ekip, hücreler tam katmanlaşmayı oluşturmadan önce zarf proteinine maruz bırakıldığında bu programın temel olarak çöktüğünü gördü. Ortaya çıkan doku düzensizdi; zayıf katmanlaşma, daha az olgun belirteç ve hücre döngüsünün erken evresinde sıkışmış çok sayıda hücre vardı. Bu hücrelerin birçoğu şekilsiz veya birden çok çekirdeğe sahipti ve apoptoza giderek sürekli bir bariyerin olması gereken yerlerde boşluklar bıraktı. Araştırmacılar ayrıca mukus ve artıkların hareketine yardımcı olan küçük saç benzeri yapılar olan sillerin durumunu incelediler. Sillerin özellikle zarf proteininin etkisi altında küçüldüğünü veya kaybolduğunu ve bunun hücre döngüsünün kritik evrelerinde meydana geldiğini buldular. Bu sillerin kaybı dokunun virüsleri ve kirleticileri temizleme yeteneğini daha da zayıflatacaktır.
Gizli Bir Moleküler Anahtar ve Yeni Bir İlaç Hedefi
Bu viral proteinlerin hücre davranışını nasıl yeniden kabloladığını ortaya çıkarmak için yazarlar enfekte ve enfekte olmayan epitel hücrelerinin protein profillerini karşılaştırdılar. Bir molekül, kalponin 2 (CNN2), tutarlı biçimde öne çıktı: üç spike dışı protein tarafından güçlü şekilde artırıldı ve COVID-19 hastalarının ağız, akciğer ve böbrek dokularında yükselmişti. CNN2 hücrenin iç iskeletini düzenlemeye yardımcı olur ve mekanik strese yanıt verir. Bilim insanları hedeflenmiş genetik araçlarla CNN2 seviyelerini azalttıklarında, zarf proteininin birçok zararlı etkisi hafifledi: epitel belirteçleri korundu, doku katmanlaşması iyileşti ve daha az hücre öldü. Ardından CNN2 düzenlemesini GLIS2 adlı bir transkripsiyon faktörüne kadar izlediler; GLIS2 normalde CNN2’yi kontrol altında tutar. Hasta örneklerinde ve virüs-proteine maruz bırakılan hücrelerde GLIS2 seviyeleri belirgin şekilde azalmıştı ve CNN2 üzerindeki freni gevşetiyordu. Bu GLIS2–CNN2 ekseni, SARS-CoV-2’nin kabuk proteinlerinin epitel hücre kaderini bozan ana yolaklarından biri gibi görünüyor.
Gelecekteki COVID-19 Bakımı İçin Anlamı
Bir uzman olmayan için temel mesaj, SARS-CoV-2’nin koruyucu örtüleri belirgin doku hasarı ortaya çıkmadan çok daha önce sessizce istikrarsızlaştırabileceğidir. Spike dışı yapısal proteinleri, özellikle zarf proteini, ön cephe epitel hücrelerini uzmanlıklarını yitirmeye, düzenli katmanlaşmalarını bozmaya, DNA’larını hasara uğratmaya ve hücreleri öldürmeye iter. Moleküler düzeyde virüs, büyük ölçüde bir GLIS2–CNN2 kontrol anahtarı aracılığıyla olgun hücreleri dediferansiyone etmek ve progenitör hücrelerin normal olgunlaşmasını engellemek suretiyle bir “çifte kaçırma” gerçekleştiriyor gibi görünmektedir. CNN2 bu yolakta kritik bir noktada yer aldığı ve laboratuvar modellerinde azaltılması hasarın çoğunu tersine çevirebildiği için, mukozal bariyerleri korumaya yönelik terapilerde umut verici bir hedef olarak öne çıkmaktadır; bu da inatçı ülserleri ve çoklu organ hasarını azaltma potansiyeli taşır.
Atıf: Gao, Y., Souza, L.L., Kang, H.S. et al. SARS-CoV-2 nonspike structural proteins hijack mucosa epithelial cell fate. Cell Death Dis 17, 340 (2026). https://doi.org/10.1038/s41419-026-08611-6
Anahtar kelimeler: SARS-CoV-2 zarf proteini, mukozal epitel, hücre dediferansiyasyonu, CNN2, GLIS2