Clear Sky Science · he
חלבוני מבנה של SARS-CoV-2 שאינם סייפק חוטפים את גורל התאים באפיתל הרירתי
כששטחי הגוף מאבדים את זהותם
הידוע על COVID-19 שהוא תוקף את הריאות, אך אצל חולים רבים מופיעות גם כיבים עקשניים בפה, במעיים ובאיברים אחרים המצופים בקרומי ריר עדינים. המחקר הזה שואל שאלה שנראית פשוטה אך חשובה: לפני שמופיעים פצעים ודלקת גלויים, מה בדיוק קורה לתאים שמרכיבים את הציפויים המגינים האלה — והאם הנזק המוקדם הזה עשוי להצביע על אסטרטגיות טיפול חדשות?
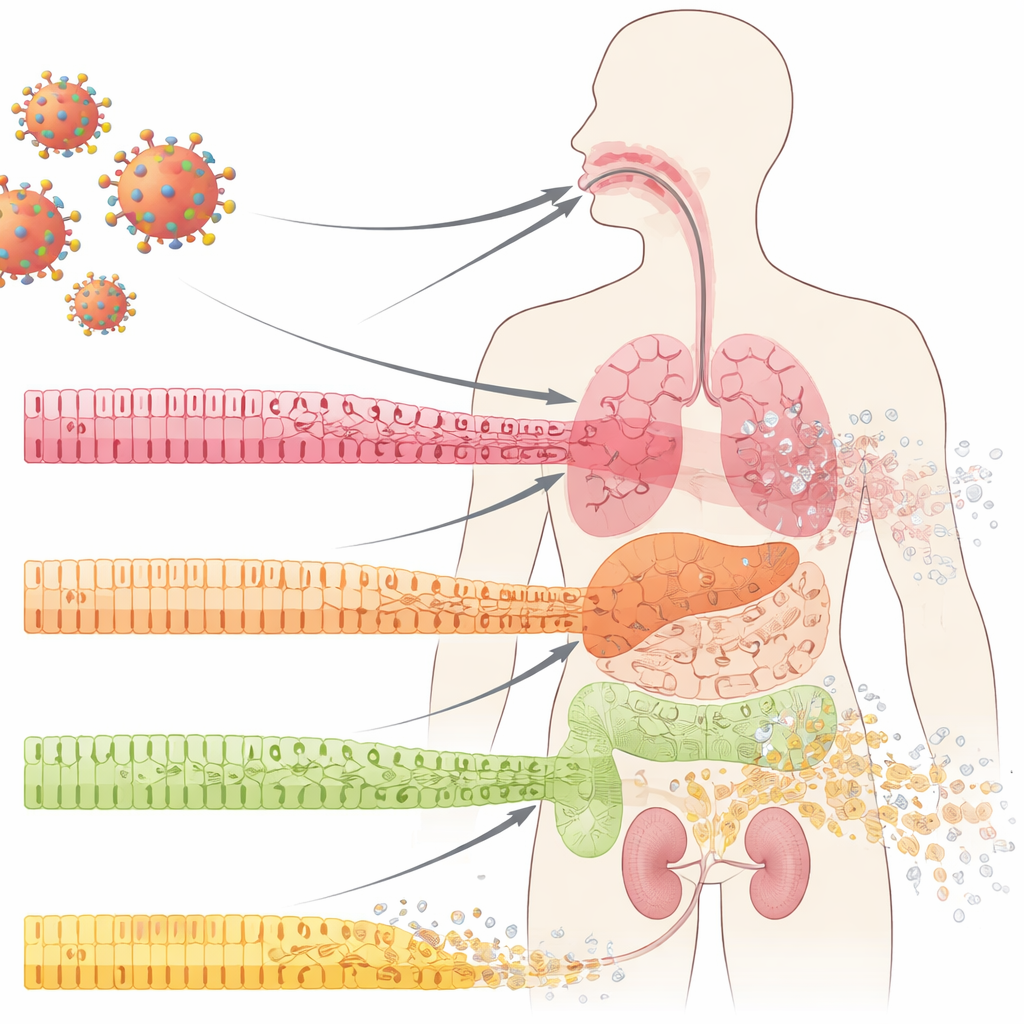
תאי החזית המגינים על האיברים שלנו
המשטחים הפנימיים שלנו — בתוך הפה, הריאות, המעי והכליות — מכוסים בתאי אפיתל מסודרים בשכבות. תאים אלה פועלים כמו אריחים בקיר אטום למים: קשורים בצפיפות, מתמחים, ומתחדשים באופן קבוע ממאגר של תאי אב תת-משטחים. ב-COVID-19, רופאים שמו לב זמן רב להתפוררות דרמטית של מחסומי ריריות אלה, כולל כיבים ושחיקה של רקמה. החוקרים בחנו דגימות מחלל הפה, מהריאות ומהכליות של חולי COVID-19 ומצאו תופעה בולטת גם באזורים שנראו נורמליים בבדיקה שגרתית: התאים הבוגרים והמתמחים איבדו את זהותם, וסמנים של תאים פחות בוגרים ודמויי-גזע עלו. תהליך זה, שנקרא דדיקרנטיפיקציה, מופיע בדרך כלל בתיקון רקמות מבוקר — אבל כאן הוא הופיע מוקדם במהלך הדבקה, לפני דלקת גלויה או צלקת.
חלבוני מעטפת ויראליים שמתכנתים מחדש את גורל התאים
קורונווירוס מוכר בעיקר בזכות חלבון הספייק, שבאמצעותו הוא נכנס לתאים. אך הוירוס נושא גם חלבוני מבנה אחרים שיוצרים את מעטפתו ופנימיותו. בעבודה זו התמקדו החוקרים בשלושה מהחלבונים ה"לא-ספייק": חלבון המעטפת (E), החלבון הממברנלי (M) והנוקלאוקפסיד (N). באמצעות מודלים תלת-ממדיים של רירית הפה האנושית ורקמות לשון של עכבר בזריעה, הם העבירו כל אחד מהחלבונים האלה לתאים אפיתליאליים כדי לבדוק מה יקרה. שלושת החלבונים יכלו לדחוף את התאים למצב פחות מתמחה, אך חלבון המעטפת בלט במיוחד. הוא הקטין במהירות סמני תאים אפיתליאליים בוגרים, הגביר סמנים של תאים פרימיטיביים יותר והחליש את E-cadherin, מולקולה שמסייעת לתאים להיצמד זה לזה. במקביל, תאים הראו סימני נזק ל-DNA כגון מיקרו-גרעינים, תקועים במעבר ביקורת מוקדם במחזור התא, והם היו מועדים יותר למות מתוכנן (אפופטוזה). יחד, השינויים האלו מרמזים שמעטפת הוירוס אינה רק ציפוי פסיבי אלא שבורסת פעילות שמערערת את יציבות האפיתל.
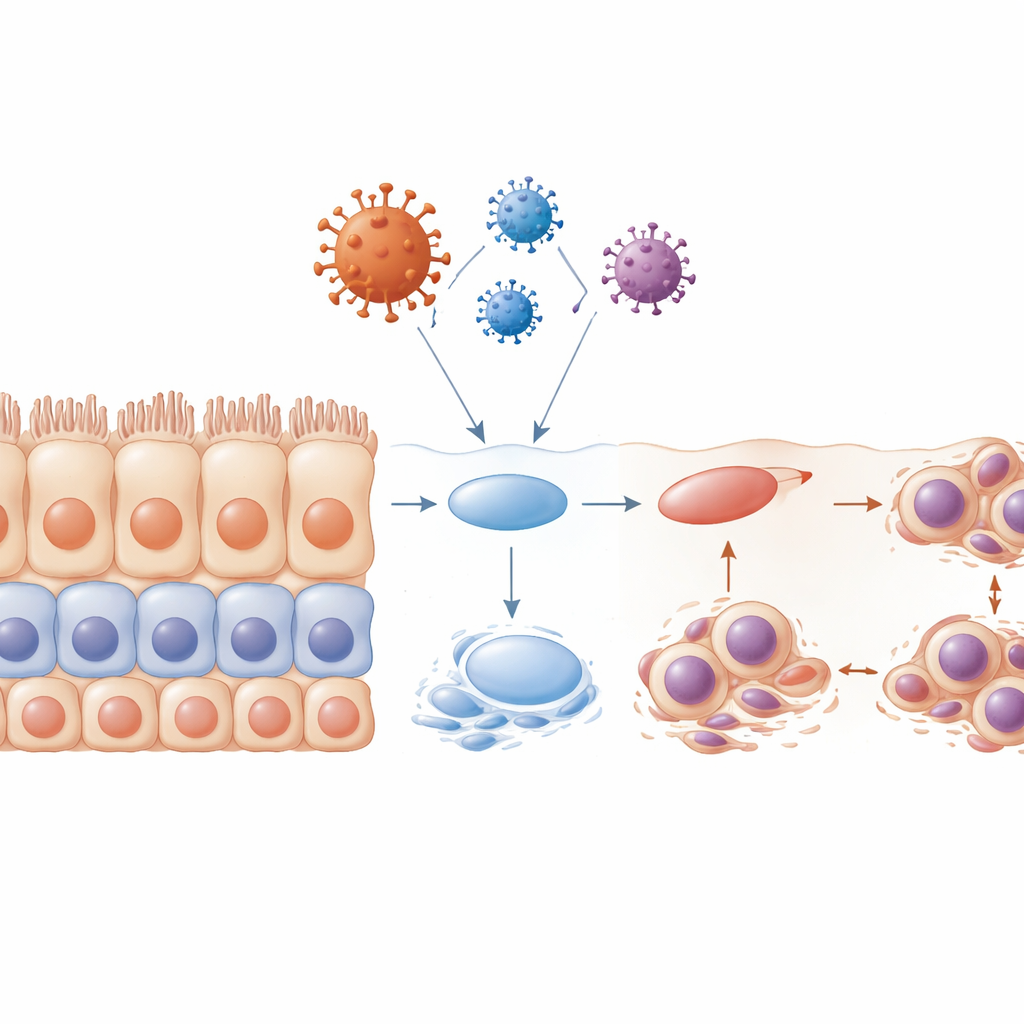
שיבוש השכבתיות ו"מברשות" תאיות פגועות
אפיתלים רב-שכבתי בריאים מתחדשים באמצעות תכנית מתואמת בקפידה: תאי אב מתחלקים קרוב לבסיס, ואז צאצאיהם נעים מעלה ומתמחים לתאים פני שטח מיוחדים מאוד. כשהצוות חשף תאים לחלבון המעטפת לפני שהיו להם שכבות מלאות, התכנית הזו התמוטטה למעשה. הרקמה שנוצרה הייתה בלתי מאורגנת, עם שכבתיות לקויה, פחות סמני בגרות והרבה תאים שנתקעו בשלב מוקדם של מחזור התא. רבים מהתאים הללו נשאו גרעינים מעוותים או מרובים ועברו אפופטוזה, והשאירו מרווחים במקום מחסום רציף. החוקרים גם בחנו מבנים זעירים דמויי שערות שנקראים ציליה, שעוזרות להזיז ריר ולנקות פסולת. הם מצאו שהציליות התקצרו או נעלמו, במיוחד תחת ההשפעה של חלבון המעטפת, ושזה קרה בשלבים מרכזיים של מחזור התא. אובדן הציליה הזה יחליש עוד יותר את יכולת הרקמה לנקות וירוסים ומזהמים.
מתג מולקולרי חבוי ויעד תרופות חדש
כדי לחשוף כיצד חלבונים ויראליים אלה מחזירים מחדש את התנהגות התאים, המחברים השוו את פרופילי החלבונים של תאים אפיתליאליים נגועים מול לא נגועים. מולקולה אחת, קלפונין 2 (CNN2), בלטה בעקביות: היא הוגברה בחוזקה על ידי כל שלושת חלבוני ה"לא-ספייק" והייתה מוגברת ברקמות הפה, הריאה והכליה של חולי COVID-19. CNN2 מסייעת לארגן את השלד התאי ומגיבה למתח מכני. כשהמדענים הפחיתו רמות CNN2 באמצעות כלים גנטיים ממוקדים, רבים מההשפעות המזיקות של חלבון המעטפת נחלשו: סמני אפיתל נשמרו, השכבתיות השתפרה וכמות התאים שמתו פחתה. הם אז עקבו אחרי ויסות CNN2 מעלה בשרשרת ונמצאו גורם שעתוק בשם GLIS2, שבדרך כלל שומר על CNN2 תחת שליטה. בדגימות מטופלים ובתאים שטופלו בחלבוני וירוס, רמות GLIS2 ירדו במידה ניכרת, מה ששחרר את הבלם על CNN2. ציר GLIS2–CNN2 הזה נראה כנתיב מרכזי שבו חלבוני מעטפת של SARS-CoV-2 מסטים את גורל התאים האפיתליאליים.
מה המשמעות לטיפול עתידי ב-COVID-19
למי שאינו מומחה, המסר המרכזי הוא ש-SARS-CoV-2 יכול לערער בשקט את הציפויים המגינים של הגוף זמן רב לפני שמופיע נזק רקמתי גלוי. חלבוני המבנה שאינם ספייק של הוירוס, ובמיוחד חלבון המעטפת, דוחפים תאי אפיתל בחזית לאבד את התמחותם, משבשים את השכבתיות הסדירה שלהם, פוגעים ב-DNA שלהם ומותרים אותם למוות. ברמה המולקולרית נראה שהוירוס מבצע "חטיפה כפולה": גם מייתר תאים בוגרים וגם חוסם את הבשלת תאי האב, בעיקר באמצעות מתג הבקרה GLIS2–CNN2. מכיוון של-CNN2 יש תפקיד מרכזי במסלול זה והפחתתו יכולה להפוך הרבה מהנזק במודלים מעבדתיים, הוא בולט כיעד מבטיח לטיפולים שמטרתם להגן על מחסומי הריר ב-COVID-19 ואולי להפחית כיבים עיקשים ופגיעה רב-אורגנית.
ציטוט: Gao, Y., Souza, L.L., Kang, H.S. et al. SARS-CoV-2 nonspike structural proteins hijack mucosa epithelial cell fate. Cell Death Dis 17, 340 (2026). https://doi.org/10.1038/s41419-026-08611-6
מילות מפתח: חלבון מעטפת של SARS-CoV-2, אפיתל רירי, דדיקרנטיפיקציה של תאים, CNN2, GLIS2