Clear Sky Science · de
SARS-CoV-2-Non-Spike-Strukturproteine kapern das Schicksal mukosaler Epithelzellen
Wenn die Auskleidungen des Körpers ihre Identität verlieren
COVID-19 ist vor allem für Angriffe auf die Lunge bekannt, doch viele Patientinnen und Patienten entwickeln auch hartnäckige Ulzera im Mund, Darm und in anderen Organen, die von empfindlichen Schleimhäuten ausgekleidet sind. Diese Studie stellt eine scheinbar einfache Frage: Was genau geschieht noch bevor sich sichtbare Wunden und Entzündungen zeigen mit den Zellen, die diese Schutzschichten bilden — und könnte dieser frühe Schaden auf neue Behandlungsstrategien hinweisen?
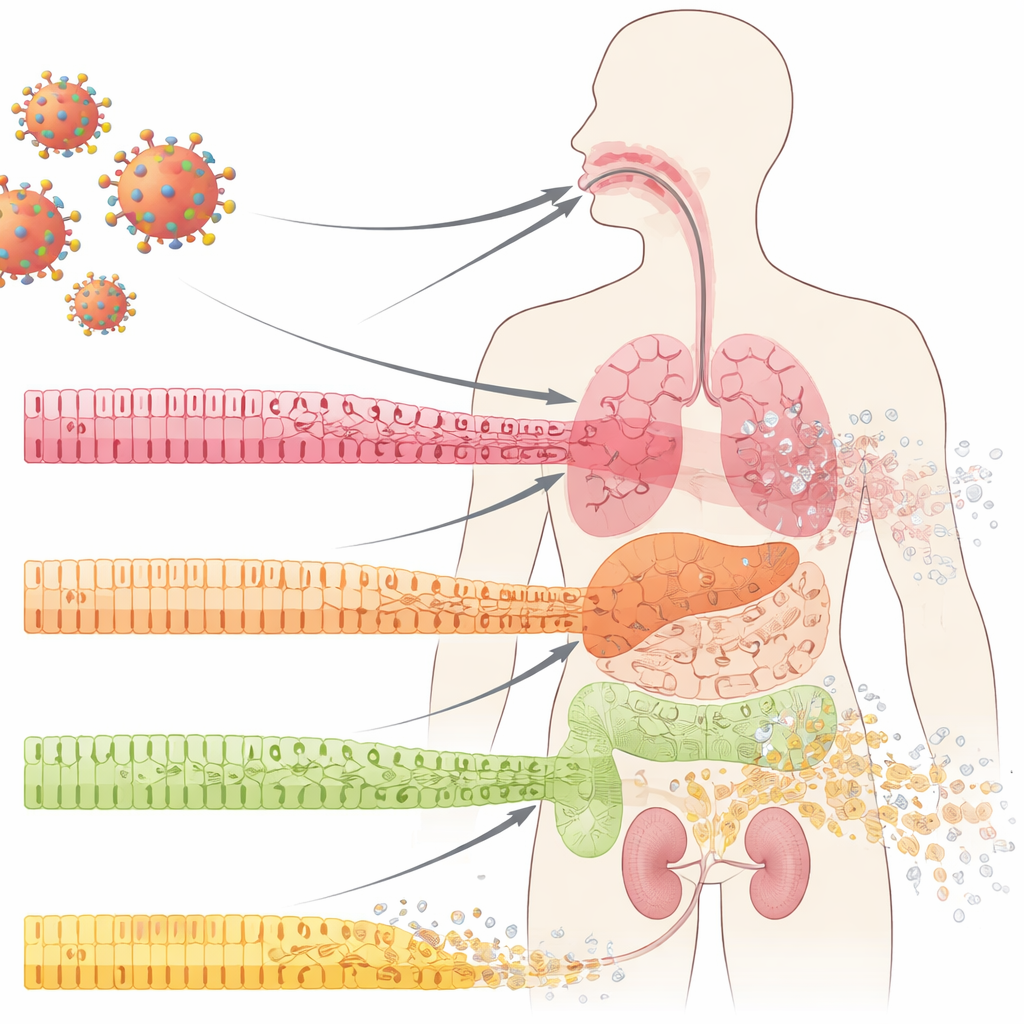
Die vordersten Zellen, die unsere Organe schützen
Unsere inneren Oberflächen — im Mund, in den Lungen, im Darm und in den Nieren — sind von Epithelzellen bedeckt, die in geordneten Schichten angeordnet sind. Diese Zellen funktionieren wie Fliesen einer wasserdichten Wand: eng verbunden, spezialisiert und ständig erneuert aus einem Pool darunter liegender Vorläuferzellen. Bei COVID-19 beobachteten Ärztinnen und Ärzte schon lange dramatische Zusammenbrüche dieser mukosalen Barrieren, einschließlich Ulzera und Gewebeerosion. Die Autorinnen und Autoren untersuchten Proben aus Mundhöhle, Lunge und Niere von COVID-19-Patienten und fanden etwas Auffälliges selbst in Bereichen, die bei Routineuntersuchungen noch normal aussahen: die ausgereiften, spezialisierten Zellen verloren ihre Identität, während Marker weniger reifer, „stammzellähnlicher“ Zellen zunahmen. Dieser Prozess, Dedifferenzierung genannt, tritt normalerweise bei kontrollierter Gewebereparatur auf — hier zeigte er sich jedoch früh in der Infektion, noch vor offensichtlicher Entzündung oder Narbenbildung.
Virale Hüllenproteine, die das Zellschicksal umprogrammieren
Das Coronavirus ist am bekanntesten für sein Spike-Protein, mit dem es in Zellen eindringt. Aber das Virus trägt auch andere Strukturproteine, die seine Hülle und sein Inneres bilden. In dieser Arbeit konzentrierten sich die Forschenden auf drei dieser „Nicht-Spike“-Proteine: Envelope (E), Membran (M) und Nukleokapsid (N). Mit ausgefeilten 3D-Modellen des menschlichen oralen Mukosaepithels und kultiviertem Mauszungengewebe lieferten sie jeweils diese Proteine in Epithelzellen, um zu beobachten, was geschieht. Alle drei konnten die Zellen in einen weniger differenzierten Zustand treiben, doch das Envelope-Protein fiel besonders auf. Es reduzierte schnell Marker reifer Epithelzellen, erhöhte Marker primitiverer Zellen und schwächte E-Cadherin, ein Molekül, das Zellen fest zusammenhält. Gleichzeitig zeigten Zellen DNA-Schadenssignale wie Mikrokerne, blieben an einem frühen Kontrollpunkt des Zellzyklus hängen und neigten eher zu programmierter Zellruhe (Apoptose). Zusammengenommen deuten diese Veränderungen darauf hin, dass die strukturelle Hülle des Virus nicht nur ein passiver Mantel ist, sondern aktiv die Stabilität des Epithels sabotiert.
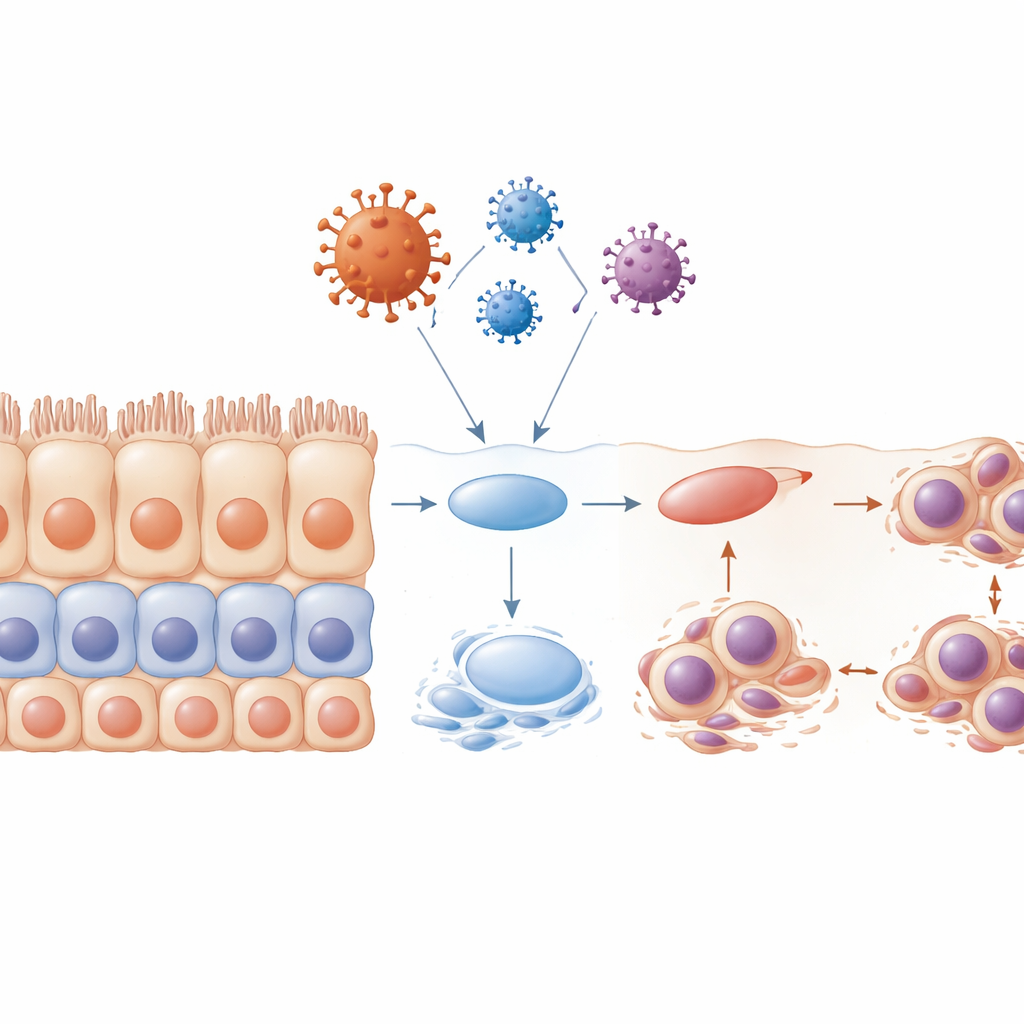
Gestörte Schichtung und beschädigte zelluläre „Bürsten“
Gesunde mehrschichtige Epithelien erneuern sich durch ein sorgfältig choreografiertes Programm: Vorläuferzellen teilen sich nahe der Basis, dann wandern ihre Nachkommen nach oben und reifen zu hochspezialisierten Oberflächenzellen heran. Wenn das Team Zellen dem Envelope-Protein aussetzte, bevor sie vollständige Schichten gebildet hatten, kollabierte dieses Programm im Wesentlichen. Das resultierende Gewebe war desorganisiert, mit schlechter Schichtung, weniger Reifungsmarkern und vielen Zellen, die in einer frühen Phase des Zellzyklus festsaßen. Viele dieser Zellen zeigten missgestaltete oder mehrere Zellkerne und gingen durch Apoptose zugrunde, wodurch Lücken entstanden, wo eine durchgehende Barriere bestehen sollte. Die Forschenden untersuchten auch winzige haarartige Strukturen, die Zilien, welche helfen, Schleim und Partikel zu bewegen. Sie stellten fest, dass Zilien schrumpften oder verschwanden, besonders unter dem Einfluss des Envelope-Proteins, und dass dies in kritischen Phasen des Zellzyklus auftrat. Dieser Zilienschwund würde die Fähigkeit des Gewebes weiter schwächen, Viren und Verunreinigungen zu entfernen.
Ein verborgener molekularer Schalter und ein neues Wirkstoffziel
Um zu klären, wie diese viralen Proteine das Zellverhalten umschreiben, verglichen die Autorinnen und Autoren die Proteinprofile infizierter und nicht infizierter Epithelzellen. Ein Molekül stach konstant hervor: Calponin 2 (CNN2) — es wurde durch alle drei Nicht-Spike-Proteine stark erhöht und war in Mund-, Lungen- und Nierengewebe von COVID-19-Patienten erhöht. CNN2 hilft, das interne Gerüst der Zelle zu organisieren und reagiert auf mechanischen Stress. Als die Forschenden CNN2 mit gezielten genetischen Werkzeugen reduzierten, wurden viele schädliche Effekte des Envelope-Proteins abgeschwächt: Epithelmarker blieben erhalten, die Gewebsschichtung verbesserte sich und weniger Zellen starben ab. Sie verfolgten die Regulierung von CNN2 weiter stromaufwärts zu einem Transkriptionsfaktor namens GLIS2, der CNN2 normalerweise in Schach hält. In Patientenproben und in Zellen, die mit Virusproteinen behandelt wurden, waren GLIS2-Werte deutlich vermindert, wodurch die Bremse auf CNN2 gelöst wurde. Diese GLIS2–CNN2-Achse scheint ein Schlüsselweg zu sein, über den die Hüllenproteine von SARS-CoV-2 das Schicksal von Epithelzellen entgleisen lassen.
Was das für die zukünftige COVID-19-Versorgung bedeutet
Für Nicht-Fachleute lautet die Kernbotschaft: SARS-CoV-2 kann die schützenden Auskleidungen des Körpers still und leise destabilisieren, lange bevor offensichtliche Gewebeschäden sichtbar werden. Seine nicht-Spike-Strukturproteine, insbesondere das Envelope-Protein, treiben die vordersten Epithelzellen dazu, ihre Spezialisierung zu verlieren, stören ihre geordnete Schichtung, beschädigen ihre DNA und führen sie zum Absterben. Auf molekularer Ebene scheint das Virus einen „doppelten Kapervorgang“ auszuführen: Es dedifferenziert ausgereifte Zellen und blockiert gleichzeitig die normale Reifung der Vorläuferzellen — größtenteils über einen GLIS2–CNN2-Kontrollschalter. Weil CNN2 an einem entscheidenden Punkt in diesem Weg sitzt und seine Reduktion in Labor‑Modellen einen Großteil des Schadens rückgängig machen kann, stellt es ein vielversprechendes Ziel für Therapien dar, die mukosale Barrieren bei COVID-19 schützen und möglicherweise hartnäckige Ulzera sowie multiorganische Schäden verringern sollen.
Zitation: Gao, Y., Souza, L.L., Kang, H.S. et al. SARS-CoV-2 nonspike structural proteins hijack mucosa epithelial cell fate. Cell Death Dis 17, 340 (2026). https://doi.org/10.1038/s41419-026-08611-6
Schlüsselwörter: SARS-CoV-2 Hüllprotein, muköses Epithel, Zelldedifferenzierung, CNN2, GLIS2