Clear Sky Science · pt
Proteínas estruturais não spike do SARS-CoV-2 sequestram o destino das células epiteliais da mucosa
Quando os Revestimentos do Corpo Perdem sua Identidade
Conhecida por atacar os pulmões, a COVID-19 também provoca em muitos pacientes úlceras persistentes na boca, no intestino e em outros órgãos revestidos por membranas mucosas delicadas. Este estudo faz uma pergunta aparentemente simples: antes de vermos feridas visíveis e inflamação, o que exatamente está acontecendo com as células que formam esses revestimentos protetores — e esse dano inicial poderia apontar para novas estratégias terapêuticas?
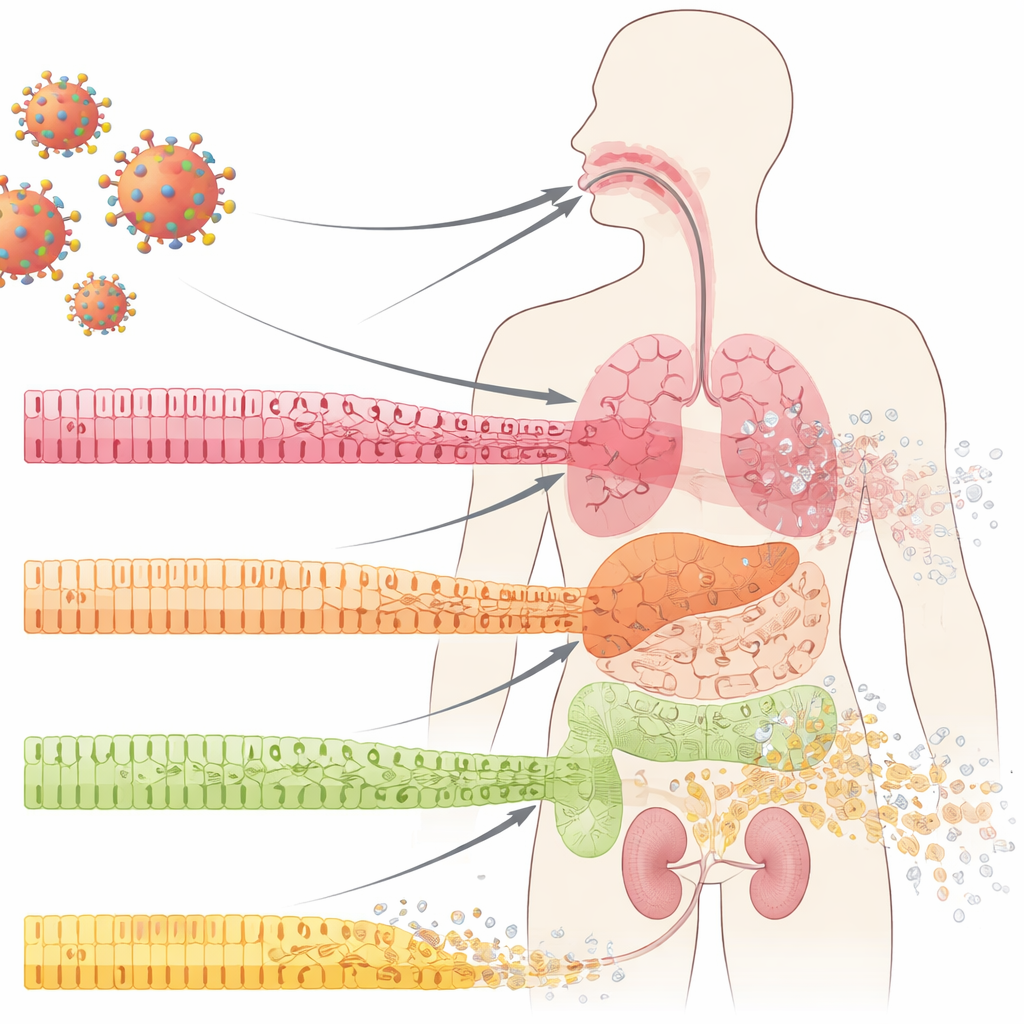
As Células de Primeira Linha que Protegem Nossos Órgãos
As superfícies internas — dentro da boca, dos pulmões, dos intestinos e dos rins — são cobertas por células epiteliais organizadas em camadas ordenadas. Essas células funcionam como azulejos em uma parede impermeável: firmemente unidas, especializadas e em renovação constante a partir de um reservatório de células progenitoras subjacentes. Na COVID-19, médicos há muito tempo notam colapsos dramáticos dessas barreiras mucosas, incluindo úlceras e erosão de tecido. Os autores examinaram amostras da cavidade oral, pulmões e rins de pacientes com COVID-19 e encontraram algo marcante mesmo em áreas que ainda pareciam normais na inspeção de rotina: as células maduras e especializadas estavam perdendo sua identidade, e marcadores de células menos maduras, “semelhantes a células-tronco”, aumentavam. Esse processo, chamado dediferenciação, geralmente aparece durante reparo tecidual controlado — mas aqui surgia cedo na infecção, antes de inflamação ou cicatrização óbvias.
Proteínas da Casca Viral que Reprogramam o Destino Celular
O coronavírus é mais conhecido por sua proteína spike, usada para entrar nas células. Mas o vírus também carrega outras proteínas estruturais que formam sua casca e interior. Neste trabalho, os pesquisadores focaram em três dessas proteínas “não spike”: envelope (E), membrana (M) e nucleocapsídeo (N). Usando modelos 3D sofisticados de mucosa oral humana e tecido de língua de camundongo em cultura, eles introduziram cada uma dessas proteínas em células epiteliais para observar o que aconteceria. As três podiam impulsionar as células para um estado menos diferenciado, mas a proteína envelope se destacou. Ela reduziu rapidamente marcadores de células epiteliais maduras, aumentou marcadores de células mais primitivas e enfraqueceu a E-caderina, uma molécula que ajuda as células a se aderirem firmemente umas às outras. Ao mesmo tempo, as células começaram a mostrar sinais de dano ao DNA, como micronúcleos, ficaram retidas em um ponto de checagem inicial do ciclo celular e tinham maior probabilidade de sofrer morte celular programada. Juntas, essas mudanças sugerem que a casca estrutural do vírus não é apenas um invólucro passivo, mas um sabotador ativo da estabilidade epitelial.
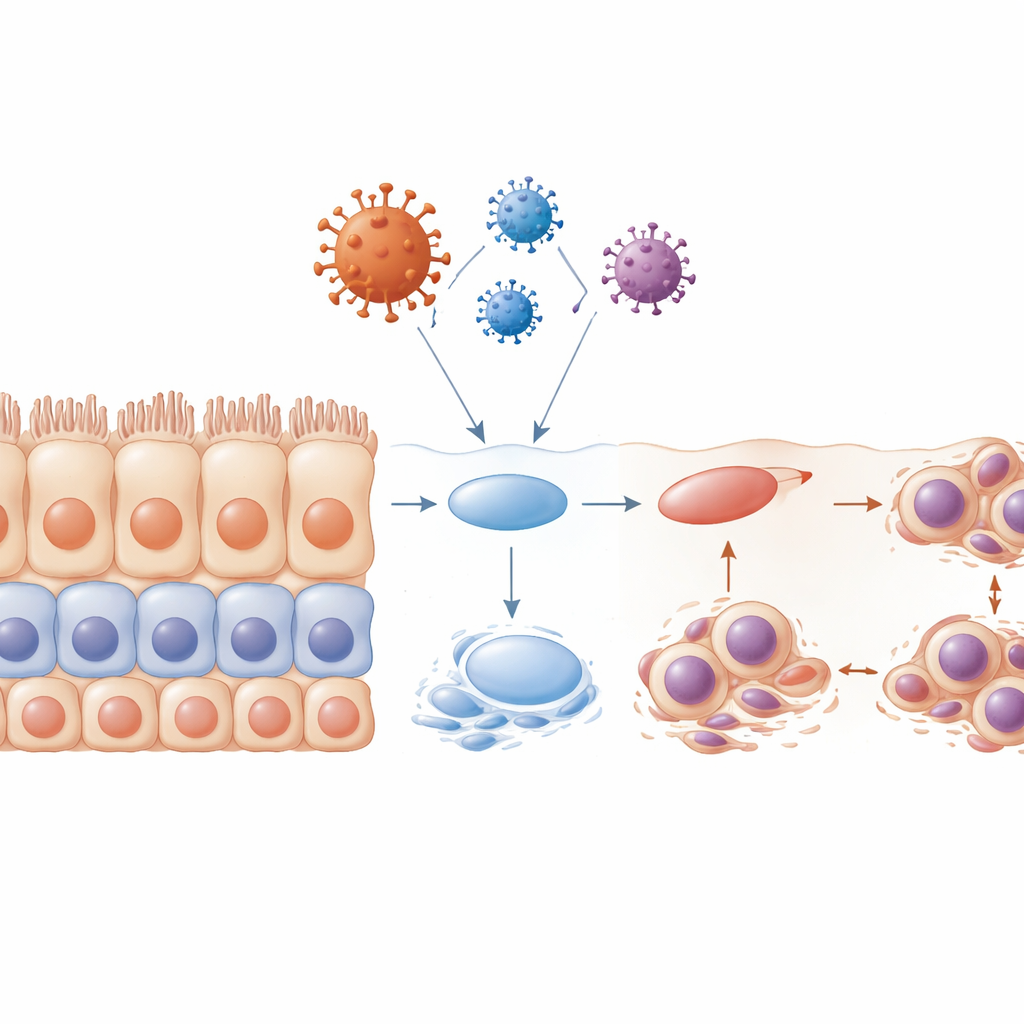
Desorganização em Camadas e Danos aos “Pincéis” Celulares
Epitélios estratificados saudáveis se renovam através de um programa cuidadosamente coreografado: células progenitoras dividem-se perto da base, depois seus descendentes migram para cima e se maturam em células de superfície altamente especializadas. Quando a equipe expôs células à proteína envelope antes que tivessem formado camadas completas, esse programa entrou em colapso. O tecido resultante ficou desorganizado, com camadas pobres, menos marcadores de maturidade e muitas células presas em uma fase inicial do ciclo celular. Muitas dessas células apresentavam núcleos malformados ou múltiplos e entraram em apoptose, deixando lacunas onde deveria haver uma barreira contínua. Os pesquisadores também examinaram estruturas minúsculas em forma de cabelo chamadas cílios, que ajudam a mover muco e detritos. Eles observaram que os cílios encolheram ou desapareceram, especialmente sob a influência da proteína envelope, e que isso ocorreu em estágios-chave do ciclo celular. Essa perda de cílios enfraqueceria ainda mais a capacidade do tecido de eliminar vírus e contaminantes.
Um Interruptor Molecular Oculto e um Novo Alvo Farmacológico
Para descobrir como essas proteínas virais reprogramam o comportamento celular, os autores compararam os perfis proteicos de células epiteliais infectadas e não infectadas. Uma molécula, calponina 2 (CNN2), destacou-se consistentemente: foi fortemente aumentada por todas as três proteínas não spike e estava elevada nos tecidos orais, pulmonares e renais de pacientes com COVID-19. A CNN2 ajuda a organizar o arcabouço interno da célula e responde ao estresse mecânico. Quando os cientistas reduziram os níveis de CNN2 usando ferramentas genéticas direcionadas, muitos dos efeitos nocivos da proteína envelope foram atenuados: marcadores epiteliais foram preservados, a estratificação tecidual melhorou e menos células morreram. Em seguida, rastrearam a regulação da CNN2 a montante até um fator de transcrição chamado GLIS2, que normalmente reprime a CNN2. Em amostras de pacientes e em células tratadas com proteínas virais, os níveis de GLIS2 estavam visivelmente reduzidos, liberando o freio sobre a CNN2. Esse eixo GLIS2–CNN2 parece ser uma via-chave através da qual as proteínas da casca do SARS-CoV-2 desvirtuam o destino das células epiteliais.
O que Isso Significa para o Cuidado Futuro da COVID-19
Para um não especialista, a mensagem central é que o SARS-CoV-2 pode desestabilizar silenciosamente os revestimentos protetores do corpo muito antes de surgir dano tecidual óbvio. Suas proteínas estruturais não spike, especialmente a proteína envelope, fazem com que células epiteliais de linha de frente percam sua especialização, desorganizem sua estratificação, danifiquem seu DNA e entrem em morte celular. No nível molecular, o vírus parece executar um “duplo sequestro”: dediferencia células maduras e bloqueia a maturação normal das células progenitoras, em grande parte por meio de um controle GLIS2–CNN2. Como a CNN2 ocupa um ponto crucial nessa via e sua redução pode reverter grande parte do dano em modelos de laboratório, ela surge como um alvo promissor para terapias destinadas a proteger as barreiras mucosas na COVID-19 e possivelmente reduzir úlceras persistentes e lesão multiorgânica.
Citação: Gao, Y., Souza, L.L., Kang, H.S. et al. SARS-CoV-2 nonspike structural proteins hijack mucosa epithelial cell fate. Cell Death Dis 17, 340 (2026). https://doi.org/10.1038/s41419-026-08611-6
Palavras-chave: proteína envelope do SARS-CoV-2, epitélio mucoso, dediferenciação celular, CNN2, GLIS2