Clear Sky Science · fr
Les protéines structurelles non-spike du SARS-CoV-2 détournent le destin des cellules épithéliales des muqueuses
Quand les revêtements du corps perdent leur identité
La COVID-19 est surtout connue pour attaquer les poumons, mais de nombreux patients développent aussi des ulcères tenaces dans la bouche, l’intestin et d’autres organes tapissés de muqueuses fragiles. Cette étude pose une question apparemment simple : avant l’apparition de lésions et d’inflammation visibles, que se passe-t-il exactement au niveau des cellules qui constituent ces barrières protectrices — et ces atteintes précoces pourraient-elles révéler de nouvelles pistes thérapeutiques ?
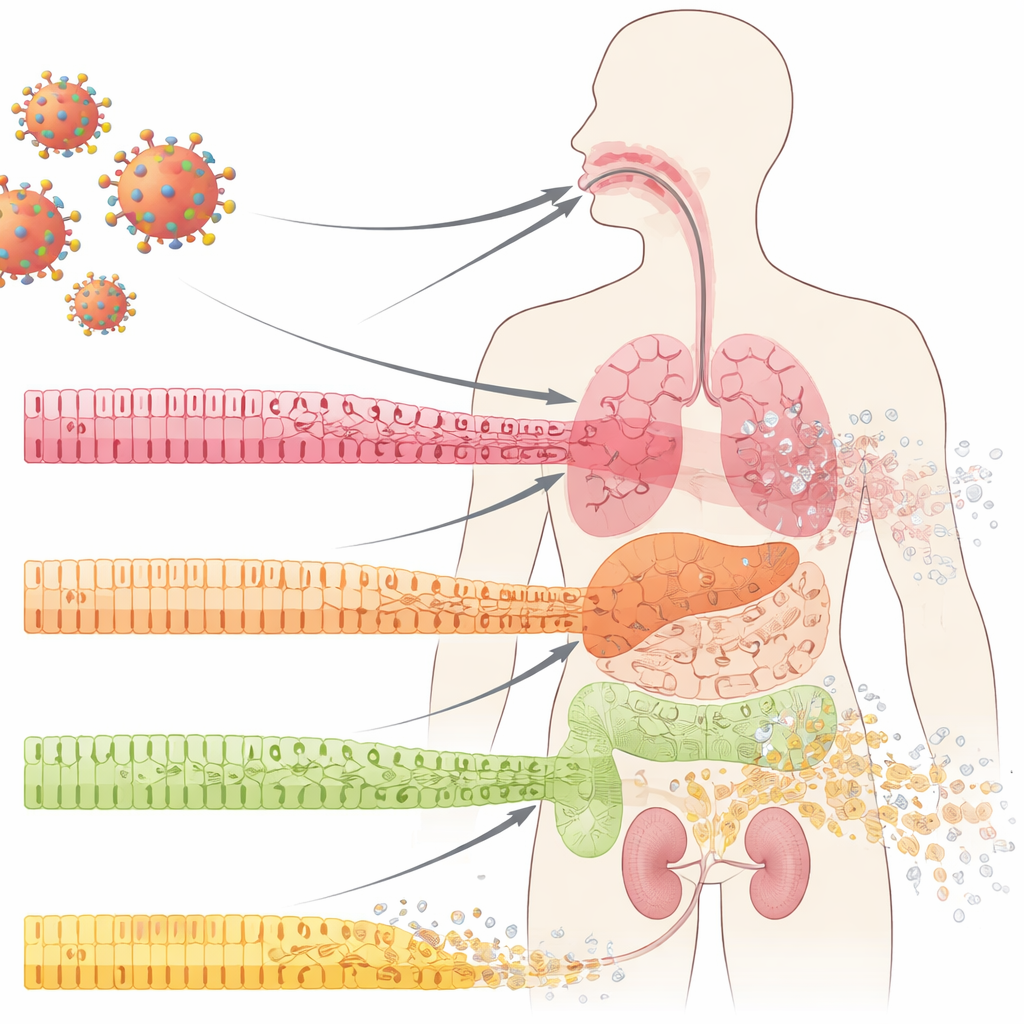
Les cellules de première ligne qui protègent nos organes
Nos surfaces internes — à l’intérieur de la bouche, des poumons, des intestins et des reins — sont recouvertes d’un épithélium formé de cellules organisées en couches régulières. Ces cellules fonctionnent comme des carreaux d’un mur étanche : fortement liées entre elles, spécialisées et renouvelées en permanence à partir d’un réservoir de cellules progénitrices sous-jacent. Dans la COVID-19, les cliniciens ont depuis longtemps observé des effondrements dramatiques de ces barrières muqueuses, notamment des ulcérations et une érosion tissulaire. Les auteurs ont analysé des prélèvements de la cavité buccale, des poumons et des reins de patients atteints de COVID-19 et ont trouvé quelque chose de frappant même dans des zones qui semblaient normales à l’inspection de routine : les cellules matures et spécialisées perdaient leur identité, tandis que des marqueurs de cellules moins matures, « semblables à des cellules souches », augmentaient. Ce processus, appelé dédifférenciation, apparaît habituellement lors de la réparation tissulaire contrôlée — mais ici, il survenait tôt dans l’infection, avant toute inflammation ou cicatrisation évidente.
Des protéines de la coque virale qui reprogramment le destin cellulaire
Le coronavirus est surtout connu pour sa protéine Spike, qu’il utilise pour pénétrer dans les cellules. Mais le virus porte aussi d’autres protéines structurelles qui forment son enveloppe et son intérieur. Dans ce travail, les chercheurs se sont concentrés sur trois de ces protéines « non-spike » : l’enveloppe (E), la membrane (M) et la nucléocapside (N). En utilisant des modèles 3D sophistiqués de la muqueuse orale humaine et des tissus de langue de souris en culture, ils ont introduit chacune de ces protéines dans des cellules épithéliales pour observer les effets. Les trois pouvaient pousser les cellules vers un état moins différencié, mais la protéine d’enveloppe s’est démarquée. Elle a rapidement diminué les marqueurs des cellules épithéliales matures, augmenté ceux des cellules plus primitives et affaibli l’E-cadhérine, une molécule qui aide les cellules à rester fortement adhérées les unes aux autres. Parallèlement, les cellules ont montré des signes de dommages à l’ADN tels que des micronoyaux, se sont retrouvées bloquées à un point de contrôle précoce du cycle cellulaire et ont été plus susceptibles de subir une mort cellulaire programmée. Ensemble, ces modifications suggèrent que la coque structurelle du virus n’est pas qu’un simple revêtement passif, mais un saboteur actif de la stabilité épithéliale.
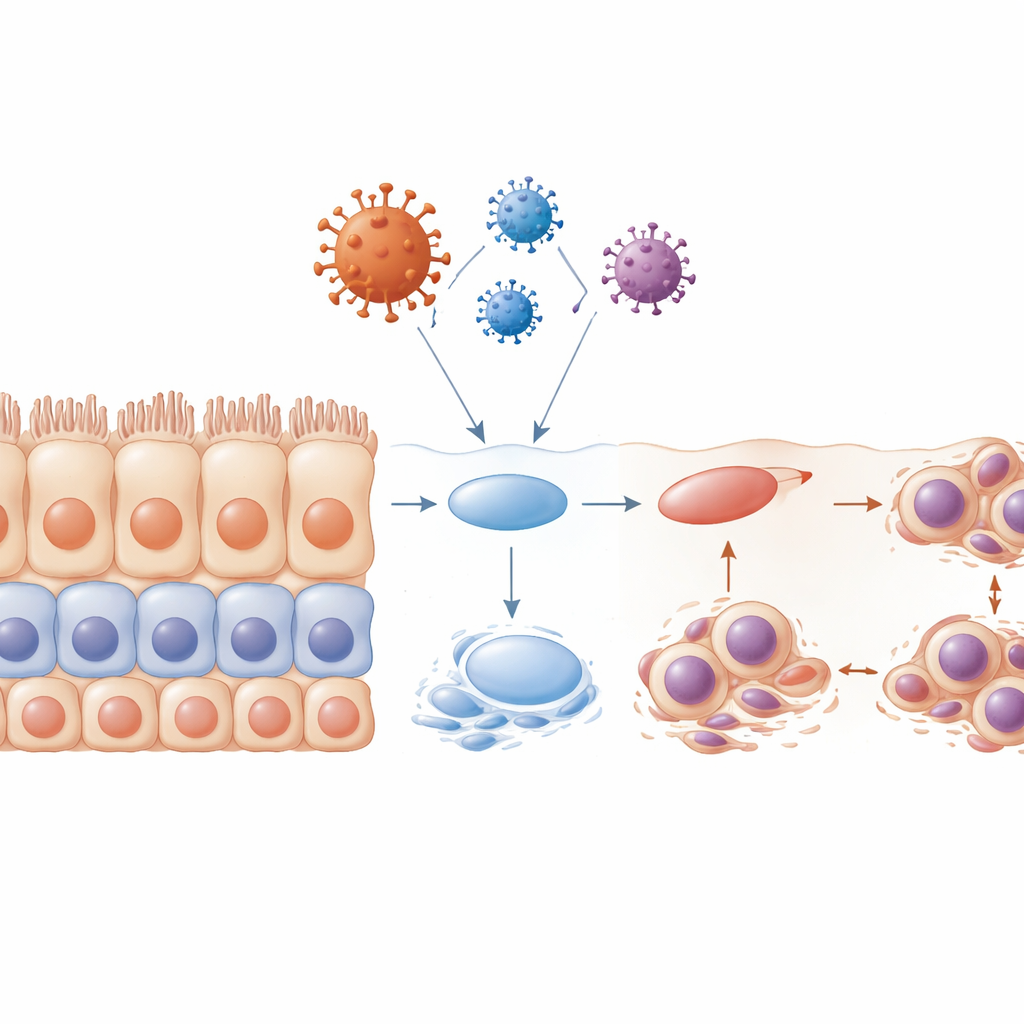
Des couches perturbées et des « brosses » cellulaires endommagées
Les épithéliums stratifiés sains se renouvellent selon un programme finement orchestré : les cellules progénitrices se divisent près de la base, puis leurs descendants montent vers la surface et se spécialisent en cellules fortement différenciées. Lorsque l’équipe a exposé des cellules à la protéine d’enveloppe avant la formation complète des couches, ce programme s’est effondré. Le tissu résultant était désorganisé, avec un mauvais empilement des couches, moins de marqueurs de maturité et de nombreuses cellules coincées dans une phase précoce du cycle cellulaire. Beaucoup portaient des noyaux malformés ou multiples et entraient en apoptose, laissant des zones dépourvues là où une barrière continue devrait exister. Les chercheurs ont également examiné de minuscules structures en forme de poils appelées cils, qui contribuent à déplacer le mucus et les débris. Ils ont constaté que les cils s’atrophiaient ou disparaissaient, surtout sous l’influence de la protéine d’enveloppe, et que cela se produisait à des étapes clés du cycle cellulaire. Cette perte de cils affaiblirait encore la capacité du tissu à éliminer virus et contaminants.
Un interrupteur moléculaire caché et une nouvelle cible médicamenteuse
Pour comprendre comment ces protéines virales reconfiguraient le comportement cellulaire, les auteurs ont comparé les profils protéiques des cellules épithéliales infectées et non infectées. Une molécule, la calponine 2 (CNN2), est apparue de façon récurrente : elle était fortement augmentée par les trois protéines non-spike et retrouvée élevée dans les tissus buccaux, pulmonaires et rénaux des patients COVID-19. CNN2 aide à organiser le cytosquelette cellulaire et répond aux contraintes mécaniques. Lorsque les scientifiques ont réduit les niveaux de CNN2 à l’aide d’outils génétiques ciblés, beaucoup des effets délétères de la protéine d’enveloppe ont été atténués : les marqueurs épithéliaux ont été préservés, la stratification tissulaire s’est améliorée et moins de cellules sont mortes. Ils ont ensuite tracé la régulation de CNN2 en amont jusqu’à un facteur de transcription appelé GLIS2, qui contrôle normalement l’expression de CNN2. Dans les échantillons de patients et dans les cellules traitées par les protéines virales, les niveaux de GLIS2 étaient nettement diminués, relâchant la contrainte sur CNN2. Cet axe GLIS2–CNN2 semble être une voie clé par laquelle les protéines de coque du SARS-CoV-2 détournent le destin des cellules épithéliales.
Ce que cela implique pour la prise en charge future de la COVID-19
Pour un non-spécialiste, le message essentiel est que le SARS-CoV-2 peut déstabiliser discrètement les revêtements protecteurs du corps bien avant l’apparition de dégâts tissulaires évidents. Ses protéines structurelles non-spike, en particulier la protéine d’enveloppe, poussent les cellules épithéliales de première ligne à perdre leur spécialisation, perturbent leur organisation en couches, endommagent leur ADN et provoquent leur disparition. Au niveau moléculaire, le virus semble exercer un « double détournement » : il dédifférencie les cellules matures et bloque la maturation normale des progéniteurs, en grande partie via un commutateur de contrôle GLIS2–CNN2. Parce que CNN2 occupe un point crucial de cette voie et que sa réduction peut inverser une grande partie des dommages dans des modèles de laboratoire, il émerge comme une cible prometteuse pour des thérapies visant à protéger les barrières muqueuses dans la COVID-19 et potentiellement réduire les ulcères tenaces et les atteintes multi-organes.
Citation: Gao, Y., Souza, L.L., Kang, H.S. et al. SARS-CoV-2 nonspike structural proteins hijack mucosa epithelial cell fate. Cell Death Dis 17, 340 (2026). https://doi.org/10.1038/s41419-026-08611-6
Mots-clés: protéine d’enveloppe du SARS-CoV-2, épithélium muqueux, dédifférenciation cellulaire, CNN2, GLIS2