Clear Sky Science · it
Proteine strutturali non spike di SARS-CoV-2 dirottano il destino delle cellule epiteliali mucosali
Quando le mucose perdono la propria identità
Il COVID-19 è noto per colpire i polmoni, ma molti pazienti sviluppano anche ulcere ostinate in bocca, intestino e altri organi rivestiti da fragili membrane mucose. Questo studio pone una domanda apparentemente semplice: prima che compaiano ferite visibili e infiammazione, cosa succede esattamente alle cellule che formano questi rivestimenti protettivi — e potrebbe quel danno precoce indicare nuove strategie terapeutiche?
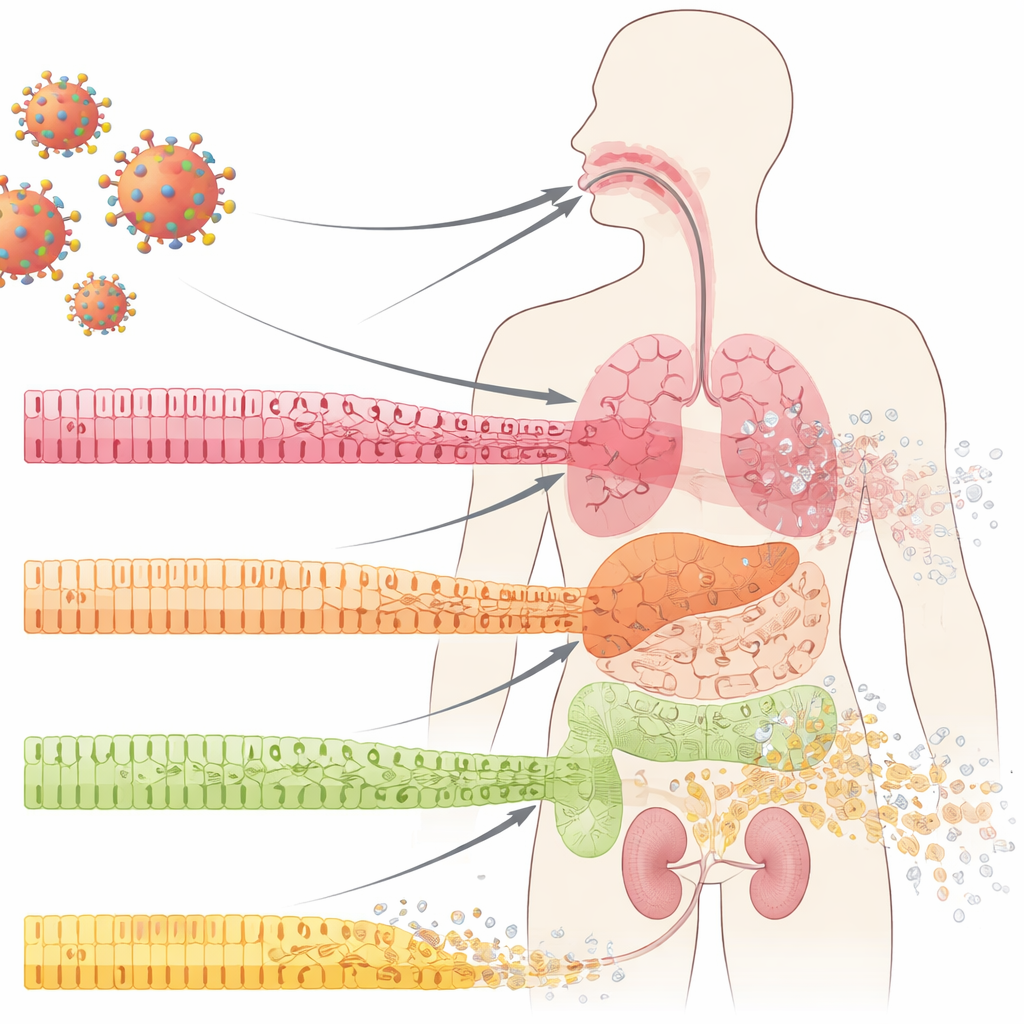
Le cellule in prima linea che proteggono i nostri organi
Le nostre superfici interne — all’interno della bocca, dei polmoni, dell’intestino e dei reni — sono coperte da cellule epiteliali disposte in strati ordinati. Queste cellule funzionano come piastrelle in una parete impermeabile: saldamente connesse, specializzate e in costante rinnovamento da un serbatoio di cellule progenitrici sottostanti. Nel COVID-19 i medici hanno da tempo osservato crolli drammatici di queste barriere mucose, incluse ulcere ed erosione tissutale. Gli autori hanno esaminato campioni della cavità orale, dei polmoni e dei reni di pazienti COVID-19 e hanno trovato qualcosa di sorprendente anche in aree che apparivano normali all’ispezione di routine: le cellule mature e specializzate stavano perdendo la loro identità e aumentavano i marcatori di cellule meno mature, «simili a staminali». Questo processo, chiamato dedifferenziazione, compare di solito durante la riparazione tissutale controllata — ma qui emergeva precocemente nell’infezione, prima di evidente infiammazione o cicatrizzazione.
Proteine del rivestimento virale che riprogrammano il destino cellulare
Il coronavirus è più noto per la sua proteina spike, che usa per entrare nelle cellule. Ma il virus porta anche altre proteine strutturali che costituiscono il suo involucro e il suo interno. In questo lavoro i ricercatori si sono concentrati su tre di queste proteine «non spike»: envelope (E), membrane (M) e nucleocapside (N). Utilizzando modelli 3D sofisticati della mucosa orale umana e tessuto linguale murino coltivato, hanno introdotto ciascuna di queste proteine nelle cellule epiteliali per osservare gli effetti. Tutte e tre potevano spingere le cellule verso uno stato meno differenziato, ma la proteina envelope si è distinta. Essa riduceva rapidamente i marcatori delle cellule epiteliali mature, aumentava i marcatori di cellule più primitive e indeboliva l’E-caderina, una molecola che aiuta le cellule ad aderire strettamente. Contemporaneamente, le cellule mostravano segnali di danno al DNA come micronuclei, restavano bloccate a un punto di controllo precoce del ciclo cellulare e avevano una maggiore probabilità di andare incontro ad apoptosi. Nel complesso, questi cambiamenti suggeriscono che l’involucro strutturale del virus non è solo un rivestimento passivo ma un sabotatore attivo della stabilità epiteliale.
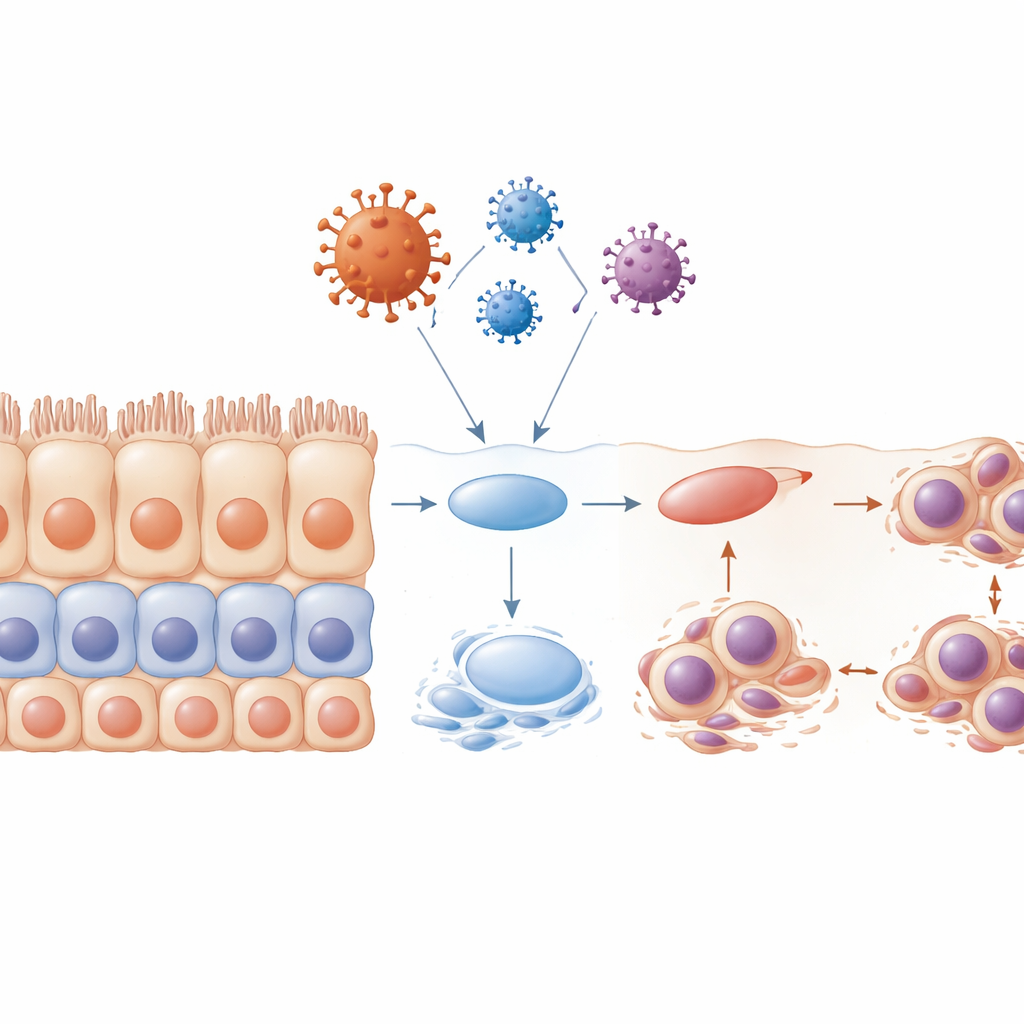
Disorganizzazione degli strati e danno alle «setole» cellulari
Gli epiteli stratificati sani si rinnovano tramite un programma attentamente coreografato: le cellule progenitrici si dividono vicino alla base, poi i loro discendenti si spostano verso l’alto e maturano in cellule di superficie altamente specializzate. Quando il team ha esposto le cellule alla proteina envelope prima che si fossero formati strati completi, questo programma è sostanzialmente collassato. Il tessuto risultante era disorganizzato, con scarsa stratificazione, meno marcatori di maturità e molte cellule intrappolate in una fase precoce del ciclo cellulare. Molte di queste cellule presentavano nuclei deformi o multipli e andavano incontro ad apoptosi, lasciando lacune dove dovrebbe esserci una barriera continua. I ricercatori hanno anche esaminato piccole strutture filamentose chiamate ciglia, che aiutano a muovere muco e detriti. Hanno riscontrato che le ciglia si rimpicciolivano o scomparivano, soprattutto sotto l’influsso della proteina envelope, e che ciò avveniva in fasi chiave del ciclo cellulare. Questa perdita di ciglia indebolirebbe ulteriormente la capacità del tessuto di rimuovere virus e contaminanti.
Un interruttore molecolare nascosto e un nuovo bersaglio farmacologico
Per scoprire come queste proteine virali riorientano il comportamento cellulare, gli autori hanno confrontato i profili proteici di cellule epiteliali infette rispetto a quelle non infette. Una molecola, calponina 2 (CNN2), è emersa con costanza: veniva fortemente aumentata da tutte e tre le proteine non spike ed era elevata nei tessuti orali, polmonari e renali dei pazienti COVID-19. CNN2 aiuta a organizzare lo scheletro interno della cellula e risponde allo stress meccanico. Quando gli scienziati hanno ridotto i livelli di CNN2 con strumenti genetici mirati, molti degli effetti dannosi della proteina envelope sono stati attenuati: i marcatori epiteliali sono stati preservati, la stratificazione tissutale è migliorata e meno cellule sono morte. Hanno quindi ricostruito la regolazione a monte di CNN2 fino a un fattore di trascrizione chiamato GLIS2, che normalmente tiene CNN2 sotto controllo. Nei campioni dei pazienti e nelle cellule trattate con le proteine virali, i livelli di GLIS2 erano visibilmente diminuiti, rilasciando così il freno su CNN2. Questo asse GLIS2–CNN2 sembra essere una via chiave attraverso cui le proteine dell’involucro di SARS-CoV-2 deviano il destino delle cellule epiteliali.
Cosa significa per la cura futura del COVID-19
Per un non specialista, il messaggio centrale è che SARS-CoV-2 può destabilizzare silenziosamente i rivestimenti protettivi del corpo molto prima che compaia un danno tissutale evidente. Le sue proteine strutturali non spike, in particolare la proteina envelope, spingono le cellule epiteliali in prima linea a perdere la loro specializzazione, a disorganizzare la stratificazione, a danneggiare il DNA e a morire. A livello molecolare, il virus sembra eseguire un «doppio dirottamento»: dedifferenzia le cellule mature e blocca la normale maturazione delle cellule progenitrici, in gran parte attraverso un interruttore di controllo GLIS2–CNN2. Poiché CNN2 occupa un punto cruciale in questa via e la sua riduzione può invertire gran parte del danno nei modelli di laboratorio, emerge come un potenziale obiettivo per terapie mirate a proteggere le barriere mucose nel COVID-19 e possibilmente a ridurre ulcere persistenti e lesioni multi-organo.
Citazione: Gao, Y., Souza, L.L., Kang, H.S. et al. SARS-CoV-2 nonspike structural proteins hijack mucosa epithelial cell fate. Cell Death Dis 17, 340 (2026). https://doi.org/10.1038/s41419-026-08611-6
Parole chiave: proteina envelope di SARS-CoV-2, epitelio mucoso, dedifferenziazione cellulare, CNN2, GLIS2