Clear Sky Science · sv
SARS-CoV-2:s icke-spikade strukturella proteiner kapar mucosala epitelcellers öde
När kroppens beklädnader förlorar sin identitet
COVID-19 är känt för att angripa lungorna, men många patienter utvecklar också envisa sår i munnen, tarmen och andra organ som är täckta av känsliga slemhinnor. Denna studie ställer en förvillelse enkelt formulerad fråga: innan synliga sår och inflammation uppstår, vad händer exakt med de celler som bildar dessa skyddande ytor — och skulle den tidiga skadan kunna peka mot nya behandlingsstrategier?
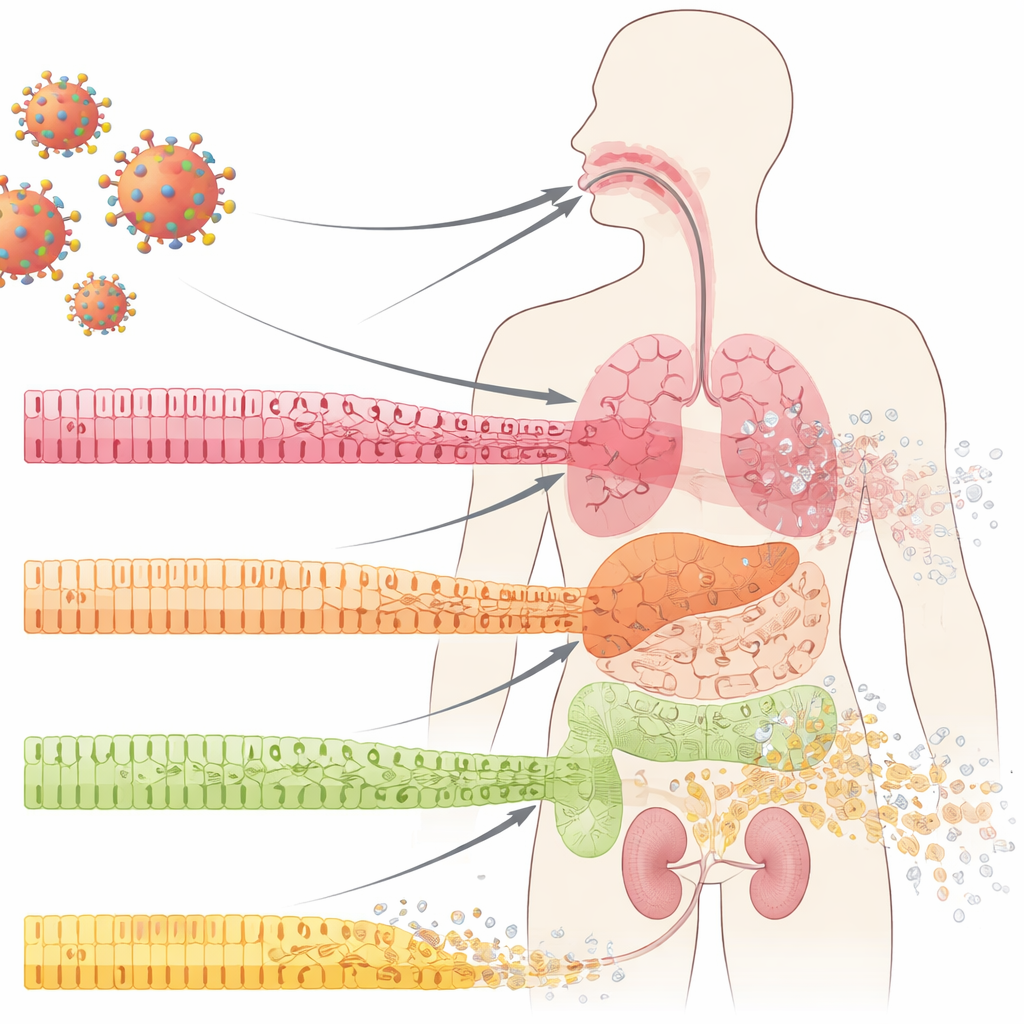
Frontcellsbarriärerna som skyddar våra organ
Våra inre ytor — inne i munnen, lungorna, tarmarna och njurarna — är täckta av epitelceller ordnade i organiserade lager. Dessa celler fungerar som kakel i en vattentät vägg: tätt sammanfogade, specialiserade och ständigt förnyande från en underliggande pool av progenitorceller. Vid COVID-19 har läkare länge observerat dramatiska förluster av dessa mukosala barriärer, inklusive sår och vävnadserosion. Författarna undersökte prover från munhåla, lungor och njurar hos COVID-19-patienter och fann något anmärkningsvärt även i områden som fortfarande såg normala ut vid rutinundersökning: de mogna, specialiserade cellerna förlorade sin identitet, och markörer för mindre mogna, ”stamliknande” celler ökade. Denna process, kallad dedifferentiering, uppstår normalt vid kontrollerad vävnadsreparation — men här visade den sig tidigt i infektionen, före uppenbar inflammation eller ärrbildning.
Virusets skalproteiner som omskolar cellödet
Coronaviruset är mest känt för sitt spikeprotein, som det använder för att tränga in i celler. Men viruset bär också andra strukturella proteiner som utgör dess skal och inre. I detta arbete fokuserade forskarna på tre av dessa ”icke-spikade” proteiner: envelope (E), membrane (M) och nucleocapsid (N). Med hjälp av avancerade 3D-modeller av mänsklig oral mukosa och odlade mus-svampyrstunga vävnader levererade de vart och ett av dessa proteiner i epitelceller för att se vad som skulle hända. Alla tre kunde driva cellerna mot ett mindre differentierat tillstånd, men envelope-proteinet stack ut. Det minskade snabbt markörer för mogna epitelceller, ökade markörer för mer primitiva celler och försvagade E-kadherin, ett molekylärt lim som får celler att sitta tätt ihop. Samtidigt började celler visa DNA-skadesignaler såsom mikronuclei, fastnade i en kontrollpunkt tidigt i cellcykeln och löpte större risk att genomgå programmerad celldöd. Tillsammans tyder dessa förändringar på att virusets strukturella skal inte bara är ett passivt hölje utan en aktiv sabotör av epitelial stabilitet.
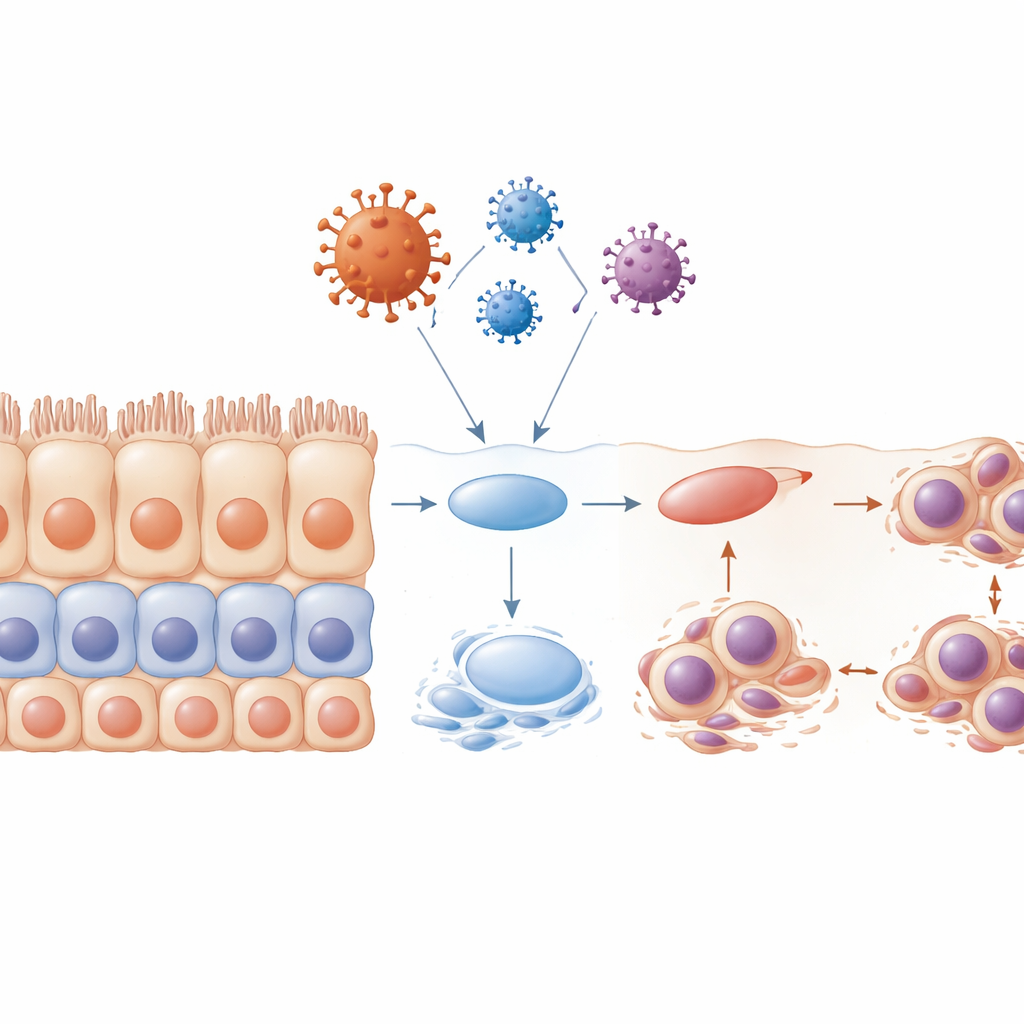
Störd lagring och skadade cellulära "borstar"
Friska flerskiktade epitel förnyar sig genom ett noggrant koreograferat program: progenitorceller delar sig nära basen, sedan rör sig deras avkommor uppåt och mognar till högt specialiserade ytceller. När teamet exponerade celler för envelope-proteinet innan de hade bildat fullständiga lager kollapsade detta program i praktiken. Den resulterande vävnaden var oorganiserad, med dålig lagerbildning, färre mognadsmarkörer och många celler fastnade i en tidig fas av cellcykeln. Många av dessa celler bar missformade eller multipla kärnor och genomgick apoptos, vilket lämnade hål där en kontinuerlig barriär borde finnas. Forskarna undersökte också de små hårliknande strukturerna som kallas cilier, vilka hjälper till att flytta slem och partiklar. De fann att cilier krympte eller försvann, särskilt under påverkan av envelope-proteinet, och att detta skedde i nyckelstadier av cellcykeln. Denna förlust av cilier skulle ytterligare försvaga vävnadens förmåga att rensa virus och föroreningar.
En dold molekylär strömbrytare och ett nytt läkemedelsmål
För att ta reda på hur dessa virusproteiner omkopplar cellbeteendet jämförde författarna proteinnivåer i infekterade och oinfekterade epitelceller. En molekyl, calponin 2 (CNN2), stack konsekvent ut: den ökades starkt av alla tre icke-spikade proteiner och var förhöjd i mun-, lung- och njurvävnader hos COVID-19-patienter. CNN2 hjälper till att organisera cellens inre skelett och svarar på mekanisk stress. När forskarna sänkte CNN2-nivåerna med riktade genetiska verktyg dämpades många av envelope-proteinet skadliga effekter: epitelmarkörer bevarades, vävnadslagren förbättrades och färre celler dog. De spårade sedan CNN2-regleringen uppströms till en transkriptionsfaktor kallad GLIS2, som normalt håller CNN2 i schack. I patientprover och i celler behandlade med virusproteiner var GLIS2-nivåerna märkbart minskade, vilket släppte bromsen på CNN2. Denna GLIS2–CNN2-axel verkar vara en nyckelväg genom vilken SARS-CoV-2:s skalproteiner spårar ur epitelcellers öde.
Vad detta betyder för framtida COVID-19-vård
För icke-specialisten är huvudbudskapet att SARS-CoV-2 tyst kan destabilisera kroppens skyddande beklädnader långt innan tydlig vävnadsskada syns. Dess icke-spikade strukturella proteiner, särskilt envelope-proteinet, får frontlinjens epitelceller att förlora sin specialisering, störa deras ordnade lageruppbyggnad, skada deras DNA och få dem att dö. På molekylär nivå verkar viruset utföra en ”dubbel kapning”: det både dedifferentierar mogna celler och blockerar normal mognad av progenitorceller, till stor del via en GLIS2–CNN2-kontrollknapp. Eftersom CNN2 sitter i en kritisk punkt i denna väg och dess nedreglering kan vända mycket av skadan i laboratoriemodeller framstår det som ett lovande mål för terapier som syftar till att skydda mukosala barriärer vid COVID-19 och möjligen minska envisa sår och organskador.
Citering: Gao, Y., Souza, L.L., Kang, H.S. et al. SARS-CoV-2 nonspike structural proteins hijack mucosa epithelial cell fate. Cell Death Dis 17, 340 (2026). https://doi.org/10.1038/s41419-026-08611-6
Nyckelord: SARS-CoV-2 omslagsprotein, mukosalt epitel, celldedifferentiering, CNN2, GLIS2