Clear Sky Science · es
Las proteínas estructurales no espiga de SARS-CoV-2 secuestran el destino de las células epiteliales mucosas
Cuando los recubrimientos del cuerpo pierden su identidad
La COVID-19 es conocida por atacar los pulmones, pero muchos pacientes también desarrollan úlceras persistentes en la boca, el intestino y otros órganos revestidos por delicadas membranas mucosas. Este estudio plantea una pregunta aparentemente sencilla: antes de que aparezcan heridas visibles e inflamación, ¿qué les sucede exactamente a las células que forman estos revestimientos protectores, y podría ese daño temprano indicar nuevas estrategias de tratamiento?
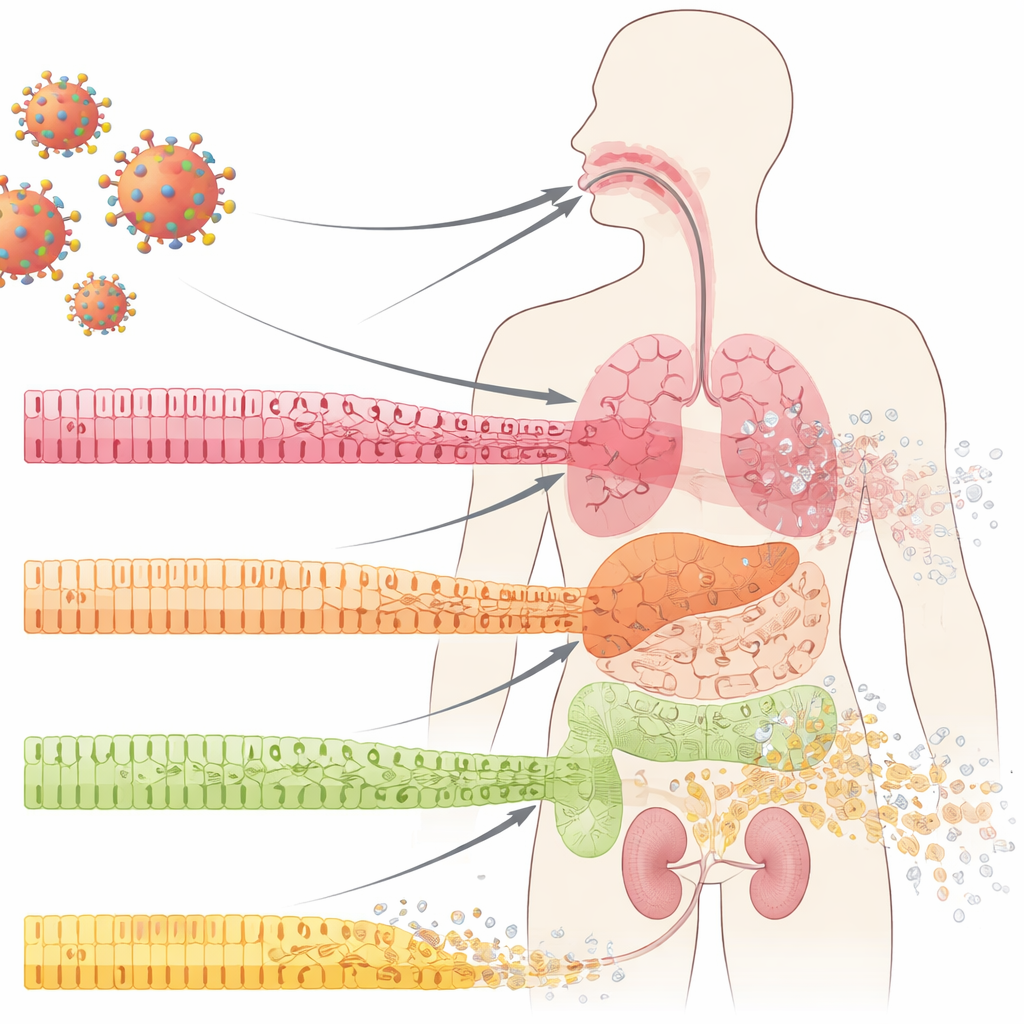
Las células de primera línea que protegen nuestros órganos
Nuestras superficies internas—dentro de la boca, los pulmones, los intestinos y los riñones—están cubiertas por células epiteliales dispuestas en capas ordenadas. Estas células actúan como los azulejos de un muro impermeable: unidas de forma estrecha, especializadas y renovándose constantemente a partir de una reserva de células progenitoras subyacentes. En la COVID-19, los médicos han observado durante tiempo rupturas dramáticas de estas barreras mucosas, incluidas úlceras y erosión tisular. Los autores examinaron muestras de la cavidad oral, los pulmones y los riñones de pacientes con COVID-19 y hallaron algo llamativo incluso en áreas que aún parecían normales en la inspección rutinaria: las células maduras y especializadas estaban perdiendo su identidad, y aumentaban marcadores de células menos maduras, “tipo stem”. Este proceso, denominado desdiferenciación, suele aparecer durante la reparación controlada del tejido, pero aquí surgía al inicio de la infección, antes de una inflamación u cicatrización evidentes.
Proteínas de la capa viral que reprograman el destino celular
El coronavirus es más conocido por su proteína de espiga, que utiliza para entrar en las células. Pero el virus también porta otras proteínas estructurales que forman su capa y su interior. En este trabajo, los investigadores se centraron en tres de estas proteínas “no espiga”: envoltura (E), membrana (M) y nucleocápside (N). Usando modelos 3D sofisticados del mucosa oral humana y tejido de lengua de ratón en cultivo, introdujeron cada una de estas proteínas en células epiteliales para observar qué ocurría. Las tres podían empujar a las células hacia un estado menos diferenciado, pero la proteína de envoltura destacó. Redujo rápidamente los marcadores de células epiteliales maduras, aumentó los marcadores de células más primitivas y debilitó la E-cadherina, una molécula que ayuda a que las células se adhieran firmemente entre sí. Al mismo tiempo, las células comenzaron a mostrar señales de daño en el ADN, como micronúcleos, se quedaron bloqueadas en un punto de control temprano del ciclo celular y tuvieron mayor probabilidad de sufrir muerte celular programada. En conjunto, estos cambios sugieren que la capa estructural del virus no es solo un recubrimiento pasivo, sino un saboteador activo de la estabilidad epitelial.
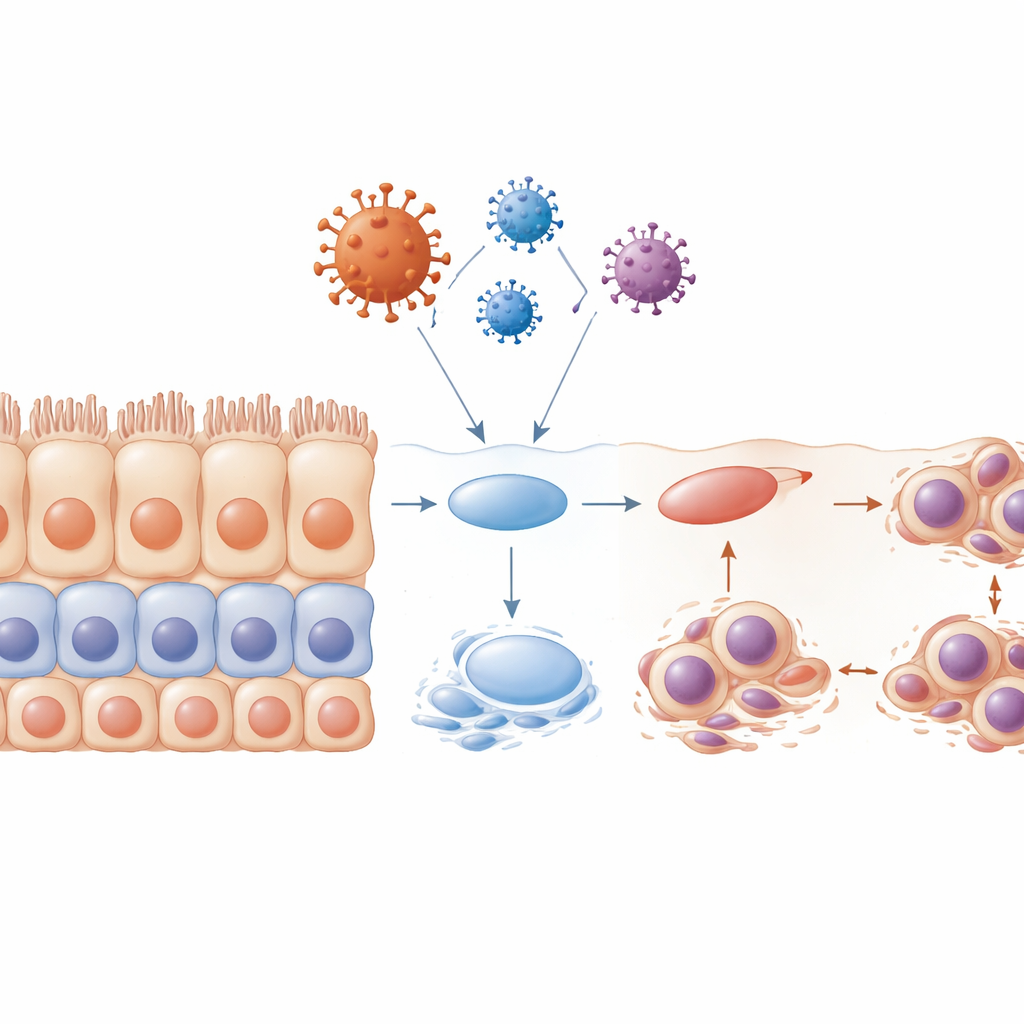
Capas alteradas y “cepillos” celulares dañados
Los epitelios estratificados sanos se renuevan mediante un programa cuidadosamente coreografiado: las células progenitoras se dividen cerca de la base, luego sus descendientes se desplazan hacia arriba y maduran en células superficiales altamente especializadas. Cuando el equipo expuso las células a la proteína de envoltura antes de que hubieran formado capas completas, este programa se vino abajo. El tejido resultante estaba desorganizado, con pobre estratificación, menos marcadores de madurez y muchas células atrapadas en una fase temprana del ciclo celular. Muchas de estas células presentaban núcleos deformados o múltiples y sufrían apoptosis, dejando huecos donde debería existir una barrera continua. Los investigadores también examinaron pequeñas estructuras en forma de pelo llamadas cilios, que ayudan a mover el moco y los desechos. Encontraron que los cilios se encogían o desaparecían, especialmente bajo la influencia de la proteína de envoltura, y que esto ocurría en etapas clave del ciclo celular. Esta pérdida de cilios debilitaría aún más la capacidad del tejido para eliminar virus y contaminantes.
Un interruptor molecular oculto y un nuevo objetivo farmacológico
Para desentrañar cómo estas proteínas virales reconfiguran el comportamiento celular, los autores compararon los perfiles proteicos de células epiteliales infectadas frente a no infectadas. Una molécula, calponina 2 (CNN2), destacó de forma consistente: fue fuertemente aumentada por las tres proteínas no espiga y se encontró elevada en los tejidos oral, pulmonar y renal de pacientes con COVID-19. CNN2 ayuda a organizar el andamiaje interno de la célula y responde al estrés mecánico. Cuando los científicos redujeron los niveles de CNN2 mediante herramientas genéticas dirigidas, muchos de los efectos nocivos de la proteína de envoltura se mitigaron: se preservaron marcadores epiteliales, mejoró la estratificación del tejido y menos células murieron. Luego rastrearon la regulación de CNN2 hacia arriba hasta un factor de transcripción llamado GLIS2, que normalmente mantiene CNN2 bajo control. En muestras de pacientes y en células tratadas con proteínas virales, los niveles de GLIS2 disminuyeron de manera notable, liberando el freno sobre CNN2. Este eje GLIS2–CNN2 parece ser una vía clave por la que las proteínas de la capa de SARS-CoV-2 desvían el destino celular epitelial.
Qué significa esto para la atención futura de la COVID-19
Para un no especialista, el mensaje central es que SARS-CoV-2 puede desestabilizar silenciosamente los recubrimientos protectores del cuerpo mucho antes de que aparezca un daño tisular evidente. Sus proteínas estructurales no espiga, en especial la proteína de envoltura, empujan a las células epiteliales de primera línea a perder su especialización, alteran su estratificación ordenada, dañan su ADN y las eliminan. A nivel molecular, el virus parece ejecutar un “secuestro doble”: desdiferencia células maduras y bloquea la maduración normal de las células progenitoras, en gran medida a través de un interruptor de control GLIS2–CNN2. Dado que CNN2 ocupa un punto crucial en esta vía y su reducción puede revertir gran parte del daño en modelos de laboratorio, surge como un objetivo prometedor para terapias destinadas a proteger las barreras mucosas en la COVID-19 y, posiblemente, reducir úlceras persistentes y lesiones multiorgánicas.
Cita: Gao, Y., Souza, L.L., Kang, H.S. et al. SARS-CoV-2 nonspike structural proteins hijack mucosa epithelial cell fate. Cell Death Dis 17, 340 (2026). https://doi.org/10.1038/s41419-026-08611-6
Palabras clave: proteína de envoltura de SARS-CoV-2, epitelio mucoso, desdiferenciación celular, CNN2, GLIS2