Clear Sky Science · ja
SARS-CoV-2 の非スパイク構造タンパク質が粘膜上皮細胞の運命を乗っ取る
身体の内面の覆いがアイデンティティを失うとき
COVID-19 は肺を攻撃することで知られていますが、多くの患者は口腔、腸管、その他の繊細な粘膜でしつこい潰瘍を発症します。本研究は一見シンプルな疑問を投げかけます:目に見える創傷や炎症が現れる前に、こうした保護上皮を形成する細胞には具体的に何が起きているのか――そしてその早期の損傷は新たな治療戦略の手がかりになるのか?
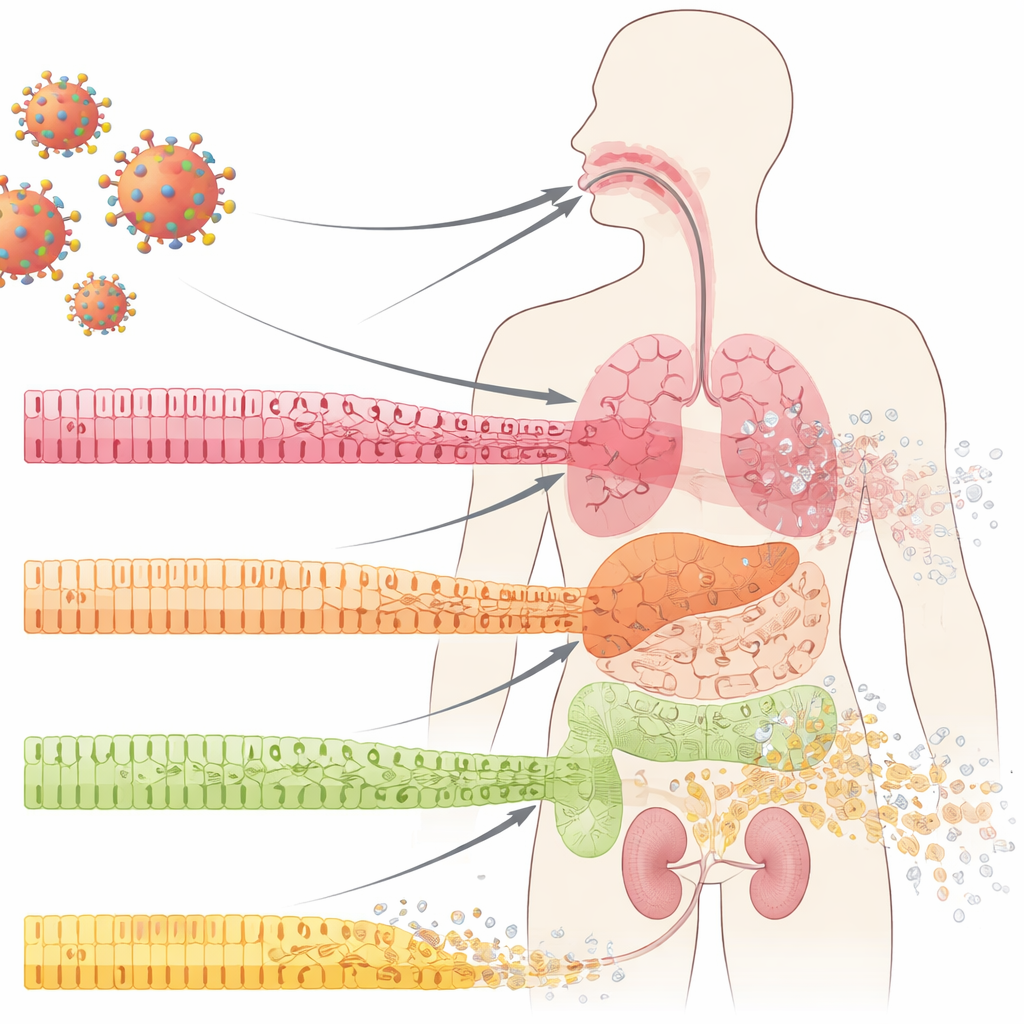
臓器を守る最前線の細胞たち
口腔、肺、腸、腎臓の内部表面は、秩序立った層を成す上皮細胞で覆われています。これらの細胞は防水壁のタイルのように機能し、密に接着し専門化しており、基底にある前駆細胞プールから絶えず更新されます。COVID-19 では、潰瘍や組織の侵食を含むこれらの粘膜バリアの劇的な崩壊が長く報告されてきました。著者らは COVID-19 患者の口腔、肺、腎臓の試料を調べ、通常の検査ではまだ正常に見える領域にも顕著な変化を見出しました:成熟した専門化細胞がそのアイデンティティを失い、より未熟で“幹様”な細胞のマーカーが増えていたのです。この過程は脱分化と呼ばれ、通常は制御された組織修復の際に現れますが、ここでは明らかな炎症や瘢痕化の前、感染の早期に現れていました。
細胞運命を書き換えるウイルスの殻タンパク質
コロナウイルスは細胞へ侵入するためのスパイクタンパク質でよく知られていますが、殻や内部を形成する他の構造タンパク質も運んでいます。本研究では研究者らはこの“非スパイク”タンパク質のうちエンベロープ(E)、膜(M)、ヌクレオカプシド(N)の三つに注目しました。ヒト口腔粘膜の高度な3次元モデルや培養したマウス舌組織を用いて、これらの各タンパク質を上皮細胞に導入し、何が起きるかを観察しました。三者とも細胞をより分化の浅い状態へと傾けることができましたが、特にエンベロープタンパク質が際立っていました。これは成熟上皮マーカーを速やかに低下させ、より原始的な細胞マーカーを増加させ、細胞同士の強い接着を助ける分子であるE-カドヘリンを弱めました。同時に、細胞は小核などのDNA損傷シグナルを示し、細胞周期初期のチェックポイントで滞留し、アポトーシスを起こしやすくなりました。これらの変化は、ウイルスの構造殻が単なる受動的な被覆ではなく、上皮の安定性を能動的に破壊する存在であることを示唆します。
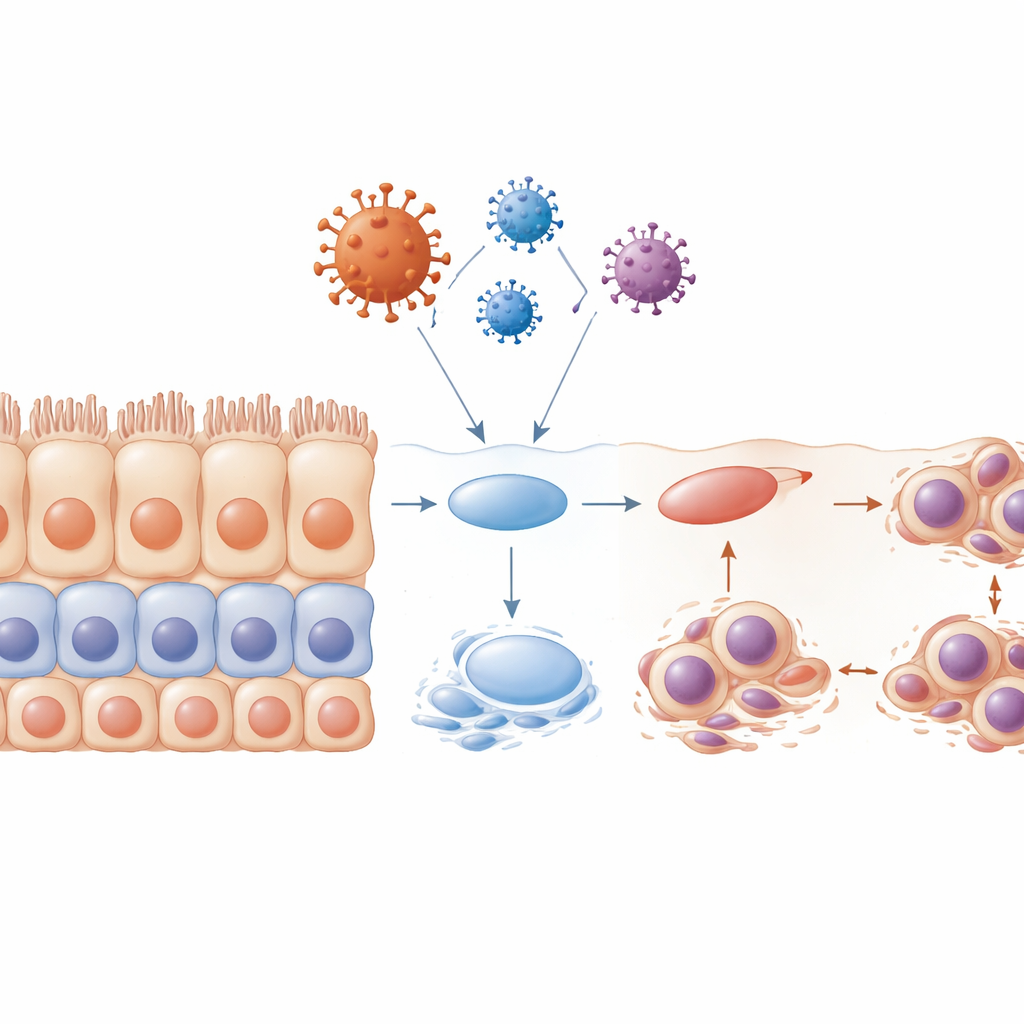
崩れた層構造と損なわれた細胞の“ブラシ”
健康な重層上皮は、前駆細胞が基底近くで分裂し、その子孫が上方へ移動して高度に専門化した表層細胞へ成熟するという、精巧に調整されたプログラムで自己を更新します。研究チームが層を完全に形成する前にエンベロープタンパク質に細胞をさらすと、このプログラムは事実上崩壊しました。結果として得られた組織は配列が乱れ、層構造が不十分で成熟マーカーが減少し、多くの細胞が細胞周期の早期段階に閉じ込められていました。これらの細胞の多くは変形した核や多核を示し、アポトーシスを起こして連続的なバリアがあるべき箇所に隙間を残しました。研究者らは粘液や異物の移動を助ける繊毛と呼ばれる毛状構造も調べ、特にエンベロープタンパク質の影響下で繊毛が縮小・消失し、これは細胞周期の重要な段階で起きていることを明らかにしました。繊毛の喪失はウイルスや汚染物質の排除能力をさらに弱めます。
隠れた分子スイッチと新たな薬剤標的
これらのウイルスタンパク質が細胞挙動を書き換える仕組みを明らかにするため、著者らは感染細胞と未感染細胞のタンパク質プロファイルを比較しました。一つの分子、カルポニン2(CNN2)が一貫して際立っていました:三つの非スパイクタンパク質すべてによって強く増加し、COVID-19 患者の口腔、肺、腎臓組織で高値を示しました。CNN2 は細胞の内部足場を組織化し機械的ストレスに応答する働きを持ちます。研究者らが遺伝学的に CNN2 レベルを低下させると、エンベロープタンパク質による多くの有害な影響が和らぎました:上皮マーカーが維持され、組織の層構造が改善し、細胞死が減少しました。さらに CNN2 の上流での制御をたどると、通常 CNN2 を抑えている転写因子 GLIS2 に行き着きました。患者試料とウイルスタンパク質処理細胞の両方で GLIS2 レベルは著しく低下しており、これが CNN2 に対するブレーキを外していました。この GLIS2–CNN2 軸は、SARS-CoV-2 の殻タンパク質が上皮細胞の運命を破壊する主要な経路であるようです。
今後の COVID-19 治療への示唆
専門外の読者にとって核心となるメッセージは、SARS-CoV-2 が明白な組織損傷が現れるずっと前に、身体の保護上皮を静かに不安定化できるということです。非スパイク構造タンパク質、特にエンベロープタンパク質は、最前線の上皮細胞に専門性を失わせ、層構造を乱し、DNA を損傷させ、細胞を死に追いやります。分子レベルでは、ウイルスは成熟細胞の脱分化を促すとともに前駆細胞の正常な成熟を阻害するという“二重の乗っ取り”を行っているようで、その多くは GLIS2–CNN2 制御スイッチを介しています。CNN2 はこの経路の重要な位置にあり、実験系での抑制が多くの損傷を可逆化するため、粘膜バリアを保護し頑固な潰瘍や多臓器損傷を減らすことを目指した治療の有望な標的として浮上します。
引用: Gao, Y., Souza, L.L., Kang, H.S. et al. SARS-CoV-2 nonspike structural proteins hijack mucosa epithelial cell fate. Cell Death Dis 17, 340 (2026). https://doi.org/10.1038/s41419-026-08611-6
キーワード: SARS-CoV-2 エンベロープタンパク質, 粘膜上皮, 細胞の脱分化, CNN2, GLIS2