Clear Sky Science · pl
Niekolcowe białka strukturalne SARS-CoV-2 przejmują los komórek nabłonka błon śluzowych
Kiedy wyściółki ciała tracą tożsamość
COVID-19 jest znany z atakowania płuc, lecz u wielu pacjentów pojawiają się też uporczywe owrzodzenia w jamie ustnej, przewodzie pokarmowym i innych narządach wyścielonych delikatnymi błonami śluzowymi. W tym badaniu postawiono na pozór proste pytanie: zanim zobaczymy widoczne rany i stan zapalny, co dokładnie dzieje się z komórkami tworzącymi te ochronne wyściółki — i czy wczesne uszkodzenia mogą wskazywać nowe strategie leczenia?
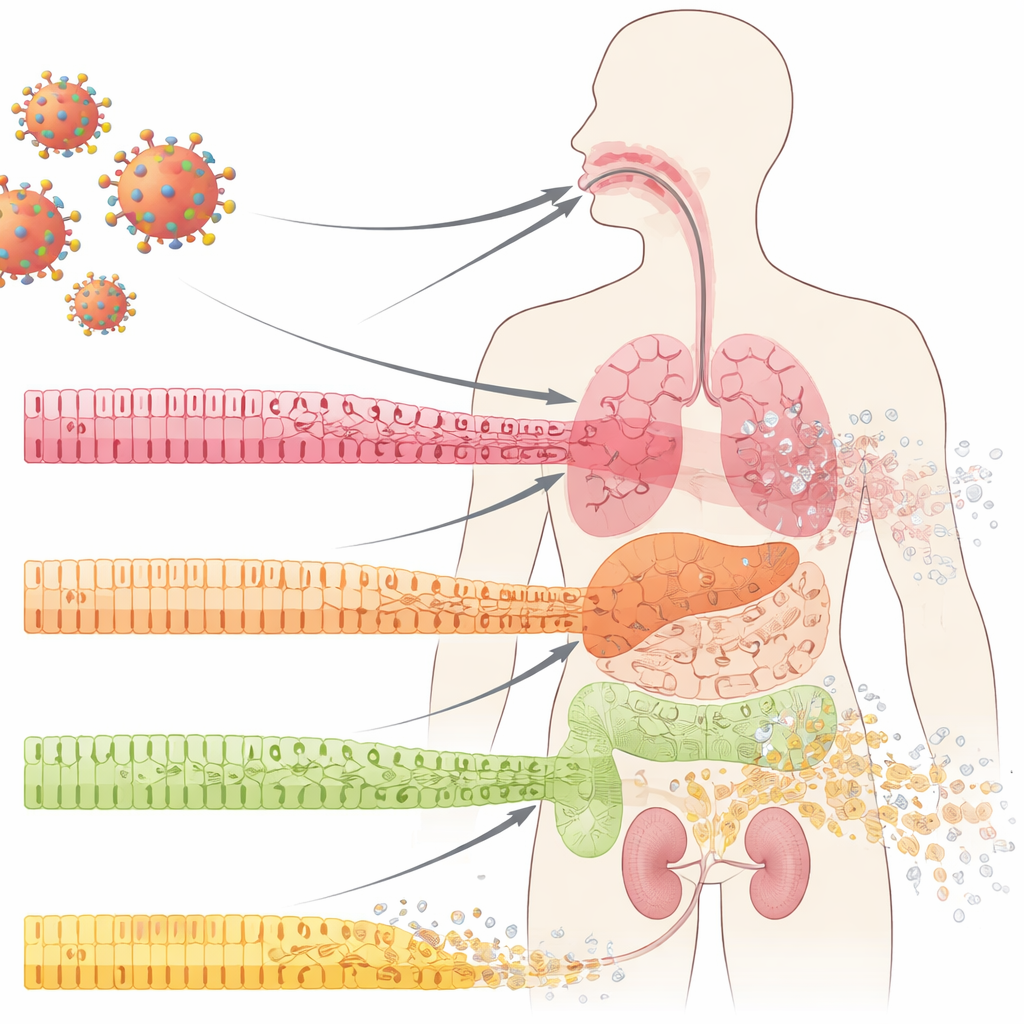
Komórki frontu, które osłaniają nasze narządy
Wnętrza naszego ciała — w jamie ustnej, płucach, jelitach i nerkach — pokryte są komórkami nabłonkowymi ułożonymi w uporządkowane warstwy. Komórki te działają jak płytki w wodoodpornej ścianie: ściśle połączone, wyspecjalizowane i ciągle odnawiane z puli komórek progenitorowych poniżej. W przebiegu COVID-19 lekarze od dawna obserwują dramatyczne załamania tych barier śluzowych, w tym owrzodzenia i erozję tkanek. Autorzy przeanalizowali próbki z jamy ustnej, płuc i nerek pacjentów z COVID-19 i odkryli coś uderzającego nawet w obszarach, które pod rutynową inspekcją wyglądały normalnie: dojrzałe, wyspecjalizowane komórki traciły swoją tożsamość, a wzrastały markery komórek mniej dojrzałych, „podobnych do komórek macierzystych”. Ten proces, zwany dedifferencjacją, zwykle pojawia się podczas kontrolowanej naprawy tkanek — tutaj jednak pojawiał się wcześnie w infekcji, zanim wystąpiły oczywiste objawy zapalenia czy bliznowacenia.
Wirusowe białka osłonki, które przeprogramowują los komórki
Koronawirus jest najbardziej znany ze swojego białka kolca, które wykorzystuje do wnikania do komórek. Wirus niesie jednak także inne białka strukturalne tworzące jego osłonkę i wnętrze. W tej pracy badacze skupili się na trzech „niekolcowych” białkach: otoczkowym (E), błonowym (M) i nukleokapsydowym (N). Korzystając z zaawansowanych trójwymiarowych modeli ludzkiej błony śluzowej jamy ustnej oraz hodowli tkanki języka myszy, wprowadzili każde z tych białek do komórek nabłonkowych, by zobaczyć efekt. Wszystkie trzy mogły przesunąć komórki w kierunku mniej zróżnicowanego stanu, ale białko otoczkowe wyróżniało się najbardziej. Szybko obniżało markery dojrzałych komórek nabłonkowych, zwiększało markery komórek bardziej prymitywnych i osłabiało E-kadherynę — cząsteczkę pomagającą komórkom ściśle się łączyć. Równocześnie komórki zaczęły wykazywać sygnały uszkodzeń DNA, takie jak mikrojądra, utknęły w punkcie kontrolnym we wczesnej fazie cyklu komórkowego i były bardziej podatne na programowaną śmierć komórkową. Razem te zmiany sugerują, że strukturalna osłonka wirusa nie jest jedynie biernym płaszczem, lecz aktywnym sabotażystą stabilności nabłonka.
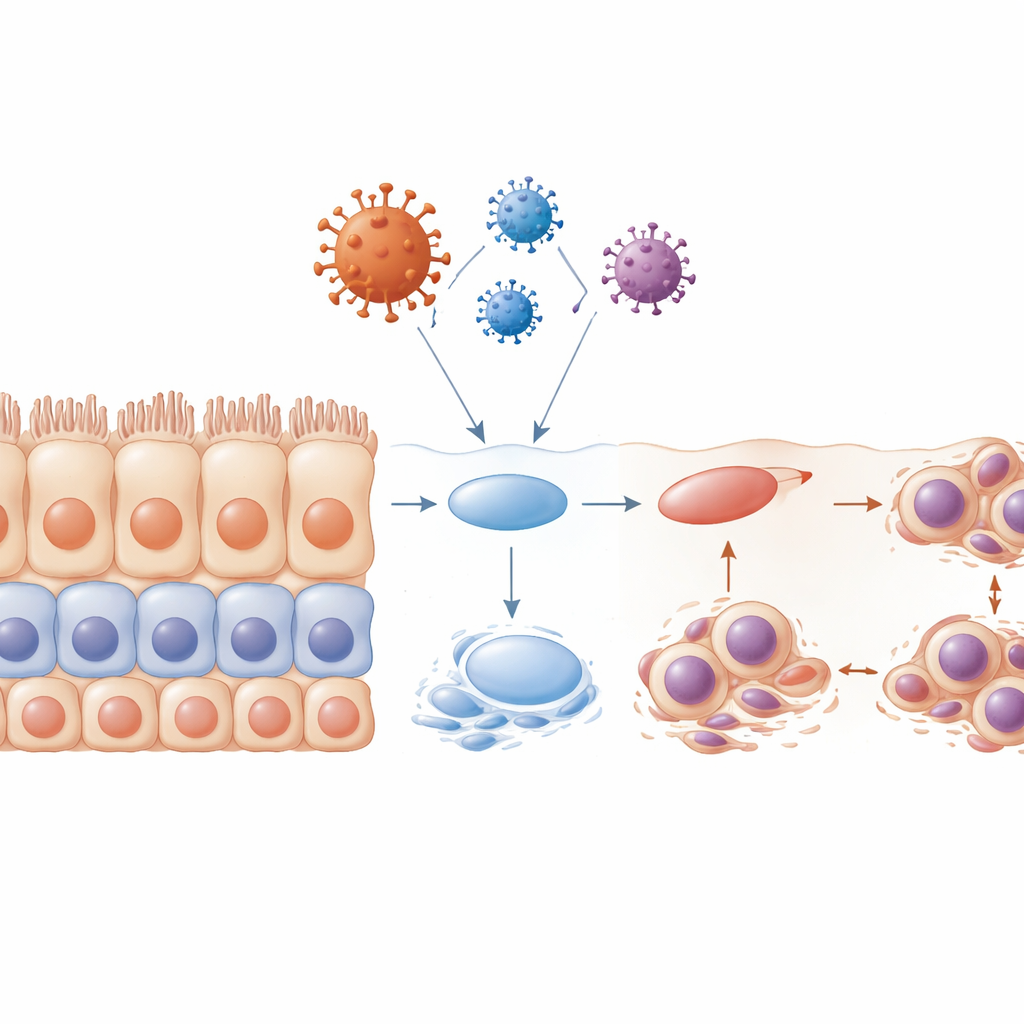
Zaburzone warstwy i uszkodzone „szczoteczki” komórkowe
Zdrowe nabłonki wielowarstwowe odnawiają się poprzez starannie zaprogramowany proces: komórki progenitorowe dzielą się przy podstawie, a ich potomstwo przesuwa się ku górze i dojrzewa do wysoko wyspecjalizowanych komórek powierzchniowych. Gdy zespół wystawił komórki na działanie białka otoczkowego zanim utworzyły pełne warstwy, program ten praktycznie się załamał. Powstała tkanka była zdezorganizowana, z słabym układem warstw, mniejszą liczbą markerów dojrzałości i wieloma komórkami uwięzionymi we wczesnej fazie cyklu komórkowego. Wiele z tych komórek miało zdeformowane lub wielokrotne jądra i przechodziło apoptozę, pozostawiając luki tam, gdzie powinna być ciągła bariera. Badacze przyjrzeli się także drobnym włoskopodobnym strukturom zwanym rzęskami, które pomagają przesuwać śluz i zanieczyszczenia. Stwierdzili, że rzęski kurczyły się lub zanikały, szczególnie pod wpływem białka otoczkowego, i że następowało to na kluczowych etapach cyklu komórkowego. Utrata rzęsek dodatkowo osłabiałaby zdolność tkanki do usuwania wirusów i zanieczyszczeń.
Ukryty przełącznik molekularny i nowy cel farmakologiczny
Aby odkryć, jak te wirusowe białka przełączają zachowanie komórek, autorzy porównali profile białkowe zakażonych i niezakażonych komórek nabłonkowych. Jedna cząsteczka, kalponina 2 (CNN2), konsekwentnie się wyróżniała: była silnie zwiększona przez wszystkie trzy niekolcowe białka i podwyższona w tkankach jamy ustnej, płuc i nerek pacjentów z COVID-19. CNN2 pomaga organizować wewnętrzny szkielet komórki i reaguje na napięcia mechaniczne. Gdy naukowcy zmniejszyli poziom CNN2 przy użyciu ukierunkowanych narzędzi genetycznych, wiele szkodliwych efektów białka otoczkowego zostało stłumionych: markery nabłonkowe zostały zachowane, warstwowanie tkanek poprawiło się, a mniej komórek uległo zgonowi. Następnie prześledzili regulację CNN2 w górę łańcucha do czynnika transkrypcyjnego zwanego GLIS2, który normalnie hamuje CNN2. W próbkach pacjentów i w komórkach traktowanych białkami wirusa poziomy GLIS2 były zauważalnie obniżone, co uwalniało hamulec na CNN2. Ta oś GLIS2–CNN2 wydaje się być kluczową drogą, przez którą białka osłonki SARS-CoV-2 wyprowadzają z toru los komórek nabłonka.
Co to oznacza dla przyszłej opieki nad COVID-19
Dla osoby nietechnicznej główne przesłanie jest takie, że SARS-CoV-2 potrafi cicho destabilizować ochronne wyściółki organizmu na długo przed pojawieniem się oczywistych uszkodzeń tkanek. Jego niekolcowe białka strukturalne, szczególnie białko otoczkowe, zmuszają komórki frontu nabłonka do utraty specjalizacji, zaburzają ich uporządkowane warstwowanie, uszkadzają DNA i powodują ich śmierć. Na poziomie molekularnym wirus wydaje się realizować „podwójne przejęcie”: zarówno dedifferencjuje komórki dojrzałe, jak i blokuje prawidłowe dojrzewanie komórek progenitorowych, w dużej mierze poprzez przełącznik kontrolny GLIS2–CNN2. Ponieważ CNN2 znajduje się w kluczowym punkcie tej ścieżki, a jego redukcja może odwrócić większość szkód w modelach laboratoryjnych, wyrasta on na obiecujący cel terapii mających chronić bariery błon śluzowych w COVID-19 i potencjalnie zmniejszać uporczywe owrzodzenia oraz uszkodzenia wielonarządowe.
Cytowanie: Gao, Y., Souza, L.L., Kang, H.S. et al. SARS-CoV-2 nonspike structural proteins hijack mucosa epithelial cell fate. Cell Death Dis 17, 340 (2026). https://doi.org/10.1038/s41419-026-08611-6
Słowa kluczowe: białko otoczkowe SARS-CoV-2, nabłonek błon śluzowych, dedifferencjacja komórek, CNN2, GLIS2