Clear Sky Science · zh
RASSF1C–HIF-1α 轴驱动巨噬细胞脂质代谢以促进胰腺癌
这则癌症研究为何重要
胰腺癌是最致命的癌症之一,部分原因是它藏得很深,常在晚期才被发现。但其侵袭性并不仅仅源于肿瘤细胞本身。本研究展示了肿瘤内部缺氧如何重新编程肿瘤细胞及其邻近的免疫细胞,从而助长肿瘤生长与转移。通过揭示这一连锁反应,研究者指明了可通过同时针对肿瘤代谢与免疫系统的新型治疗策略。
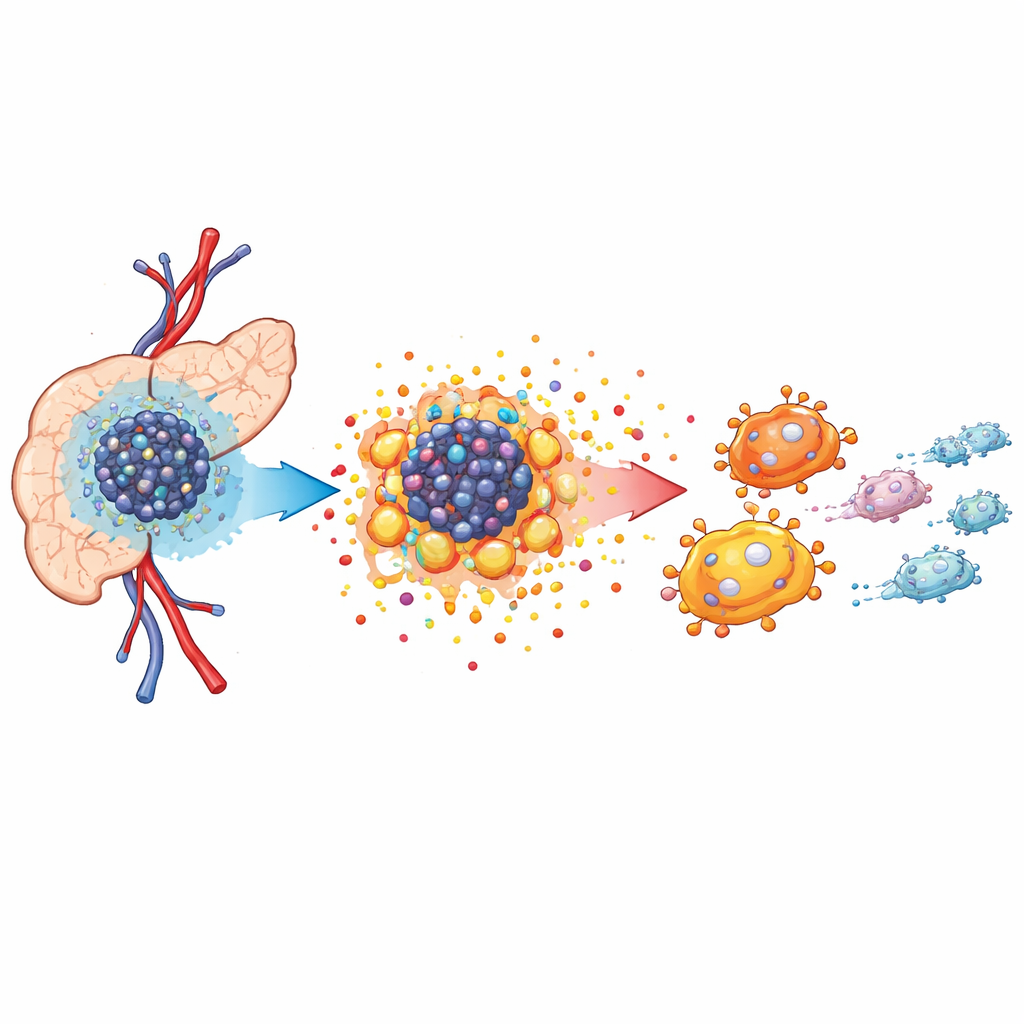
低氧与饥饿的肿瘤“街区”
胰腺肿瘤生长在一种拥挤且不利的环境中,称为肿瘤微环境。血供匮乏导致氧气下降,迫使癌细胞改变能量获取方式。作者在小鼠模型中结合单细胞 RNA 测序与空间定位,发现肿瘤组织中充斥着癌细胞、癌相关成纤维细胞以及一种称为肿瘤相关巨噬细胞的特殊免疫细胞。这些巨噬细胞聚集在癌细胞附近,往往采取支持肿瘤生长而非对抗癌症的角色。分析显示,癌细胞高度依赖改变后的代谢来驱动快速生长,从而为更大范围的组织重塑奠定基础。
用糖和酸为癌症供能
在氧气匮乏时,癌细胞依赖一种类似于快速但低效的糖类燃烧过程,通常称为瓦尔堡效应。研究团队发现,一种先前与癌症行为相关的蛋白变体 RASSF1C 在低氧条件下被强烈激活。在另一个氧感蛋白 HIF-1α 的驱动下,RASSF1C 增强糖酵解,导致大量乳酸产生并使周围环境酸化。在细胞和动物实验中,下调 RASSF1C 可减少酸性产物并减慢肿瘤生长,而上调则有相反效果。重要的是,用药物阻断乳酸形成可以削弱 RASSF1C 带来的生长优势,表明这种代谢转变并非单纯副作用,而是积极推动疾病进展。
肿瘤副产物如何重编程免疫细胞
肿瘤细胞释放的乳酸不仅改变局部化学环境,它还充当信号。当研究者用富含乳酸的胰腺癌细胞条件培养液处理巨噬细胞时,巨噬细胞转向类似 M2 的肿瘤支持状态。它们产生更多抗炎因子,减少与攻击和清除癌细胞相关的分子。在小鼠中,高 RASSF1C 水平的肿瘤含有更多这类促肿瘤巨噬细胞,而阻断乳酸生成可抑制这一效应。进一步测试显示,乳酸还重塑了巨噬细胞的脂质与胆固醇处理方式,增加脂质积累,这种变化与更有利于肿瘤生长与转移的微环境一致。
免疫细胞内的一个隐秘稳定性开关
深入研究发现了一个将肿瘤代谢与免疫细胞行为连接起来的分子开关。一种关键免疫调节因子 IRF7——通常支持更警觉、准备攻击的巨噬细胞状态并维持健康的脂质代谢——在胰腺肿瘤中呈低表达。来自癌细胞的乳酸使巨噬细胞内的 IRF7 蛋白变得不稳定并加速降解。这一过程依赖于另一种蛋白 UFL1,UFL1 附加一个小标签(UFM1)以保护 IRF7 不被标记为降解对象。乳酸在巨噬细胞中抑制了 UFL1,使平衡倾向于将 IRF7 送往细胞的蛋白质降解通路。缺乏稳定的 IRF7,巨噬细胞在代谢上出现缺陷,更容易协助肿瘤细胞迁移并侵入周围组织。
对未来治疗的启示
在来自胰腺癌患者的肿瘤样本中,研究者观察到明显的模式:肿瘤细胞中 RASSF1C 与 HIF-1α 水平升高,而周围组织中 UFL1 与 IRF7 水平降低。这些模式与疾病更晚期及转移特征相符。总体来看,研究勾勒出一条链条:低氧激活 RASSF1C 与 HIF-1α,驱动乳酸过量生成,继而在巨噬细胞内破坏保护性的 UFL1–IRF7 制动机制。对非专业读者而言,结论是胰腺癌通过将自身的废弃物转化为武器来钝化周围免疫细胞。中断这一链条——通过限制乳酸、阻断 RASSF1C–HIF-1α 信号或稳定 IRF7——可能为将代谢药物与免疫疗法结合的新型治疗方案打开道路。
引用: Zhan, T., Huang, M., Chen, M. et al. The RASSF1C-HIF-1α axis drives macrophage lipid metabolism to promote pancreatic cancer. Cell Death Dis 17, 430 (2026). https://doi.org/10.1038/s41419-026-08609-0
关键词: 胰腺癌, 肿瘤微环境, 肿瘤代谢, 巨噬细胞, 乳酸