Clear Sky Science · pl
Oś RASSF1C–HIF-1α napędza metabolizm lipidów w makrofagach, wspierając raka trzustki
Dlaczego ta historia o raku ma znaczenie
Rak trzustki należy do najgroźniejszych nowotworów, częściowo dlatego, że rozwija się głęboko w ciele i często jest wykrywany zbyt późno. Jednak jego agresywność to nie tylko cecha komórek nowotworowych. Badanie pokazuje, jak niedobór tlenu w obrębie guzów trzustki przebudowuje zarówno komórki nowotworowe, jak i pobliskie komórki odpornościowe w sposób sprzyjający rozwojowi i szerzeniu się choroby. Odkrycie tego łańcucha zdarzeń wskazuje nowe możliwości ataku na chorobę poprzez jednoczesne ukierunkowanie metabolizmu guza i układu odpornościowego.
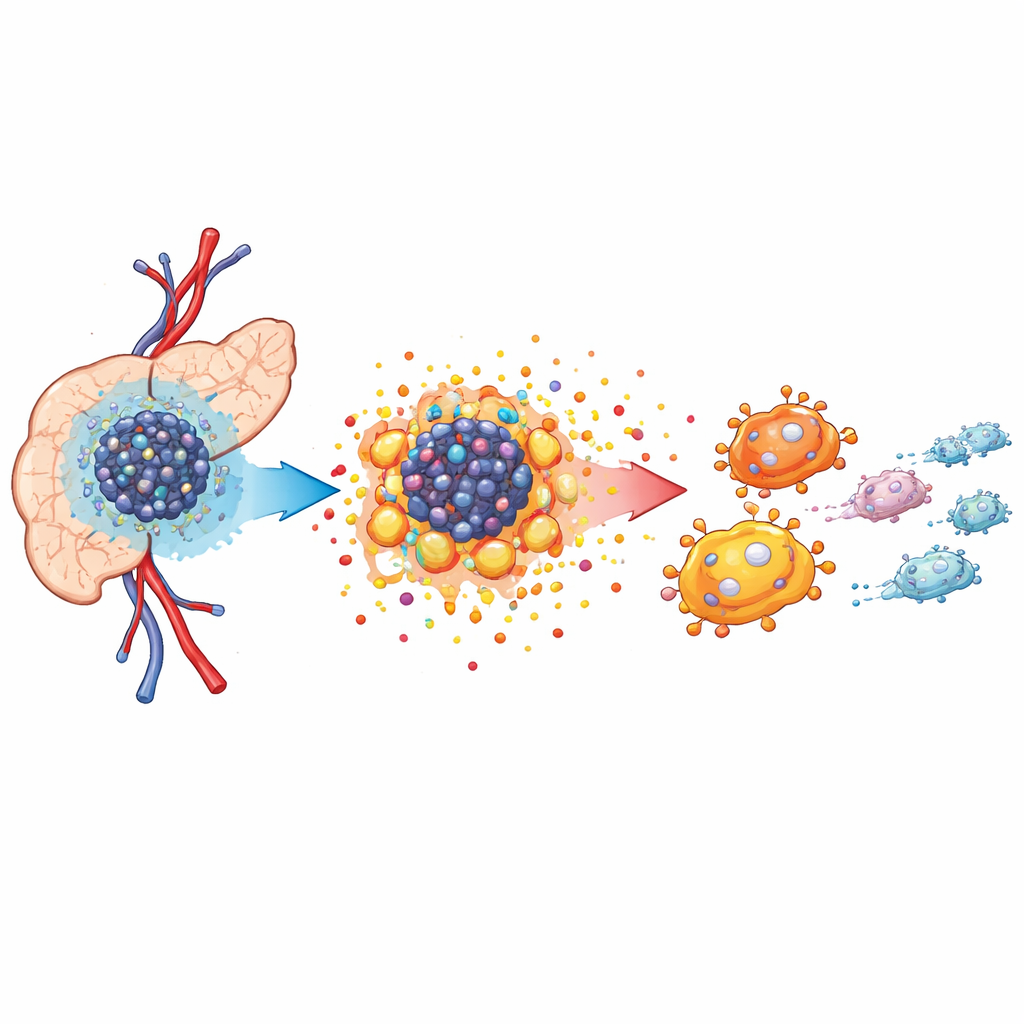
Mało tlenu i wygłodniałe sąsiedztwo guza
Guzy trzustki rozwijają się w zatłoczonym, wrogim otoczeniu zwanym mikrośrodowiskiem guza. Układ krwionośny jest ubogi, więc poziom tlenu spada, zmuszając komórki nowotworowe do zmiany sposobu pozyskiwania energii. Przy użyciu sekwencjonowania RNA pojedynczych komórek i mapowania przestrzennego w modelach mysich autorzy wykazali, że tkanka guza jest wypełniona komórkami nowotworowymi, fibroblastami związanymi z rakiem oraz wyspecjalizowanymi komórkami odpornościowymi zwanymi makrofagami związanymi z guzem. Te makrofagi skupiają się blisko komórek nowotworowych i mają skłonność do przyjmowania roli wspierającej wzrost, zamiast zwalczania nowotworu. Analiza ujawniła, że komórki nowotworowe silnie polegają na zmienionym metabolizmie, by zasilać szybki wzrost, co przygotowuje grunt pod szerszą przebudowę środowiska tkankowego.
Zasilanie raka cukrem i kwasem
Gdy brakuje tlenu, komórki nowotworowe opierają się na procesie przypominającym szybkie, mało wydajne spalanie cukru, często nazywanym efektem Warburga. Zespół badawczy odkrył, że wariant białka o nazwie RASSF1C, wcześniej powiązany z zachowaniem nowotworu, ulega silnej aktywacji w warunkach niskiego tlenu. Pobudzany przez inny czujnik tlenu, białko HIF-1α, RASSF1C zwiększa glikolizę, prowadząc do wysokiej produkcji mleczanu i zakwaszenia otoczenia. W eksperymentach na komórkach i zwierzętach wyciszenie RASSF1C zmniejszało produkcję kwasu i spowalniało wzrost guza, podczas gdy jego wzmocnienie miało efekt przeciwny. Co istotne, blokowanie powstawania mleczanu lekiem osłabiało przewagę wzrostową nadawaną przez RASSF1C, pokazując, że ta zmiana metaboliczna nie jest jedynie efektem ubocznym — aktywnie napędza progresję choroby.
Jak produkty uboczne guza przeprogramowują komórki odpornościowe
Mleczan uwalniany przez komórki nowotworowe robi więcej niż zmienia lokalną chemię; działa też jako sygnał. Gdy badacze hodowali makrofagi w pożywce od komórek raka trzustki bogatych w mleczan, makrofagi przeszły w stan przypominający M2, wspierający guz. Produkowały więcej czynników przeciwzapalnych i mniej cząsteczek związanych z atakiem i eliminacją komórek nowotworowych. U myszy guzy o wysokim poziomie RASSF1C zawierały więcej takich pronowotworowych makrofagów, efekt który można było osłabić przez blokowanie produkcji mleczanu. Dalsze testy wykazały, że mleczan przeprogramowuje także sposób, w jaki makrofagi gospodarują tłuszczami i cholesterolem, zwiększając akumulację lipidów w sposób zgodny z tworzeniem się bardziej sprzyjającej niszy dla wzrostu i rozsiewu guza.
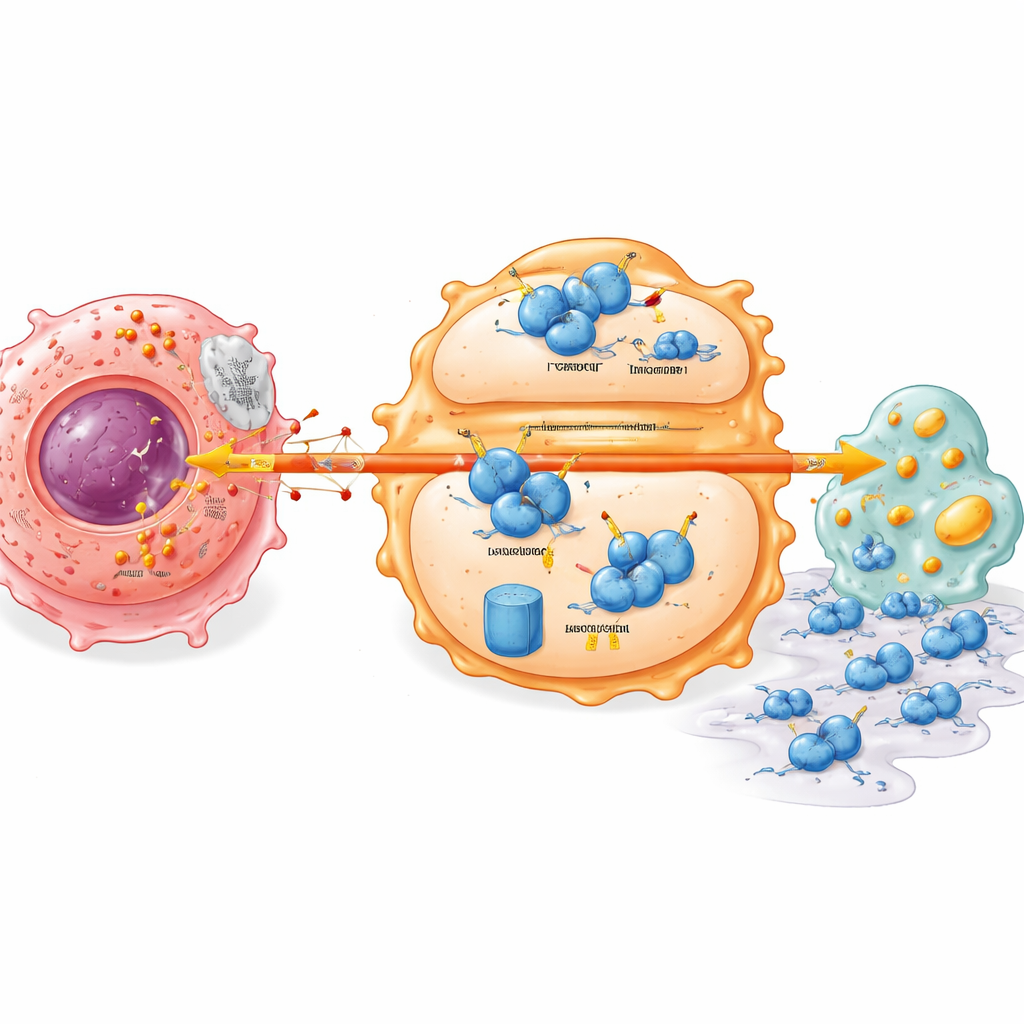
Ukryty przełącznik stabilności w komórkach odpornościowych
Dążąc dalej, badanie odkryło molekularny przełącznik łączący metabolizm guza z zachowaniem komórek odpornościowych. Kluczowy regulator odpornościowy zwany IRF7, który normalnie wspiera bardziej czujny, gotowy do ataku stan makrofagów i prawidłowe zarządzanie lipidami, występował na niskich poziomach w guzach trzustki. Mleczan pochodzący z komórek nowotworowych powodował, że białko IRF7 w makrofagach stawało się niestabilne i ulegało szybszemu rozkładowi. Zależało to od innego białka, UFL1, które przyłącza mały znacznik (UFM1) chroniący IRF7 przed oznaczeniem do zniszczenia. Mleczan tłumił UFL1 w makrofagach, przechylając równowagę w kierunku systemu znakowania wysyłającego IRF7 do komórkowej „niszczarki białek”. Bez stabilnego IRF7 makrofagi gromadzą defekty metaboliczne i chętniej wspomagają migrację komórek nowotworowych oraz naciekanie otaczających tkanek.
Co to oznacza dla przyszłych terapii
W próbkach guzów od pacjentów z rakiem trzustki badacze zaobserwowali wyraźny wzorzec: wyższe poziomy RASSF1C i HIF-1α w komórkach nowotworowych oraz niższe poziomy UFL1 i IRF7 w tkance otaczającej. Wzorce te korelowały z bardziej zaawansowaną chorobą i cechami przerzutowymi. Łącznie wyniki opisują łańcuch, w którym niski poziom tlenu aktywuje RASSF1C i HIF-1α, napędza nadprodukcję mleczanu, a to z kolei dezaktywuje ochronny hamulec UFL1–IRF7 w makrofagach. Dla czytelników niebędących specjalistami najważniejszy wniosek jest taki: rak trzustki wykorzystuje produkty odpadowe własnego metabolizmu jako broń, by unieszkodliwiać pobliskie komórki odpornościowe. Przerwanie tego łańcucha — poprzez ograniczenie mleczanu, blokowanie sygnalizacji RASSF1C–HIF-1α lub stabilizację IRF7 — może otworzyć nowe drogi terapii łączące leki metaboliczne z podejściami immunologicznymi.
Cytowanie: Zhan, T., Huang, M., Chen, M. et al. The RASSF1C-HIF-1α axis drives macrophage lipid metabolism to promote pancreatic cancer. Cell Death Dis 17, 430 (2026). https://doi.org/10.1038/s41419-026-08609-0
Słowa kluczowe: rak trzustki, mikrośrodowisko guza, metabolizm guza, makrofagi, mleczan