Clear Sky Science · pt
O eixo RASSF1C-HIF-1α dirige o metabolismo lipídico de macrófagos para promover o câncer de pâncreas
Por que essa história sobre câncer é importante
O câncer de pâncreas está entre os mais letais, em parte porque fica bem escondido no interior do corpo e muitas vezes é detectado tardiamente. Mas sua agressividade não depende apenas das células tumorais. Este estudo mostra como a falta de oxigênio dentro dos tumores pancreáticos reorganiza tanto as células cancerosas quanto as células imunes vizinhas de modo a favorecer o crescimento e a disseminação do câncer. Ao desvendar essa cadeia de eventos, os pesquisadores apontam novas maneiras de atacar a doença, atuando tanto no metabolismo tumoral quanto no sistema imunológico.
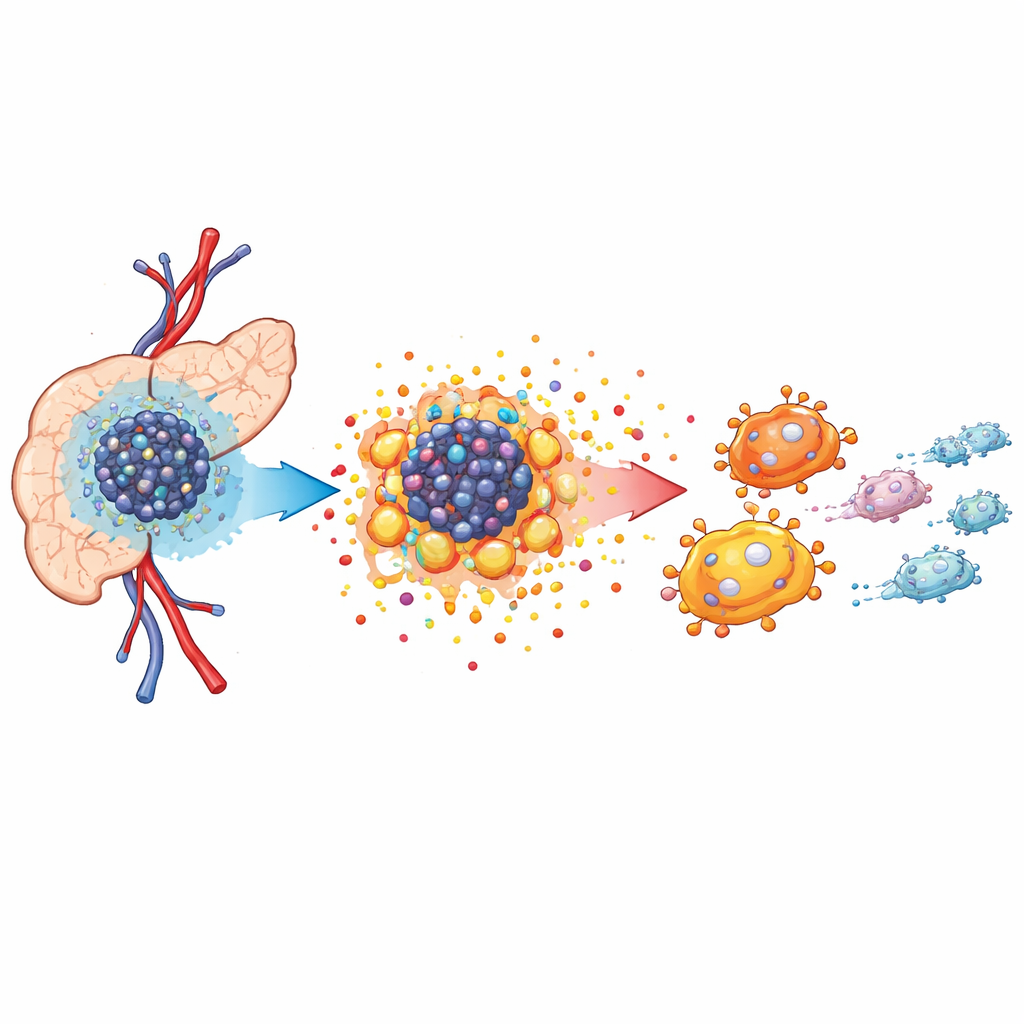
Baixo oxigênio e um bairro tumoral faminto
Os tumores pancreáticos crescem em um ambiente lotado e hostil conhecido como microambiente tumoral. O suprimento sanguíneo é pobre, portanto os níveis de oxigênio caem, forçando as células cancerosas a alterar como produzem energia. Usando RNAseq de célula única e mapeamento espacial em modelos murinos, os autores mostraram que o tecido tumoral está repleto de células cancerosas, fibroblastos associados ao tumor e células imunes especializadas chamadas macrófagos associados ao tumor. Esses macrófagos se agrupam perto das células cancerosas e tendem a assumir um papel de suporte ao crescimento, em vez de combate ao câncer. A análise revelou que as células tumorais dependem fortemente de um metabolismo alterado para sustentar o crescimento rápido, preparando o terreno para uma remodelação mais ampla do tecido.
Alimentando o câncer com açúcar e ácido
Quando o oxigênio é escasso, as células tumorais recorrem a um processo parecido com a queima rápida e ineficiente de açúcar, frequentemente chamado de efeito Warburg. A equipe descobriu que uma variante proteica denominada RASSF1C, previamente associada ao comportamento canceroso, torna-se fortemente ativada em condições de baixo oxigênio. Impulsionada por outra proteína sensora de oxigênio, HIF-1α, RASSF1C estimula a glicólise, levando à alta produção de lactato e acidificação do ambiente. Em experimentos celulares e em animais, reduzir a expressão de RASSF1C diminuiu a produção de ácido e retardou o crescimento tumoral, enquanto aumentá‑la teve o efeito oposto. Importante, bloquear a formação de lactato com um fármaco atenuou a vantagem de crescimento conferida por RASSF1C, mostrando que essa mudança metabólica não é apenas um efeito colateral — ela alimenta ativamente a progressão da doença.
Como os subprodutos tumorais reprogramam células imunes
O lactato liberado pelas células tumorais faz mais do que alterar a química local; age como um sinal. Quando os pesquisadores expuseram macrófagos a meio condicionado por células de câncer pancreático ricas em lactato, os macrófagos migraram para um estado do tipo M2, de suporte ao tumor. Produziram mais fatores anti‑inflamatórios e menos moléculas associadas ao ataque e à eliminação de células cancerosas. Em camundongos, tumores com altos níveis de RASSF1C continham mais desses macrófagos pró‑tumorais, um efeito que pôde ser reduzido ao bloquear a produção de lactato. Testes adicionais mostraram que o lactato também reprogramou o manejo de gorduras e colesterol pelos macrófagos, aumentando o acúmulo lipídico de formas que se correlacionam com um nicho mais favorável ao crescimento e à disseminação tumoral.
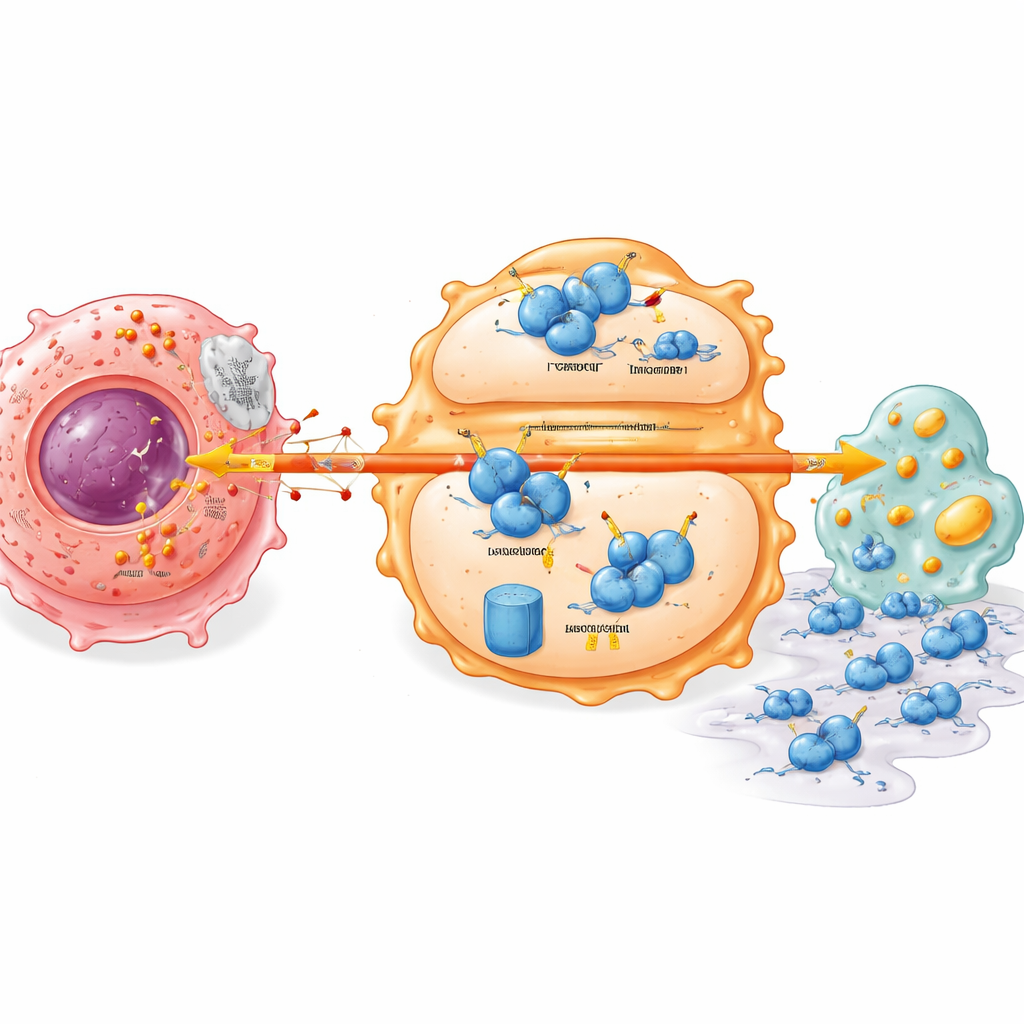
Um interruptor de estabilidade oculto dentro das células imunes
Ao aprofundar, o estudo revelou um interruptor molecular que conecta o metabolismo tumoral ao comportamento das células imunes. Um regulador imune chave chamado IRF7, que normalmente sustenta um estado mais vigilante e agressivo dos macrófagos e um manejo lipídico saudável, foi encontrado em níveis baixos nos tumores pancreáticos. O lactato das células cancerosas tornou a proteína IRF7 nos macrófagos instável e acelerou sua degradação. Isso dependia de outra proteína, UFL1, que anexa uma pequena marca (UFM1) que protege IRF7 de ser marcada para destruição. O lactato suprimiu UFL1 nos macrófagos, inclinando o equilíbrio para um sistema de marcação que envia IRF7 ao “triturador” proteico da célula. Sem IRF7 estável, os macrófagos acumulam defeitos metabólicos e mais facilmente auxiliam as células tumorais na migração e invasão dos tecidos vizinhos.
O que isso significa para tratamentos futuros
Em amostras tumorais de pessoas com câncer de pâncreas, os pesquisadores observaram um padrão claro: níveis mais altos de RASSF1C e HIF-1α nas células tumorais e níveis mais baixos de UFL1 e IRF7 no tecido circundante. Esses padrões corresponderam a doença mais avançada e características metastáticas. Em conjunto, os achados descrevem uma cadeia em que o baixo oxigênio ativa RASSF1C e HIF-1α, impulsiona a superprodução de lactato e, por sua vez, desativa o freio protetor UFL1–IRF7 dentro dos macrófagos. Para leitores leigos, a conclusão é que o câncer de pâncreas prospera transformando seus próprios resíduos em armas que desarmam as células imunes vizinhas. Interromper essa cadeia — limitando o lactato, bloqueando a sinalização RASSF1C–HIF-1α ou estabilizando IRF7 — pode abrir novas vias para terapias que combinem drogas metabólicas com abordagens baseadas no sistema imunológico.
Citação: Zhan, T., Huang, M., Chen, M. et al. The RASSF1C-HIF-1α axis drives macrophage lipid metabolism to promote pancreatic cancer. Cell Death Dis 17, 430 (2026). https://doi.org/10.1038/s41419-026-08609-0
Palavras-chave: câncer de pâncreas, microambiente tumoral, metabolismo tumoral, macrófagos, lactato